Capsaicin og dens effekt på treningsytelse, tretthet og betennelse
Mar 26, 2022
Ta kontakt med:joanna.jia@wecistanche.com/ WhatsApp: 008618081934791
Gaia Giuriato 1,2, Massimo Venturelli 1,3, Alexs Matias 2, Edgard MKVK Soares 2,4, Jessica Gaetgens 5, Kimberley A. Frederick 5 og Stephen J. Ives 2,*
Abstrakt:Capsaicin (CAP) aktiverer den forbigående reseptorpotensialet vanilloid 1 (TRPV1) kanal på sensoriske nevroner, og forbedrer ATP-produksjon, vaskulær funksjon, utmattelsesmotstand og dermed treningsytelse. Imidlertid forblir de underliggende mekanismene for CAP-induserte ergogene effekter og tretthetsmotstand unnvikende. For å evaluere de potensielle anti-tretthetseffektene av CAP, utførte 10 unge, friske menn tester med konstant belastning av sykling, tid til utmattelse (TTE) (85 prosent maksimal arbeidsrate) etter inntak av placebo (PL; fiber) eller CAP-kapsler i et blindet, motbalansert, crossoverdesign, mens kardiorespiratoriske responser ble overvåket. Fatigue ble vurdert med interpolatedtwitch-teknikken, pre-post trening, under isometriske maksimale frivillige sammentrekninger (MVC). Ikke-signifikante forskjeller (p > 0,05) ble påvist i kardiorespiratoriske responser og selvrapportert tretthet (RPE-skala) under tidsforsøket eller i TTE (henholdsvis 375 ± 26 og 327 ± 36 s). CAP dempet reduksjonen i potensierte rykninger (PL: −52 ± 6 vs. CAP: −42 ± 11 prosent , p=0.037), og hadde en tendens til å dempe nedgangen i maksimal avslapningshastighet (PL: −47 ± 33 vs. CAP: -29 ± 68 prosent, p=0.057), men ikke en maksimal hastighet for kraftutvikling, MVC eller frivillig muskelaktivering. Dermed kan CAP dempe nevromuskulær tretthet gjennom endringer i afferent signalering eller nevromuskulær avslapningskinetikk, kanskje mediert via det sarko-endoplasmatiske retikulum Ca2 pluss ATPase (SERCA) pumper, og dermed øke hastigheten på Ca2 pluss gjenopptak og avslapning.
Nøkkelord: motoneuron; afferent; skjelettmuskulatur; hjerteutgang; ventilasjon; metabolisme; perfusjon

Cistanche kosttilskuddhar enanti-tretthetseffekt.
1. Introduksjon
Den primære skarpe bioaktive ingrediensen i paprika, capsaicin (CAP), har lenge vært ansett for sitt terapeutiske potensial. Capsaicin (8-metyl-N-vanillyl-trans-6-ingen amid) er klassisk beskrevet som et irritasjonsmiddel og er en velkjent endogen aktivator av den forbigående reseptorpotensialet vanilloid type 1 (TRPV1) på sensoriske nevronmodulerende signaler for varme og/eller smerte. Eksponering for CAP utløser en potent nevronalkalsiumtilstrømning, ofte etterfulgt av en refleks nedregulering av TRPV1-aktiviteten [1–3]. Av denne grunn er CAP et lovende klinisk verktøy for å modulere TRPV1-relaterte veier, fra smerteoppfatning [1–4], betennelse [5] og immunitet [6], til de fleste alvorlige patologier som schizofreni [7], angst, depresjon [8], fedme [9] og kronisk tretthet [10]. Inntak av CAP øker termogenese ved å stimulere katekolaminsekresjon fra binyremargen, redusere adipogenese og forbedre energimetabolismen [11–15], forbedre mitokondriell biogenese og adenosintrifosfat (ATP) syntese, og er til og med foreslått å forbedre helsemarkører for kardiovaskulære [16–20] ].
Hos gnagere fremkaller CAP en spontan aktiv atferd, øker grepstyrken og svømmetiden til utmattelse på en doseavhengig måte [21–24]. Disse forbedringene i fysisk ytelse var korrelert til økninger i leverglykogeninnholdet [21], sannsynligvis som et resultat av glykogensparing [24] og økt fettsyreutnyttelse på grunn av CAP-indusert adrenal katekolaminsekresjon [22]. Studier på mus viste dessuten at TRPV1-aktiveringen ved CAP-administrasjon oppregulerer PGC-1, fremmer mitokondriell biogenese, øker bidraget til oksidativ ATP-produksjon og oppregulerer uttrykket av oksidative fibre i skjelettmuskulaturen [25,26]. I en murin modell formidles CAP-indusert muskelavslapning via en direkte hemmende virkning på de spenningsdrevne Ca2 pluss-kanalene inne i cellen [4]. I tillegg nedregulerer en enkelt høy dose CAP uttrykket av det mitokondrielle frakoblingsproteinet UCP3, og reduserer ATP-kostnadene ved sammentrekning, til tross for en uendret, og til tider økt, generering av elektrisk rykningskraft [25,27]. Selv om CAP har blitt mye studert i celle- og murinemodeller, har dens akutte in vivo fysiologiske effekter i kombinasjon med trening fått relativt minimal oppmerksomhet, spesielt hos mennesker.
Forskere har utforsket effekten av CAP-inntak og dens innflytelse på forskjellige treningsparadigmer hos friske menn [28–31]. Det har derfor vært noen rapporter om ytelsesforbedringer indusert av inntak av en enkelt dose på 12 mg renset CAP under en 1500-m løpetidsprøve [30], intermitterende trening med høy intensitet [28], og motstandstrening [29] , men ikke under en 10 km løpeprestasjon [31]. I tillegg reduserte CAP vurderingen av opplevd anstrengelse (RPE) under utholdenhets- og motstandsoppgavene, uten forskjeller mellom grupper i laktatkonsentrasjon, noe som tyder på en mulig medierende effekt av CAP på tretthet eller tretthetsfølelse. Tvert imot, Opheim og kolleger observerte ingen effekt av 7 dagers inntak av 28,5 mg CAP på ytelse eller nivå av opplevd tretthet under gjentatte sprintintervaller (15 × 30 m sprint med intervaller på 35 s), men dette doseringsregimet induserte betydelig gastrointestinale plager [32], som fremhever viktigheten av dosering. Videre fokuserte disse nevnte studiene på CAP utelukkende på treningsytelse, og etterlot de underliggende mekanismene til CAP på den utmattende prosessen stort sett uutforsket.
Trening øker sirkulerende konsentrasjoner av spesifikke inflammatoriske cytokiner, f.eks. interleukin-6 (IL-6) og interleukin-1 (IL-1) [33,34], som har blitt foreslått aspotensielle mediatorer av tretthet i sentralnervesystemet ved forskjellige sykdommer [35]. Trening med høy intensitet øker også spytt-amylaseaktivitet [36] og kortisolnivåer [37], som sannsynligvis gjenspeiler den nevroendokrine responsen på trening; kortisol har vist seg å ha anti-inflammatoriske egenskaper, så de inflammatoriske og anti-inflammatoriske responsene bør vurderes sammen. Videre har CAP kjente smertestillende og antiinflammatoriske egenskaper, sammen med kapasiteten til å redusere uttrykket av flere proinflammatoriske cytokiner og kjemokiner [38,39]. Så vidt vi vet har ingen studier til dags dato undersøkt de potensielle mekanismene for CAP-assosierte ytelsesforbedringer, spesielt om CAP kan endre den inflammatoriske eller endokrine responsen på trening og derved påvirke utmattelsesresponsen hos mennesker.
Derfor, gitt mangelen på data, forsøkte vi å utforske den potensielle effekten av akutt oral CAP-forbruk på treningsytelse, tretthet og den inflammatoriske-endokrine responsen ved å bruke en blindet, placebokontrollert, motbalansert crossover-design. Det primære målet med vår studie var å bedre forstå de iboende fysiologiske effektene av capsaicin-administrasjon hos unge, friske individer og for å fylle et tomrom i litteraturen angående den ergogene og tretthetsmotstanden til capsaicin hos mennesker. For å oppnå dette brukte vi twitch-interpolasjonsteknikken for å avsløre omfanget av perifer tretthet og tolke sentralnervesystemets bidrag (frivillig aktivering) til maksimal frivillig sammentrekning. Vi antok at CAP-tilskudd ville forbedre syklingsytelsen og/eller dempe den observerte nevromuskulære trettheten etter en sykkeltreningstid til utmattelsesforsøk ved bruk av den interpolerte rykningsteknikken, som kan skyldes svekket endokrin og inflammatorisk respons på trening.
2. Materialer og metoder
2.1. Emner og generelle prosedyrer
Tretten unge og fysisk aktive menn ble rekruttert til denne studien fra Skid-more College og samfunnet rundt. For å bli inkludert må deltakerne ha vært friske uten noen historie med kardiovaskulære, nevromuskulære, lunge- eller metabolske sykdommer. I tillegg kunne deltakerne ikke være nåværende eller nylig (mindre enn 6 måneder) røykere, ha noen kjente allergier og/eller overdreven følsomhet for krydret mat (dvs. hotpeppers, jalapenos, paprika, etc.) eller fiber (psylliumskall). Deltakernes helsehistorie og kvalifisering ble screenet ved hjelp av helsespørreskjemaer for å vurdere om de er kvalifisert (AHA/ACSMPre-Participation Screening Questionnaire og Physical Activity Readiness Questionnaire[PAR-Q]). Deltakerne ble bedt om å avstå fra å innta vitaminer eller ergogene kosttilskudd (dvs. L-Arginin, Citrulline-Malate, Pre-Workout) minst 2 dager før hvert eksperimentelle besøk, og å avstå fra alkohol og koffein, 24 timer før testing. De ble bedt om å rapportere til laboratoriet 2 timer før testene. Alle deltakerne ga skriftlig informert samtykke før de deltok i studien. Studieprotokollen ble utført i samsvar med de siste revisjonene av Helsinki-erklæringen og ble godkjent av Institutional Review Board (IRB#1807-733) og Institutional Biosafety Committees of Skidmore College.

cistanche ekstrakt pulver
2.2. Eksperimentelt design
Forsøkspersonene rapporterte til laboratoriet på tre forskjellige dager, med minimum 72 timer mellom øktene (se figur 1). Antropometriske og kroppssammensetningsdata ble samlet inn på den første økten ved bruk av luftforskyvningspletysmografi (Bod Pod, Cosmed, Concord, CA, USA) [40]. Deltakerne ble deretter bedt om å utføre en maksimal inkrementell test på et magnetisk bremset syklusergometer (828E, Monark, Cosmed, Vansbro, Sverige) med start på 50 W med trinn på 25 W/min, med en selvvalgt tråkkfrekvens som ble opprettholdt i varigheten av den inkrementelle testen samt påfølgende eksperimentelle forsøk.Testen fortsatte til deltakerne ikke var i stand til å fortsette den foreskrevne arbeidsmengden.På slutten av økten ble deltakerne kjent med de isometriske maksimale frivillige sammentrekningene og de elektrisk fremkalte muskelkontraksjonene. I en enkeltblindet, motbalansert, crossover-design, på dag 2 og 3, ble deltakerne bedt om å innta enten 2 × 390 mg CAP-kapsler (Capsicool, Natures Way, Medley FL, USA) eller 2 × 500 mg placebo-piller (PL; Fiber). , Psyllium Husk, Kirkland Signature, Seattle, WA, USA). Kapslene hadde lignende utseende (f.eks. farge, størrelse osv.), smak (begge var omsluttet med cellulose/hypromellose-kapsler), og ble kodet upåfallende for å sikre blending. Doseringen var i samsvar med produsentens foreslåtte retningslinjer og ble godt tolerert i pilottesting. Tiden til topp i serumkonsentrasjon av CAP etter oralt inntak er ~1 time [41]; av denne grunn ble tretthetsvurdering i hvile vurdert 50 minutter etter pilleinntak for å sikre tilstrekkelig biotilgjengelighet. Dette ble fulgt av en syklingøvelse med konstant belastning (85 prosent av maksimal effekt) til utmattelse (TTE) og en annen utmattelsesvurdering umiddelbart etter trening (mindre enn eller lik 60 s). Den nevromuskulære vurderingen besto av 6 maksimale frivillige kontraksjoner (MVC) og overlagrede rykninger, pre- og post-time-to-exhaustion-forsøk. Sykkeltesten ble avsluttet da forsøkspersonene ikke kunne opprettholde det selvvalgte tempoet i mer enn 10 s. Spyttprøver ble samlet tre ganger under eksperimentelle forsøk: før start av den første nevromuskulære vurderingen, etter den siste nevromuskulære vurderingen, og etter 5 minutter med restitusjon.

Figur 1. Eksperimentell design av studien.
2.3. Kardiorespiratoriske treningsresponser
Ventilasjon (VE) og lungegassutveksling (VO2, VCO2) ble målt pust for pust i hvile og under de to forsøkene gjennom et munnstykke og enveis ikke-repustventil (Hans Rudolph 2700, Shawnee, KS, USA), neseklemme, og ekspirasjonsporten koblet til en metabolsk vogn (TrueOne 2400, Parvomedics, Sandy, UT, USA) [42]. Samtidig ble sentrale hemodynamiske markører (HR: hjertefrekvens; SV: slagvolum; CO: hjertevolum) samlet ved hjelp av en ikke-invasiv thorax impedanskardiograf (PhysioFlow®, Paris, Frankrike). Validiteten og reliabiliteten til denne metoden er tidligere etablert [43].
2.4. Vurdering av nevromuskulær funksjon og tretthet
Følgende metoder ble utført på en måte som ligner på tidligere studier [44,45]. Følgelig, etter riktig hudforberedelse, ble to full-overflate fastklebende hydrogelstimulerende elektroder (størrelse: 50 90 mm, Myotrode Plus, Globus G0465) påført på quadriceps: anoden ble plassert på den proksimale delen av låret , mens katoden ble plassert på den distale delen av benforlengerne, 3 cm over patella. Stimuleringsintensiteten ble bestemt før målingene med 25-mA-økninger inntil størrelsen på den fremkalte rykningen og det sammensatte muskelaksjonspotensialet (M-bølge) ikke viste noen ytterligere økning. Den stimulerte rykkkraften ble målt av en tilstrekkelig kalibrert krafttransduser (MLP-300; Transducer Techniques, Temecula, CA, USA) statisk koblet til en spesiallaget stol gjennom en ikke-kompatibel stropp plassert rundt ankelen på selvet. -rapportert dominant lem (høyre ben i alle tilfeller). Forsøkspersonene ble sittende med en 90◦ knefleksjon under tretthetsvurderingene. Den overlagrede rykningen (SIT) og den hvilende rykningen (Qtw, pot) ble målt under en 5-s MVC av kneekstensorene og etter 2-s med avslappet muskel. Denne prosedyren ble gjentatt seks ganger før og etter tiden til utmattelsessykling. Dataene til de tre beste MVC-ene ble analysert og gjennomsnittet. Frivillig muskelaktivering (VMA prosent ) ble beregnet som VMA prosent=[1- (SIT/Qtw,pott)x100]. Toppkraft, maksimal kraftutviklingshastighet (MRFD) og maksimal relaksasjonshastighet (MRR) ble analysert for alle Qtw, pot. Toppkraft ble beregnet som den høyeste verdien nådd for hver Qtw, pott, MRFD og topp MRR for hvilerykningen ble beregnet som maksimal bratthet av skråningen over et 10-ms intervall. Data ble samlet inn ved hjelp av et Biopac-system (MP150) og registrert ved hjelp av AcqKnowledge AD-innsamlingssystemet (v. 4.4, Biopac, Goleta, CA, USA) på en separat datamaskin. Alle data i løpet av utmattelsestiden ble analysert hvert 30. sekund. For å forstå den potensielle effekten av CAP på oppfatninger av tretthet, vurderte vi hele kroppen og beinhastigheten for opplevd anstrengelse (henholdsvis RPEtot og RPEleg) hvert minutt under forsøkene.
2.5. Mikrovaskulær oksygenering
Mikrovaskulær oksygenering ble overvåket med et multi-distanse frekvens-oppløst nær-infrarødt spektroskopi-oksymeter (NIRS; Oxiplex TS; ISS, Champaign, IL, USA). NIRS-teknikken gir ikke-invasive og kontinuerlige målinger av oksygenert (HbO2), deoksygenert (HHb) og totalt (Hbtot) hemoglobinnivå, med en frekvens på 2 Hz. Sonden ble kalibrert hver gang før bruk og deretter plassert på vastus lateralis av det ikke-dominante (venstre) benet, og festet med teip og en bandasje for å unngå lyskontaminering, som i tidligere studier [46–48]. På grunn av identiske spektrale kvaliteter kan ikke hemoglobin og myoglobin identifiseres unikt ved bruk av NIRS, og representerer dermed et konglomeratsignal.
2.6. Spyttanalyse
Prøver av {{0}}mL hel spytt ble samlet som angitt ovenfor, via passiv sikleteknikk, og umiddelbart lagret ved -80 ◦C inntil analysen. Analyse av kortisol, IL-1, IL-6 og -amylase ble utført ved bruk av kommersielt tilgjengelig ELISA og enzymsett (Sali-metrics, Carlsbad, CA, USA). Analysene ble kjørt med prøver/standarder i duplikat, i samsvar med produsentens retningslinjer, og lest med et kolorimetrisk spektrofotometer (iMark, Biorad, Hercules, CA, USA). Lineariteten for disse analysene var R2 > 0,99, mens variasjonskoeffisienten (CV) var<5% on="" standards="" for="" all="">
2.7. Biokjemisk analyse av kapsler
Capsaicintilskudd (n {{0}}) og kontrollfibertilskudd (n=3) ble analysert ved ekstraksjon med etanol for å kvantifisere mengden av analyttene capsaicin og dihydrocapsaicin i hvert tilskudd, da begge virker på TRPV1 . Innholdet i hvert tilskudd ble kombinert i 1,5 ml etanol og fikk ekstrahere i åtte timer i en ovn ved 80 ◦C med periodisk risting. Prøvene ble filtrert og ekstraktet ble analysert ved HPLC (Thermo Vanquish, Waltham, MA, USA) med massespektrometrisk deteksjon (Thermo ISQ-EC, Waltham, MA, USA) for å kvantifisere innholdet av capsaicin og dihydrocapsaicin. Eksterne standarder var brukes til kalibrering med en typisk intra-analyse CV på 3 prosent og linearitet på R2 > 0,995.
2.8. Statistisk analyse
I et design med én hale, paret utvalg, en effektstørrelse på 0.8, og en alfa på 0.05, ble en prøvestørrelse på 12 deltakere estimert for å sikre en statistisk styrke på {{10}}.80 (G*Powersoftware, Kiel, Tyskland). Statistiske sammenligninger ble utført med kommersielt tilgjengelig programvare (Prism v. 8.0, GraphPad Software, San Diego, CA, USA). Data under TTE (kardiovaskulære, ventilatoriske, inflammatoriske og RPE-variabler) ble analysert ved å bruke en toveis variansanalyse med gjentatte mål (ANOVA) for å evaluere forskjellene mellom forsøk. Tester av normalitet og forutsetninger ble utført, hvis det ble funnet et betydelig brudd, ble det foretatt en passende justering av frihetsgradene. For TTE var det siste tidspunktet den subjektive tiden til oppgavesvikt. Sammenkoblede prøvers t-tester ble brukt for å vurdere forskjellene mellom tilstandene i pre-to-post TTE-endringene i nevromuskulære vurderinger. Statistisk signifikans ble erklært når p < 0,05.="" data="" er="" presentert="" som="" middel="" ±="" sd="" med="" mindre="" annet="" er="">
3. Resultater
3.1. Deltakeregenskaper
Ti unge, friske og fysisk aktive menn oppfylte alle inklusjonskriterier og fullførte alle forsøk (tabell 1). Kardiorespiratoriske parametere før trening var ikke forskjellige mellom forsøkene (alle p > 0.05, data ikke vist).

Tabell 1.Deltakeregenskaper.
3.2. Supplement Analyse
Prøvesporing av absorbansspektra for Capsaicin og dihydrocapsaicin brukt for etterfølgende kvantifisering er presentert i figur 2. Gjennomsnittlig kapsaicininnhold i hvert tilskudd var 0.957 mg/tablett med et område på 0.951–{ {5}}.969 mg/kapsel, dermed var totaldosen 1.914 mg. For dihydrokapsaicin var gjennomsnittet 0.329 mg/kapsel med et område på 0.326–0.332 mg/kapsel, og dermed var den totale dosen 0. 658 mg. Kontrollfibertilskuddene inneholdt ingen påvisbare nivåer av capsaicin eller dihydrocapsaicin.

Figur 2. Prøveabsorbanssignal
3.3. Treningsytelse, nevromuskulær funksjon og tretthet
Både placebo- og capsaicin-tilstander viste lignende utmattelsestider (TTE) på henholdsvis 375 ± 26 og 327 ± 36 s (p > 0.05, figur 3A). Når det gjelder kraften før trening, var ikke MVC-ene forskjellige mellom de to tilstandene (640 ± 127 vs. 643 ± 161 N, p > 0.05), samt etter TTE (479 ± 125 vs. 499 ± 133 N, p > 0.05). Følgelig viste baseline-hviletrekningene (Qtw, pot) lignende verdier (201 64 vs. 205 59 N, p > 0,05), men trendet mot en større Qtw, pot umiddelbart etter trening i CAP-tilstanden som sammenlignet med PL-tilstanden (100 ± 28 vs. 116 ± 37 N, p=0.07, figur 4F). Dette sees også i den prosentvise endringen i nedgang etter trening i Qtw, pot i de to tilstandene, som nådde statistisk signifikans (52 ± 6 vs. 42 ± 11 prosent, p=0.037, figur 4E). Når den potenserte rykningen (Qtw,pot percent ) ble plottet som en funksjon av TTE, var signifikant positiv korrelasjon med både PL (r=0.7, p=0.04) og CAP (r {{42 }}.7, p=0.04) ble observert (figur 3B). VMA prosent ble ikke påvirket av verken trening eller kosttilskudd (p > 0,05). Når vi ser på de iboende muskelkontraktile funksjonene, viste MRR og MRFD signifikante reduksjoner i pre-to-post TTE (p < 0.000).="" i="" tillegg="" dempet="" cap="" den="" treningsinduserte="" nedgangen="" i="" mrr="" (p="0.01;" figur="" 4c).="" spesifikt,="" i="" pl-tilstanden,="" ble="" mrr="" redusert="" med="" 57="" ±="" 22="" prosent,="" mens="" det="" bare="" ble="" dempet="" med="" 41="" ±="" 19="" prosent="" i="" cap.="" i="" motsetning="" sank="" mrfd="" på="" samme="" måte="" i="" begge="" tilstandene,="" nemlig="" med="" 55="" ±="" 16="" prosent="" og="" 49="" ±="" 21="" prosent="" i="" henholdsvis="" pl="" og="" cap="" (figur="">

Figur 3. Tid til utmattelse
3.4. Mikrovaskulær oksygenering under TTE
Etter inntak av CAP eller PL, nivåene av muskeloksygenering før trening (StO2 prosent ; 64 ± 3 vs. 68 ± 8 prosent ), totalt hemoglobininnhold (THC; 63 ± 23 vs. 66 ± 20 μM) , oksygenert hemoglobin (HbO; 40 ± 14 vs. 44 ± 11 μM), og oksygenert hemoglobin (Hb; 23 ± 10 vs. 22 ± 10 μM) var ikke forskjellige mellom tilstandene (p > 0,05). Starten av TTE modifiserte de mikrovaskulære muskeloksygeneringsindeksene, men endringene var ikke forskjellige med CAP-behandling. Imidlertid viste muskelsirkulasjonen en generell trend for høyere verdier med CAP, som reverserte under trening, med THC (77,5 ± 28,1 vs. 80,2 ± 30,9 μM) og Hb (36,2 ± 20,3 vs. 40,2 ± 19,4 μM) høyere i μM tilstand. Når vi ser på hyperemien under restitusjon, viste CAP høyere nivåer av StO2 prosent sammenlignet med PL (71,6 ± 1,6 vs. 69,5 ± 2,8 prosent , p=0.02), men det var ingen forskjeller mellom tilstandene for [THC] (90,1 ± 29,7 vs. 88,9 ± 31,8 μM), [HbO] (64,7 ± 22,0 vs. 62,3 ± 23,1 μM), og [Hb] (25,4 ± 7,9 vs. 26,37).

Figur 4. Nevromuskulære funksjonsparametre uttrykt som den anstrengelsesinduserte relative endringen etter tiden til utmattelse (TTE) hos unge aktive menn (n=10).
3.5. Sentral hemodynamikk, ventilasjon og opplevd anstrengelse under TTE
Indeksene til den sentrale hemodynamikken (HR, SV og CO) ble ikke påvirket ulikt av de to forholdene (figur 5). Ingen statistisk signifikante tilstand x tid interaksjoner (p > 0.05) ble observert for HR, SV og CO under både baseline og trening. Som forventet var det en hovedeffekt av tid for alle de sentrale hemodynamiske markørene (p < 0.00),="" men="" ikke="" en="" effekt="" av="" cap-="" eller="" pl-administrasjon.="" med="" cap="" var="" hr-toppen="" under="">
180 ± 7 bpm, SV var 212 ± 48 mL/min, og CO var 36 ± 8 L/min. I samsvar med PL var toppen av HR 181 ± 9 bpm, SV var 225 ± 49 ml/min, og CO var 38 ± 9 l/min. En signifikant tidseffekt ble funnet for ventilasjonsresponsene på øvelsen (p < {{30}}.05)="" i="" vo2,="" ve="" og="" rer="" (data="" ikke="" vist),="" mens="" ingen="" interaksjons-="" eller="" tilstandseffekt="" ble="" vist="" .="" videre="" økte="" vurderingen="" av="" opplevd="" anstrengelse="" (figur="" 5d)="" av="" både="" hele="" kroppen="" og="" benet="" i="" henhold="" til="" fremdriften="" av="" treningen="" og="" uavhengig="" av="" behandlingen="" (rpetot:="" 7,8="" ±="" 2,2="" vs.="" 6,9="" ±="" 2,8;="" rpeleg:="" 9,3="" ±="" 1,3="" vs.="" 9,0="" ±="" 1,1;="" alle="" p=""> 0,05).
3.6. Stress og proinflammatoriske biomarkører
CAP påvirket ikke spyttkortisolsekresjonen ved baseline, under og etter trening. Faktisk var det en hovedeffekt av tid (p {{0}}.002) med en økning i spyttkortisolkonsentrasjon under restitusjon; CAP påvirket imidlertid ikke den generelle kinetikken (p > 0,05, tabell 2). Aktiviteten til spytt-amylasen hadde en tendens til å bli redusert med CAP (p=0.07), og viste under begge tilstander en hovedeffekt av tid (p < 0.001,="" tabell="" 2).="" når="" vi="" ser="" på="" interleukinene,="" økte="" cap="" den="" gjennomsnittlige="" spytt-il-6-konsentrasjonen="" (p="0.009)" ved="" baseline="" og="" under="" treningen,="" og="" deretter="" sank="" nivået="" til="" pl-konsentrasjoner="" etter="" trening.="" dessuten="" hadde="" cap="" en="" tendens="" til="" å="" dempe="" økningen="" i="" il-1="" etter="" trening="" (p="0.053," tabell="">
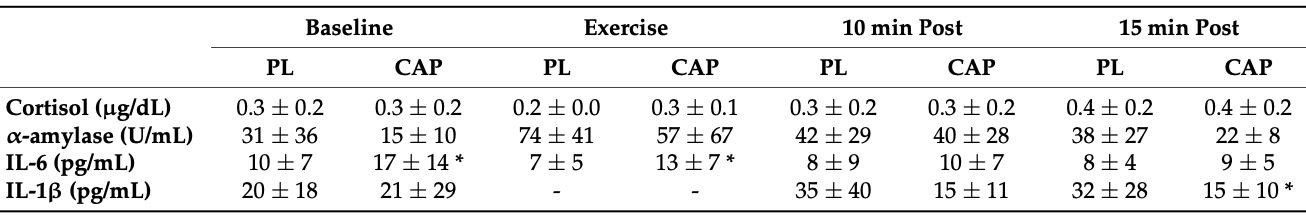
Tabell 2.Endokrine og inflammatoriske biomarkører.

cistanche pdf-filer
4. Diskusjon
Denne studien søkte å bestemme den potensielle innvirkningen av akutt oral capsaicin (CAP) administrering på utholdenhetsytelse til sykling til utmattelse og analysere de tilknyttede fysiologiske mekanismene som ligger til grunn for nevromuskulær tretthet. Til tross for at det ikke var noen forskjeller mellom CAP og PL når det gjaldt sykkelprestasjon fra tid til utmattelse, dempet CAP nedgangen etter trening i den potensierte rykningen. Det påvirket delvis den kontraktile kinetikken til muskelen, og ga en større avspenningshastighet, men ingen forskjell i sammentrekningshastigheten. CAP hadde ingen effekter på kardiorespiratorisk, oppfatning av tretthet eller mikrovaskulære responser på TTE-studien. Dette antyder en potensiell forbedring av det sarkoendoplasmatiske retikulum Ca2 pluss ATPase (SERCA) pumpeaktivitet, og dermed bevare muskelavslapping. Dessuten modulerte CAP endringer i de pro-inflammatoriske interleukinene, og dempet økningen av IL-1 under restitusjon. Delvis i samsvar med vår hypotese, forbedret ikke CAP tiden til utmattelse, men det så ut til å dempe perifer nevromuskulær tretthet, øke muskelavslapningshastigheten og forbigående endre den inflammatoriske responsen, uavhengig av endringer i kardiorespiratoriske eller mikrovaskulære responser.
4.1. CAP og treningsytelse
Til dags dato har bare noen få forskere undersøkt rollen til capsaicin under trening hos mennesker [28–32]. Så vidt vi vet, er dette den første studien som undersøker hvordan CAP påvirker nevromuskulær tretthet hos mennesker i fysiologiske termer og ikke bare med perseptuelle indekser. Faktisk ser det ut til at akutt CAP-inntak øker ytelsen eller tretthetsmotstanden under en løpende tidsprøve [30], høyintensiv intermitterende trening [29] og motstandstrening [28]. I denne studien observerte vi imidlertid ingen ytelsesforbedring (figur 3), noe som stemmer overens med funnene til Opheim og kolleger [32]. Tidligere arbeid med gnagere antyder at CAP øker ytelsen på en doseavhengig måte [21–24], og det er derfor mulig at dosen som ble brukt i denne studien ikke var nok til å fremkalle en ytelsesforbedring; Vi kan imidlertid være de første som faktisk bekrefter capsaicin/dihydrocapsaicin-innholdet i kosttilskuddet, og viktigere, vi unngikk enhver potensiell betydelig gastrointestinal lidelse som kan ha svekket treningsytelsen.
4.2. CAP og treningsindusert nevromuskulær tretthet
I den nåværende studien, etter sykkeltreningsforsøket, ble indeksene for bevegelsesmuskeltretthet alle negativt påvirket, som forventet. Faktisk reduserte både kraften og den frivillige muskelaktiveringen i tilsvarende grad uavhengig av CAP-tilskudd (Figur 4). Interessant nok ble de treningsinduserte reduksjonene i indekser for perifer tretthet tilsynelatende svekket med CAP, hovedsakelig blant dem, den maksimale avspenningshastigheten og omfanget av den potensierte rykningen. Mekanistisk kan en årsak til disse forskjellene tilskrives endret Ca2 pluss-håndtering. Det er allerede dokumentert at under intens trening, reduseres Ca2 pluss frigjøring fra det sarkoplasmatiske retikulum (SR) som svar på en markert uttømming av cellulær ATP [49,50], som kan virke for å redusere kraftutgangen til treningen og forhindre perifer tretthet fra å krysse en kritisk terskel [51]. Denne studien undersøkte capsaicin, som øker TRPV1-kanalaktiviteten som kan påvirke Sarco/Endoplasmic Reticulum Calcium ATPase (SERCA)-pumpen [52] i muskelen. Forhøyet SERCA-pumpeaktivitet med CAP-indusert aktivering av TRPV1 i muskel forbedret følgelig kinetikken til SR Ca2 pluss gjenopptak [49,50,53], noe som kanskje forklarer den bedre bevarte maksimale avspenningshastigheten etter trening. Dessuten kan capsaicin fremme mitokondriell depolarisering og produksjon av reaktive oksygenarter (ROS), i det minste ved høye doser [52], men på den annen side er det også påstått å ha bemerkelsesverdig antioksidantaktivitet [54], spesielt i lavere doser. Reaktive oksygenarter øker betydelig under intens muskelaktivitet [51] og er kjent for å bidra til tretthet, men forholdet mellom redoksbalanse og ytelse er komplekst [55]. Det er holdbart at CAP, i en antioksidantkapasitet, kan motvirke de utmattende effektene av forhøyet ROS, kanskje bedre opprettholde nevromuskulær funksjon etter trening, men det er nødvendig med ytterligere undersøkelser.
Disse resultatene fremhever en potensiell rolle til CAP i å dempe utviklingen av perifer tretthet, kanskje via modulering av Ca2 pluss-håndtering og antioksidanteffekten. Disse funnene støttes også av studier som undersøker andre antioksidanter som askorbaterende trening hos friske mennesker [55,56] og i sykdom [57,58]. Dessuten, hvis vi integrerer mikrosirkulasjonsresultatene, selv om vi ser en tendens til høyere StO2-prosent og HbO under anstrengende trening, kan den betydelige økningen i O2-levering under utvinning i CAP forbedre perifer vaskulær funksjon [59]. Årsaken til at ingen signifikante forskjeller under trening kan være at CAP kan påvirke muskelvaskulaturen i høyere doser enn de vi har gitt. I denne studien hadde vi imidlertid som mål å minimere de potensielle bivirkningene av capsaicin-inntak, nemlig gastrointestinale plager. Vi oppdaget ingen forskjeller i indeksene for sentral tretthet, selv om tidligere studier på rotter fant at CAP aktiverer undergrupper av de metabosensitive muskelreseptorene i gruppe IV [60], hvis stimulering refleksivt øker sentraldriften [61]. Perseptuelt ble det tidligere funnet at akutt CAP-tilskudd kunne redusere vurderingen av opplevd anstrengelse under utholdenhet [28], selv om dette ikke var tilfelle i vår studie, da RPE økte like mye i løpet av tiden til utmattelse i både CAP- og PL-forhold.
4.3. CAP og den fysiologiske responsen på trening
Ettersom capsaicin har blitt foreslått å forbedre treningsytelsen og utmattelsesmotstanden, er det viktig å forstå hvordan det kan endre den fysiologiske responsen på trening og til slutt støtte større arbeid. For dette formål antyder tidligere arbeid i dyremodeller at CAP-induserte forbedringer i ytelse var assosiert med økt hepatisk glykogeninnhold [21], kanskje på grunn av glykogensparing [24], og økt fettsyreutnyttelse som et resultat av katekolaminsekresjon og/eller aktivitet [22]. Dessuten ble det funnet at en enkelt høy dose CAP nedregulerte uttrykket av det mitokondriavkoblingsproteinet UCP3, noe som reduserte energikostnaden for en gitt elektrisk indusert sammentrekning [25,27]. Hos mennesker er det imidlertid ikke funnet noen endring i muskelfettoksidasjon med akutt CAP-tilskudd under treningsrestitusjon [62]. I denne studien var de metabolske responsene like gjennom hele øvelsen, noe som tyder på at akutt tilskudd hos mennesker ikke påvirker energiforbruket, målt via VO2 (Figur 5), eller valg av energisubstrat under trening, som vurdert av RER, i det minste ved dette relativt sett. høy treningsintensitet paradigme. Følgelig var de sentrale hemodynamiske og ventilasjonsresponsene også like mellom forsøkene, i tråd med en lignende metabolsk kostnad. I tillegg skilte mikrosirkulasjonen av lemmuskelen seg heller ikke signifikant under trening, noe som tyder på at CAP, i det minste i denne dosen, utøver en minimal vasodilatorisk effekt på musklene. Faktisk, under den første hvilen, viste muskelsirkulasjonen en generell trend for høyere indekser for mikrovaskulær perfusjon med CAP, som reverserte under trening med THC og Hb høyere med PL. Samlet virker oksygentilførsel og bruk upåvirket av CAP-tilskudd og ser ikke ut til å være sannsynlige kandidater for forbedret nevromuskulær tretthet.
4.4. CAP og nevroinflammatoriske indekser
Under normale forhold er kortisolkonsentrasjonen etter akutt trening intensitetsavhengig [63] og øker til toppkonsentrasjoner 20–30 minutter etter avsluttet fysisk aktivitet [64]. Resultatene våre bekrefter den økende kortisoltrenden etter slutten av TTE, men CAP hadde ingen effekt på det. Faktisk har det blitt sett at gjentatt CAP-administrasjon hos rotter øker og forlenger stressresponsen [65], kanskje til nivåer som kan sammenlignes med anstrengende trening, selv om dette vanligvis sees med store doser. Når vi ser på andre biomarkører for spyttstress, hadde CAP en tendens til å senke spytt-amylase-enzymaktiviteten, kanskje et tegn på lavere sympatisk aktivitet [66], kanskje via endret TRPV1-afferentaktivitet. Selv om in vitro-studier har vist lignende resultater, finner vi at capsaicin-avledede forbindelser er potensielle amylasehemmere [67], og forsterker dermed funnene våre. Et annet viktig aspekt er de antiinflammatoriske egenskapene til CAP. I resultatene våre reduserer CAPattenuerer økningen i IL-1 etter trening, noe som kanskje gjør den proinflammatoriske cytokinproduksjonen sløv [39]. På den annen side fant vi en økt spyttkonsentrasjon av IL-6etter trening som ikke var påvirket av CAP [68,69], som sannsynligvis kan være et resultat av den anstrengende ytelsen [32,70], eller capsaicin- indusert TRPV1-aktivering i fett [71], eller andre steder. IL-6 kan i dette tilfellet ha metabolske konsekvenser [11,72] snarere enn inflammatorisk gitt divergensen mellom IL-6 og IL-1. Imidlertid er det nødvendig med ytterligere arbeid hos mennesker for å dechiffrere den potensielle effekten av oral capsaicin på betennelse hos mennesker og de potensielle konsekvensene på fysiologi og/eller tretthet. Videre bør fremtidig forskning se på større og/eller mer kroniske doser av capsaicin og hvordan de interagerer med laktatnivåer under trening.
4.5. Studiens begrensninger
Denne studien ble ikke utført uten begrensninger. Først ble bare unge aktive menn rekruttert fra et høyskolesamfunn inkludert, og derfor er fremtidig arbeid i eldre og/eller kvinnelige populasjoner nødvendig. For det andre kan bruk av elektrisk stimulering på muskelmagen og ikke femoralnerven føre til lavere nevromuskulære responser. Til slutt kan mer invasive mål på metabolisme, inkludert laktat og muskelnivå VO2, være interessant å undersøke under og etter treningen med CAP i fremtidige studier.
Cistanche-urter har en anti-tretthetseffekt.
For mer informasjon, vennligst klikk her.
5. Konklusjoner
Så vidt vi vet, er dette den første studien som undersøker effekten av capsaicin på treningsytelse, nevromuskulær tretthet og spyttindikatorer for stress og proinflammatoriske biomarkører hos mennesker. I motsetning til tidligere funn hos mennesker, forbedret ikke akutt capsaicin-administrasjon treningsytelsen eller vurderingen av opplevd anstrengelse. Den viste imidlertid kapasiteten til å dempe utviklingen av perifer tretthet, som ikke ser ut til å være et resultat av endringer i sentral hemodynamikk, muskeloksygentilførsel eller størrelsen på den sentrale motordriften etter sykkeløvelsen. Dessuten modulerte CAP spyttbiomarkørene, noe som tyder på en potensiell deprimert sympatisk aktivitet og antiinflammatorisk effekt under toppkonsentrasjonen med en sen reduksjon i proinflammatoriske markører. Samlet har capsaicin potensialet til å endre de perifere komponentene av nevromuskulær tretthet, noe som fører til mulige forbedringer av trening.







