Omfattende analyse av pyroptoseregulatorer og tumorimmunmikromiljø i klarcellet nyrecellekarsinom
May 23, 2022
For mer info. ta kontakt medtina.xiang@wecistanche.com
Abstrakt
Bakgrunn: Økende bevis har indikert at pyroptose kan reguleresvulst immun mikromiljø(TIME) for å påvirke tumorutvikling. Som en svært immunogen svulst kan klarcellet nyrecellekarsinom (ccRCC) dra nytte av immunterapi, men relatert forskning på pyroptose i TIDEN av ccRCC er fortsatt mangelfull.
Metoder: Tilgjengelige data hentet fra TCGA- og GEO-databaser ble analysert for å identifisere de forskjellige ekspresjonsprofilene for pyroptose i ccRCC og normalt vev, og korrelasjonen mellom pyroptoseregulatorer og TIME ble evaluert i cCRCC.
Resultater: I henhold til konsensusklyngeanalyse ble to differensielle ekspresjonsnivåer av subtyper identifisert for å påvirke pasientprognosen, og var relatert til histologisk tumorstadium og -grad. Immunceller ble beregnet ved hjelp av CIBERSORT-algoritmen. Høyere infiltrerte nivåer av B-celler naive, T-celler CD4-minne hviler, NK-celler hvilende, monocytter og makrofager ble observert i klynge 1, mens høyere infiltrerte nivåer av CD8 pluss T-celler, T-follikulære hjelpeceller og tregs ble observert i klynge 2 Anrikningsanalyse av gensett indikerte at klynge 2 ble beriket i flere immunrelaterte veier, inkludert JAK-STAT-signalveien. Videre var overekspresjon av åtte immunkontrollpunkter relatert til utvikling av ccRCC, spesielt i klynge 2. Ettersom fire potensielt nøkkelregulatorer for pyroptose ble AIM2, CASP5, NOD2 og GZMB bekreftet å være oppregulert i ccRCC ved RT-qPCR-analyse og ytterligere verifisert av HPA database. Ytterligere pan-kreftanalyse antydet at disse fire pyroptoseregulatorene ble differensielt uttrykt og relatert til TIME i flere kreftformer.
Konklusjon: Denne studien ga et omfattende syn på pyroptoseregulatorer i CCRCC-tiden, som kan gi potensiell verdi for immunterapi.
Nøkkelord: Klarcellet nyrecellekarsinom, Pyroptose, Tumorimmunmikromiljø, Immunkontrollpunkter, Immunterapi

Klikk for å lære herba cistanches behandle nyrefunksjon
Bakgrunn
Nyrecellekarsinom(RCC) er den vanligste ondartede solide svulsten i nyrene hos voksne, og står for omtrent 3 prosent av alle voksne maligniteter og 90 prosent av nyrekrefter[1]. For tiden har antallet dødsfall på grunn av RCC hvert år over hele verden oversteget 1,00,000, og sykelighets- og dødelighetsraten øker med en hastighet på 2-3 prosent hvert 10. år [2]. I følge 2004-versjonen av WHOs RCC patologiske klassifisering er forekomsten av klarcellet nyrecellekarsinom (ccRCC) omtrent 70 prosent [3]. Selv om kirurgisk reseksjon fortsatt er den beste behandlingen for ccRCC, finnes det foreløpig ingen effektiv postoperativ adjuvant behandling, og ccRCC er ikke følsom for strålebehandling og kjemoterapi. I følge litteraturen opplever 20-40 prosent av pasientene tilbakefall etter operasjonen [4]. Som en svært immunogen svulst kan ccRCC dra nytte av immunterapi.
Pyroptose er en type programmert celledød ledsaget avbetennelseutløst av patogen mikroorganismeinfeksjon eller andre skadelige signaler [5]. Pyroptose er hovedsakelig preget av cellehevelse, lysis og frigjøring av cytoplasmatisk innhold. Passende pyroptose er en viktig mekanisme for at verten skal motstå infeksjon av fremmede patogene mikroorganismer. Imidlertid er overdreven pyroptose skadelig eller til og med dødelig for verten. Et økende antall studier har vist at pyroptose også spiller en viktig rolle i utviklingen av svulster [6]. Pyroptose skaper et tumorhemmende miljø ved å frigjøre inflammatoriske faktorer. Imidlertid kan pyroptose også svekke kroppens immunfunksjon mot tumorceller og akselerere veksten av svulster i forskjellige kreftformer. Noen studier har vist at den effektive proinflammatoriske effekten av pyroptose er relatert til reguleringen av svulstens immunmikromiljø [7]. Disse funnene tyder på at pyroptose spiller en viktig rolle i tumorutvikling og antitumorprosessen. Imidlertid er effekten av pyroptose på prognosen for ccRCC uklar. En omfattende forståelse av pyroptose i ccRCC mangler fortsatt, inkludert krysstale mellom pyroptoseregulatorer og tumorimmunmikromiljøet.
I denne studien utførte vi en omfattende retrospektiv analyse basert på The Cancer Genome Atlas (TCGA) database og Gene Expression Omnibus Database (GEO) for å estimere påvirkningen av pyroptose på TIME og undersøkte videre de underliggende mekanismene mellom pyroptosis og individuell TIME karakteriseringer basert på konsensusklyngeanalysen. I tillegg bekreftet denne studien også forholdet mellom pyroptose og immunt hot checkpoint-uttrykk.
Materialer og metoder
Datainnsamling og identifikasjon av differensialuttrykk
RNA-sekvenseringsdata (RNA-seq) for 539 ccRCC-vev og 72 normalenyrevev så vel som de tilsvarende kliniske egenskapene fra TCGA-databasen (https://portal.gdc.cancer.gov/) ble innhentet. GSE46699- og GSE53757-dataene fra GEO-databasen (https://www.ncbi.nlm.nih.gov/geo/) ble samlet inn og brukt til å evaluere pyroptoseregulatoruttrykk. Videre ble TCGA pan-cancer genekspresjonsdata for 33 typer ondartede svulster og tilsvarende klinisk informasjon, for eksempel stamness-score basert på mRNA (RNAss) og DNA-metylering (DNAss) samt immunsubtyper, hentet fra universitetet California Santa Cruz database (UCSC Xena, http://xena.ucsc.edu/). De 37 pyroptoseregulatorene er presentert i tilleggsfil 4: Tabell S1 og ble hentet fra tidligere undersøkelser [8, 9]. Ved å bruke "limma"-pakken, mer enn to ganger endringer og en falsk oppdagelsesrate (FDR, justert p-verdi)<0.05 is="" considered="" differential="" gene="" expression.="" the="" immunohistochemistry="" (ihc)="" staining="" images="" of="" pyroptosis="" regulators="" in="" normal="" kidney="" and="" tumor="" tissues="" were="" analyzed="" and="" obtained="" from="" the="" hpa="" database="" (http://www.proteinatlas.org/).to="" compare="" the="" expression="" between="" normal="" and="" tumor="" samples,="" all="" tissues="" were="" selected="" using="" the="" same="">
Konsensus klynging
Univariate Cox regresjonsanalyse ble brukt til å trekke ut pyroptoseregulatorer via R-pakkens "overlevelse" p-verdi<0.05). consensus="" clustering="" was="" performed="" to="" explore="" the="" potential="" molecular="" subtype="" between="" the="" bca="" patients="" using="" the="" r="" package"consensus="" cluster="" plus".="" the="" cluster="" count="" (k)="" was="" set="" from="" 1="" to="" 9,="" and="" the="" best="" optimal="" k="" value="" was="" selected="" for="" further="">
Estimering av tumorimmunmikromiljø
CIBERSORT, et analyseverktøy basert på LM22-immungensignaturen, ble brukt til å evaluere tumorimmuninfiltrasjonsnivåene til ccRCC. Algoritmen ble kjørt for 1000 permutasjoner og ccRCC-prøver med en utgang P<0.05 were="" selected="" for="" further="" analysis.="" the="" "estimate"="" package="" in="" r="" was="" used="" to="" evaluate="" the="" immune="" score="" and="" the="" stromal="" score.="" moreover,="" 8="" com-mon="" immune="" checkpoint="" genes,="" including="" pd-1,="" pd-l1,="" pd-l2,="" ctla4,="" siglec15,="" tigit,="" tim3,="" and="" lad3,="" were="" extracted="" and="" evaluated="" for="" their="" correlations="" with="" pyroptosis="" regulators="" in="">
Funksjonell berikelsesanalyse
Gene Ontology(GO)-analyse og Kyoto Encyclopedia of Genes and Genomes (KEGG) signalveianalyse ble utført ved bruk av "cluster Profiler"-pakken i R. I tillegg ble Gene Set Enrichment Analysis (GSEA) utført for å identifisere forskjellene i settet med gener uttrykt mellom de to klyngene i berikelsen av KEGG-banen. Antall permutasjoner ble utført 1000 ganger for
hver analyse, og banene med justert p-verdi<0.05 and="" q="" values=""><0.05 were="" considered="" statistically="">
Prediksjon av medikamentrespons
Basert på informasjonen hentet fra databasen Genomics of Drug Sensitivity in Cancer (GDSC) (https://www.cancerrxgene.org/), ble de kjemoterapeutiske sensitivitetene for ccRCC beregnet. Tre vanlige kliniske legemidler ble valgt for å forutsi den kjemoterapeutiske responsen, og R-pakken "pRRophetic" ble brukt til å estimere den kjemoterapeutiske responsen bestemt av den halvmaksimale hemmende konsentrasjonen (IC50).
Cellelinjer og RT-qPCR-analyse
De humane ccRCC-cellelinjene,786-O og Caki-1, ble levert av Haixiang Shen, og den normale humane epitelcellelinjen i nyrebarken, HK-2, ble levert av Yanhong Ma.RPMI 1640 medium (Gibco) supplert med 10 prosent føtalt bovint serum (FBS, Gibco) ble brukt til å dyrke cellene. Og alle cellene ble dyrket ved 37 grader med 5 prosent karbondioksid. Totalt RNA ble ekstrahert fra cellene med Trizol Kit (Invitrogen, Carlsbad, CA, USA) i henhold til produsentens instruksjoner. Den første strengen (cDNA) ble revers-transkribert og brukt som mal for qPCR-analyse som tidligere beskrevet [10]. Ekspresjonsnivåene til pyroptoseregulatorer (AIM2, NOD2, GZMB og CASP5) ble målt ved å bruke et SYBR Green qPCR Kit (Takara, Japan). Gennavnet og primersekvensene er oppført i tilleggsfil 5: Tabell S2. mRNA-nivåene til alle gener ble normalisert til GAPDH (en endogen normaliseringsreferanse).
Statistisk analyse
Statistisk analyse ble utført ved bruk av R-programvare (http://www.R-project.org,versjon 4.0.3), programmeringsspråket PERL (versjon 5.32.1.1, https://www.perl.org /), og GraphPad Prism 8.0. Korrelasjonskoeffisienter ble beregnet av Spearmen og avstandskorrelasjonsanalyser. Kaplan-Meier-kurver ble plottet, og en log-rank test ble brukt for å beregne den signifikante overlevelsesforskjellen. Wilcoxon signed-rank test ble brukt til å analysere kontinuerlige variabler, mens chi-square testen ble brukt til å analysere de kategoriske dataene. RT-qPCR-resultatene ble uttrykt som gjennomsnitt ± SEM. Forskjellene mellom gruppene ble evaluert ved enveis ANOVA etterfulgt av ad hoc Dunnetts multiple sammenligningstest for å sammenligne med normale nyreceller. En p-verdi mindre enn 0.05 ble ansett som statistisk signifikant for alle analyser.

Resultater
Identifikasjon og klassifisering av differensielt pyroptose-assosierte regulatorer
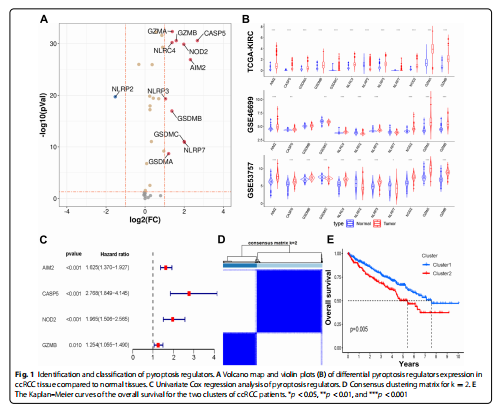
Ekspresjonen av 37 pyroptose-assosierte gener ble sammenlignet i TCGA-KIRC-kohorten, og 11 gener ble identifisert som differensielt uttrykte gener (fig. 1A). Etter at to uavhengige datasett fra GEO-databasen ble brukt til eksternt å illustrere uttrykket av disse 11 genene i ccRCC, viste seks pyroptose-assosierte regulatorer (AIM2, CASP5, NLRP3, NOD2, GZMA og GZMB) å være sterkt uttrykt i ccRCC (fig. .1B). Kombinert med pasientprognostisk informasjon lastet ned fra TCGA-datasett, ble univariat Cox-regresjon implementert for å screene gener fra disse 6 regulatorene, og fire av dem (AIM2, CASP5, NOD2 og GZMB) var signifikant relatert til ccRCC-pasientprognose (fig. 1C). . For ytterligere å undersøke forholdet mellom uttrykket av disse 4 regulatorene og ccRCC-subtypene, ble konsensusklyngeanalyse utført med TCGA-KIRC-kohortpasienter. Konsensusklyngeanalysen ble utført med ccRCC-pasienter basert på disse fire pyroptoseregulatorene, og resultatet viste at klyngevariabelen (k) =2 ble identifisert som den høyeste klyngestabiliteten fra k =1 til 9, noe som indikerer at ccRCC-pasienter kunne deles inn i to klynger med de høyeste intragruppekorrelasjonene og de laveste intergruppekorrelasjonene (fig. 1D). Dessuten hadde pasienter i klynge 1 gunstig total overlevelse (OS) sammenlignet med de i klynge 2(fig.1E).
TID-analyse av klyngene i henhold til pyroptoseregulatorene
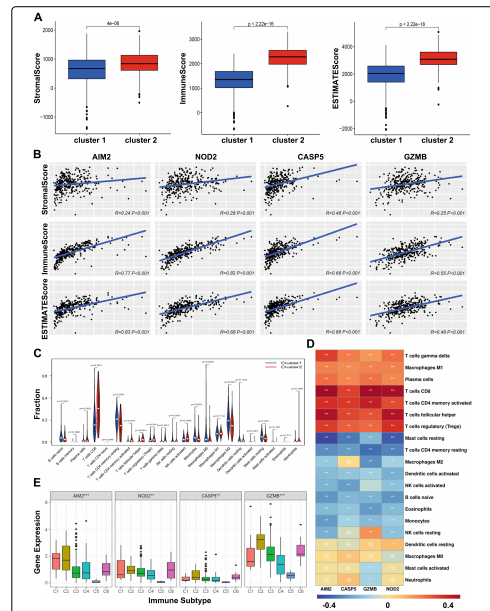
For å undersøke hvilke veier som er beriket i klyngene, ble GSEA-analyse utført for å identifisere de signifikante KEGG-veiene assosiert med de to klyngene. Resultatene viste at cytokinreseptorinteraksjon, T-cellereseptorsignalvei, antigenbehandling og presentasjon, kjemokinsignalvei, naturlig drepende cellemediert cytotoksisitet, tolllignende reseptorsignalvei, B-cellereseptorsignalvei og JAK-STAT-signalering vei var signifikant relatert til klynge 2 (tilleggsfil 1: figur S1), noe som indikerer at klyngene som inneholdt pyroptoseregulatorer var assosiert med tumorimmunmikromiljø. Derfor, for å utforske forskjellen i immunfunksjon mellom de to klyngene, ble ESTIMATE-skåre beregnet og demonstrert at klynge 2 hadde signifikant høyere ESTIMATE-, stromal- og immunskårer sammenlignet med klynge 1 (fig. 2A), og de fire pyroptoseregulatorene var positive relatert til disse skårene (fig. 2B). Videre avslørte de to klyngene signifikante forskjeller i immuncelleinfiltrering (fig. 2C). Klynge 1 hadde høyere infiltrerte nivåer av B-celler naive, T-celler CD4-minne hviler, NK-celler hviler, monocytter, makrofager M0, makrofager M2, aktiverte dendrittiske celler og mastceller i hvile, mens klynge 2 var høyere relatert til plasmaceller, T-celler CD8, T-cellers minne aktivert, T-celler follikulær hjelper, T-celler regulatoriske (Tregs), T-celler gamma delta og NK-celler aktivert. Analyse av korrelasjonen mellom de fire regulatorene og immuncelletypene viste at de fire regulatorene hadde en positiv eller negativ korrelasjon med de fleste immuncelletyper (Fig.2D). Interessant nok avslørte ytterligere undersøkelser av det differensielle uttrykket av immungener mellom to klynger at en masse immungener ble oppregulert i klynge 2 mens bare 5 gener ble nedregulert (tilleggsfil 2: figur S2A). De 10 mest oppregulerte og nedregulerte genene ble valgt for å analysere korrelasjonen, og resultatet vises i tilleggsfilen 2: Figur S2B. GO-analyse av biologiske prosesser viste at det differensielle uttrykket av immungener mellom klynger ble beriket i aktivering av celleoverflatereseptorsignalvei og signaloverføring avimmun respons. Cellulær komponentanalyse indikerte at de differensielt uttrykte immungenene var rikelig i immunglobulinkomplekset. Molekylær funksjonsanalyse indikerte at de differensielt uttrykte immungenene involverte antigenbinding. KEGG-analyse viste at de differensielt uttrykte immungenene ble beriket i cytokin-cytokinreseptorinteraksjoner (Tilleggsfil 2: Figur S2C, D). Disse resultatene indikerte at klynge 2 og de fire regulatorene er involvert i tumorimmunmikromiljøet.
Assosiasjon av pyroptoseregulatorer med immunkontrollpunkthemmere og de målrettede legemiddelsensitivitetene Immunkontrollpunkthemmere (ICI) terapier har blitt etablert som et potent behandlingsalternativ for flere tumortyper, mens bare en brøkdel av pasientene har nytte av slik terapi. Derfor ble det differensielle uttrykket av ICI-er i forskjellige undertyper undersøkt videre. Åtte varme immunsjekkpunktgener (SIGLEC15, TIGIT, PD-L1, TIM3, PD-1, CTLA4, LAG3 og PD-L2) var positivt relatert til klynge 2 (fig.3A, B). Interessant nok var fire regulatorer nært knyttet til de fleste ICI-er, mens det ikke var noen signifikant sammenheng mellom GZMB og SIGLEC15(fig.3C). I tillegg, tatt i betraktning den kliniske behandlingsverdien i målmedisinens sensitivitet, viste Sunitinib og Temsirolimus mer sensitivitet i klynge 1, mens Axitinib var nært knyttet til klynge 2 (fig. 3D-F). Disse resultatene indikerte at denne klassifiseringen kan gi en viss referanseverdi for den kliniske medisinen til forskjellige ccRCC-pasienter.

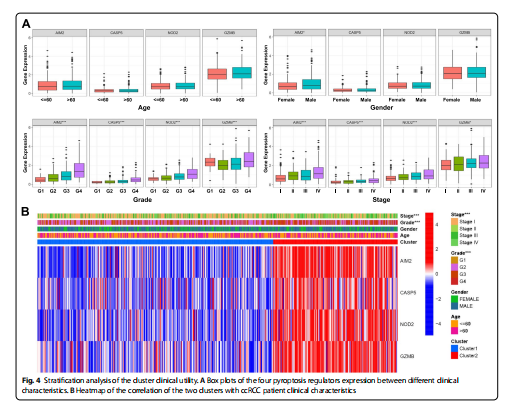
Stratifiseringsanalyse av klyngens kliniske nytte For ytterligere å utforske den kliniske verdien av forholdet mellom denne klassifiseringen og ulike kliniske egenskaper, ble ccRCC-pasienter delt inn i forskjellige grupper i henhold til pasientens alder, kjønn, grad og sykdomsstadium. Det er verdt å merke seg at det høyere sykdomsstadiet var mer assosiert med pasientene i klynge 2, så vel som den patologiske karakteren (tabell 1; fig.4B). Ytterligere analyse av forholdet mellom pyroptoseregulatorer og kliniske trekk viste at ekspresjonsnivået til de fire regulatorene ble økt med økningen av sykdomsstadiet og patologisk grad, mens bare AIM2 ble mer uttrykt hos menn enn hos kvinner. Det var ingen signifikant forskjell mellom uttrykket til de fire regulatorene og pasientens alder (fig.4A).

Eksperimentell verifisering av de fire regulatorenes uttrykk Basert på den bioinformatiske analysen av uttrykket til disse fire regulatorene, analyserte vi mRNA- og proteinekspresjonsnivåene. Sammenlignet med normale celler ble ekspresjonsnivåene til disse 4 genene oppregulert i ulik grad i de to ccRCC-cellelinjene (fig. 5A). Tilsvarende avslørte proteinekspresjonsmønstrene til AIM2, NOD2 og GZMB fra HPA-databasen at regulatorene også ble overuttrykt i ccRCC-vev sammenlignet med normalt vev (fig. 5B).

Fire pyroptoseregulatoruttrykksmønstre i flere kreftformer
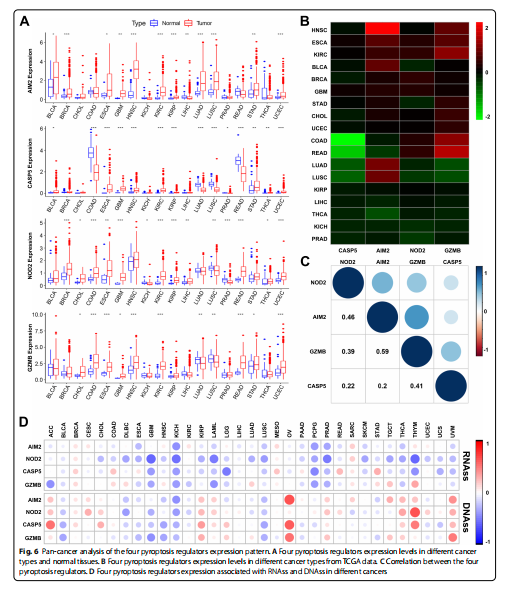
Ytterligere undersøkelse av uttrykksmønsteret til disse fire pyroptoseregulatorene i pan-cancer viste at fire pyroptoseregulatorer ble differensielt uttrykt i flere kreftformer (fig.6A). AIM2 ble differensielt uttrykt i flere kreftformer, inkludert blære, bryst, spiserør, nyre, lever , lunge, mage og endometrium, så vel som CASP5, NOD2 og GZMB (fig. 6A). Videre analyse fant at AIM2 var det mest positivt relatert til HNSC, mens CASP5 var negativt relatert til COAD(fig.6B). Og AIM2 og GZMB var de to genene med den mest signifikante positive assosiasjonen (korrelasjonskoeffisient =0.59, fig.6C).
Under kreftprogresjon kan tumorceller gradvis miste en differensiert fenotype og få stamceller og stamcelle-lignende egenskaper [11]. Generelt kan RNA-ene og DNA-ene brukes til å vurdere stammen til kreftstamceller [12]. Derfor ble korrelasjonen mellom pyroptoseregulatorer med tumorstamme målt ved RNAss og DNAss undersøkt. De fire regulatorene var signifikant positivt eller negativt korrelert med RNAs og DNAs i de fleste pan-cancers (fig. 6D). Spesielt i KIRC var AIM2 og GZMB positivt eller negativt assosiert med henholdsvis RNA, mens NOD2 var negativt assosiert med DNAss (tilleggsfil 3: figur S3).
Forening av de fire pyroptoseregulatorene med tumorimmunmikromiljø i pan-kreft
Basert på den viktige regulatoriske effekten av pyroptose-gener på ulike immuncelletyper, ble de fire regulatorene undersøkt videre i pan-cancer-mikromiljøet. Interessant nok, bortsett fra at AIM2 var negativt assosiert med DLBC og CASP5 var negativt assosiert med COAD og READ i ESTIMATE score og stromal score, andre var positivt assosiert med kreft i immunscore, stromal score og ESTI-MATE score (fig.7A) ). For å utforske de fire pyroptoseregulatorenes uttrykk i forskjellige immunsubtyper i pan-cancer, ble immuninfiltrater delt inn i seks typer for analyse som tilsvarer henholdsvis tumorfremmende til tumorundertrykkende, inkludert sårheling, IFN-y dominant, inflammatorisk, lymfocytt utarmet, immunologisk stille og TGF-dominerende. Interessant nok var de fire pyroptoseregulatorene alle signifikant relatert til immunsubtyper, og de fire pyroptoseregulatorene ble mest uttrykt i IFN-y dominant, etterfulgt av TGF-dominant (fig.7B). I KIRC var imidlertid uttrykket av de fire pyroptoseregulatorene høyest i C2 på samme måte som pan-cancer-analyse. AIM2, som hadde det nest høyeste uttrykket i immunsubtyper, var relatert til Cl, mens NOD2, CASP5 og GZMB var relatert til C6 (fig. 2E).

Diskusjon
Kirurgisk reseksjon er den første behandlingen for nyrecellekarsinom i vår kliniske praksis. Imidlertid er det fortsatt vanskelig å fjerne nyrecellekarsinommetastaser. Metastatisk nyrecellekarsinom er resistent mot strålebehandling og systemisk terapi, inkludert hormonbehandling og kjemoterapi [13]. En klinisk studie av nivolumab, en anti-PD-L1 immunkontrollpunkthemmer, for behandling av metastatisk ccRCC (CheckMate-025) har vist at nivolumab har et betydelig overlegent OS, hazard ratio, ORR og generell responsrate [ 14]. Disse studiene indikerer at anvendelsen av immunterapi i behandlingen av ccRCC har store utsikter. En dybdeanalyse av heterogeniteten til ccRCC TIME kan bidra til å gi presis og individualisert immunterapibehandling for å forbedre behandlingseffekten og kvaliteten på pasientens prognoseoverlevelse. Her ble ccRCC-pasienter separert i to uavhengige molekylære subtyper med forskjellige kliniske egenskaper, immungenuttrykk og TIME gjennom konsensusklyngning for fire hovedpyroptoseregulatorer. I følge denne studien hadde klynge 2 en dårligere prognose enn klynge 1, men klynge 2 var mer følsom for immunterapi.
Blant de iboende dødsmekanismene til celler har pyroptose fått økende oppmerksomhet. Pyroptose er en nylig anerkjent type programmert inflammatorisk celledød som aktiveres gjennom veier mediert av klassiske caspase-1 inflammasomer eller ikke-klassiske caspase-4,caspase-5 og caspase{{4} } [15]. Nylig har nye bevis rapportert den viktige rollen til pyroptose i tumorigenesen av menneskelige maligniteter [16,17]. Pyroptose hemmer svulstvekst i tykktarmskreft, leverkreft og hudkreft, men det har en toveis effekt på brystkreft [18-20]. I ccRCC er det fortsatt ukjent hvordan pyroptose-relaterte gener samhandler og om de er relatert til pasientens overlevelsestid. Uttrykket av de fleste pyroptose-regulerende gener er positivt korrelert og spiller en viktig prognostisk rolle i ccRCC. Disse funnene tyder på at pyroptoseregulatorer kan spille en nøkkelrolle i å regulere tumorgenese og utvikling av ccRCC. I denne studien ble det identifisert fire pyroptoseregulatorer som er sterkt uttrykt i nyrekreft og forårsaker dårlig prognose. AIM2 er en cytosolisk medfødt immunreseptor som gjenkjenner dobbelttrådet DNA (dsDNA) frigitt under cellulær forstyrrelse og patogent angrep. Aktivert AIM2 aktiverer den klassiske banen for pyroptose gjennom caspase-1 [21]. AIM2 kan spille en unik rolle i forskjellige krefttyper [22-25], og denne studien viste at AIM2 spiller en kreftfremmende rolle i ccRCC. Caspase-5(CASP5), lik caspase-4 og caspase-1l, er et utøvende protein av caspase-1-uavhengig pyroptose [26]. GZMB brukes av cytotoksiske lymfocytter som et molekylært våpen for forsvar mot virusinfiserte og ondartet transformerte vertsceller [27]. Det lave uttrykket av GZMB er relatert til tidlig metastase i tykktarmskreft, noe som tyder på infiltrasjon av blodkar og nerver [28]. Interessant nok fant vår analyse at GZMB er et positivt korrelert gen i nyrekreft. NOD2 er en mønstergjenkjenningsreseptor som kan regulere vertens medfødte immunrespons og forhindre betennelse, steatose og fedme [29]. Ekstracellulært histon H3 indusert av LPS kan forårsake pyroptose under sepsis via NOD2 og VSIG4/NLRP3-veier [30]. Det er fortsatt ukjent hvordan disse genene interagerer med hverandre under cellepyroptose i ccRCC.
I vår kliniske praksis har vaskulære endotelvekstfaktorreseptor tyrosinkinasehemmere (VEGFR-TKI) blitt standarden for omsorg for mRCC [31]. Sunitinib, en bredspektret hemmer av reseptortyrosinkinaser, har blitt mye brukt som standard for behandling for førstelinjebehandling av avansert ccRCC [32]. Imidlertid er ikke alle RCC-pasienter følsomme for sunitinib-behandling, og de fleste pasienter vil utvikle resistens mot sunitinib etter noen måneders behandling. Derfor er nøkkelen til å velge sunitinib for behandling å velge pasienter som er sensitive for sunitinib. Den nåværende studien viste at klynge 1 er mer følsom for sunitinib, mens klynge 2 er mer følsom for axitinib.
Å forstå uttrykket av pyroptoseregulatorer i ccRCC før behandling kan bidra til å designe mer optimaliserte målrettede behandlingsalternativer til fordel for pasienter. Noen studier har vist at den effektive proinflammatoriske effekten av pyroptose er relatert til reguleringen av tumorimmunmikromiljøet [33]. Imidlertid er den potensielle rollen til pyroptose i immunmikromiljøet til ccRCC fortsatt unnvikende. Basert på uttrykksegenskapene til pyroptoseregulatorer, indikerte denne studien at pasienter i forskjellige klynger har forskjellige korrelasjoner med forskjellige immuninfiltrasjoner. Høyere infiltrerte nivåer av B-celler naive, T-celler CD4-minne hviler, NK-celler hviler, monocytter, makrofager M0 og makrofager M2 ble observert i klynge 1. På den annen side var klynge 2 høyere relatert til CD8 pluss T-celle-, Tregs- og T-follikulære hjelpeceller. Tregs kan skille ut en rekke immunsuppressive cytokiner, noe som fører til immunflukt fra tumorceller. Studier har vist at Tregs effektivt hemmer spredningen av effektor-T-celler og et høyt CD8+ T-celleinfiltrasjonsnivå er en ugunstig prognostisk faktor for ccRCC [34,35]. Den dårlige prognosen for klynge 2 og konklusjonene til disse to konklusjonene er gjensidig konsistente. Klynge 2 er positivt korrelert med åtte varme ICI-er (SIGLEC15, TIGIT, PD-L1, T IM3, PD-1, CTLA4, L AG3 og PD-L2). Basert på disse funnene kan de dårlige overlevelsesresultatene for klynge 2 være forårsaket av redusert nivå av antitumorimmunitet, og klynge 2 kan være mer fordelaktig i immunterapi. Resultatene av GSEA indikerer at klynge 2 er relatert til en rekke immunregulatoriske signalveier. Viktigere er at JAK-STAT-signalveien er relatert til karsinogenesen og immuninfiltrasjonen av ccRCC. Dermed spekulerte vi i at pyroptose kan regulere sammensetningen av tumorimmunmikromiljøet. Vår studie antydet at ccRCC med høy ekspresjon av disse 4 genene kan være mer følsomme for immunterapi.
Ekspresjonsnivået til de fire regulatorene økte med økende sykdomsstadium og patologisk grad, og det var ingen signifikant forskjell mellom uttrykket til de fire regulatorene og pasientens alder, noe som stemte overens med den dårligere prognosen for klynge 2.
Gitt at pyroptose er mye involvert i ulike biologiske prosesser, undersøkte vi om disse fire pyroptoseregulatorene i klynge 2 også spiller en viktig rolle i andre krefttyper. En pan-cancer-analyse ble deretter utført, og resultatene viste at disse fire pyroptoseregulatorene var nært beslektet med stromal score, immunscore og ESTIMATE score i flere krefttyper. Disse resultatene indikerte at disse fire pyroptoseregulatorene er potensielle mål for en rekke kreftimmunterapier og ikke er begrenset til ccRCC.
I fremtiden er det behov for ytterligere pålitelig verifikasjonsanalyse i et større kohort. I tillegg er det nødvendig med ytterligere in vitro og in vivo eksperimenter for å klargjøre reguleringsmekanismen mellom pyroptoseregulatorer og tumorimmune mikromiljø.
Konklusjoner
Oppsummert analyserte denne studien systematisk ekspresjonsprofilen til pyroptoseregulatorer i ccRCC og dens korrelasjon med immunkontrollpunkter og rollen i tumorimmunmikromiljøet. Uttrykket av pyroptoseregulatorer er signifikant relatert til immunkontrollpunkter som PD-L1 og CTLA4. To uavhengige undertyper ble også etablert gjennom den konsekvente klyngingen av pyroptoseregulatorer. Tumorheterogenitet og forskjeller i immunkontrollpunktuttrykk og tumorimmunmikromiljø ble observert mellom de to subtypene, noe som vil bidra til risikostratifisering og presis behandling av ccRCC-pasienter. En ett-trinns pan-cancer-analyse viste at disse pyroptoseregulatorene er nært beslektet med stromal score, immunscore og ESTIMATE score i mange krefttyper. Viktigere, fremtidige kliniske studier og grunnleggende forskning vil bidra til å bestemme mål for å forbedre effekten av kreftimmunterapi.
