Del 3: Skreddersydd funksjonalisering av naturlige fenoler for å forbedre biologisk aktivitet
Mar 28, 2022
For mer info. ta kontakt medtina.xiang@wecistanche.com
5. Lipidiske fenoler
Lipidiskfenoler(eller fenoliske lipider, også kalt fenolipider) er fenoler substituert med lipofile kjeder, som gir molekylets amfifile egenskaper. Et viktig fenollipid er -tokoferol[330]; Denne forbindelsen alene fortjener imidlertid en anmeldelse, så den er ikke inkludert.
Betydningen av naturlige lipidfenoler har vært undervurdert i lang tid [331]. Men deres utmerketantioksidant, antigenotoksiske og cytostatiske egenskaper er nå etablert [332], sammen med deres bioaktivitet i å påvirke biologiske veier involvert iAlzheimers sykdompatogenese 333]. Anti-inflammatoriske og anti-artritt aktiviteter ble også rapportert for lipidfenoler ekstrahert fra cashewnøtter (Anacardium occidentale) [334].
På grunn av viktigheten av en slik klasse av forbindelser, har flere syntetiske lipidfenoler blitt foreslått de siste tiårene for ytterligere å utvide deres biologiske anvendelser.

Klikk her for å lære flere produkter
5.1. Biokatalyserte synteser av lipidfenoler
Lipaser er de foretrukne enzymene for å utføre transesterifiseringsreaksjoner for å oppnå modifiserte eller syntetiske lipider, med funksjonelle eller farmasøytiske applikasjoner [335,336]. Et stort antall estere fra katekol og fettsyrer ble fremstilt for å røre en suspensjon av katekol i etylester av en fettsyre [337].
Halvsyntetiske lipidfenoler ble fremstilt ved transesterifiseringsreaksjoner av fenolsyrer med linfrøolje [338,339], olein [340], fiskeleverolje [341] og krillolje [342]. Reaksjonene, utført i organiske løsningsmidler eller i et løsningsmiddelfritt system [343,344], ble katalysert av Novozym 435 isolert av Candida Antarctica (skjema 33).

Mer nylig forbedret utbyttet ved bruk av superkritisk karbondioksid som reaksjonsmedium [345]. De fremstilte blandingene av lipidfenoler ble testet for antioksidantaktivitet. Den oppnådde radikalfjernende aktiviteten varierte fra moderat til god, men den var alltid lavere enn -tokoferol. Resultatene ble dessuten oppnådd fra blandinger og kunne ikke tilskrives en enkelt forbindelse.
Motsatt ble rene fenollipider med fettsyrer med varierende kjedelengde fremstilt med ferulsyre [346]. Syntesen involverte et biokatalysert trinn (av Nosozyme) (skjema 34).
Deantioksidant aktivitetundersøkelser ga blandede resultater fordi radikalfjerningsanalysen ikke viste noen forbedring med hensyn til ferulsyre, mens autooksidasjon av linolsyre i et micellært system viste en viss forbedring, tilskrevet økt løselighet.

Kjemo-enzymatisk syntese av fosfatidylkoliner som inneholder fenolsyre og fettsyrer ble rapportert [347], med ett av de aktive derivatene, 1-(4-hydroksy-3,5-dimetoksy) cinnamoyl-2-acyl-sn-glycerol-3-fosfokolin, som viser utmerket antioksidantaktivitet.
En annen tilnærming var å oppnå lipidfenoler fra en fenol og frie fettsyrer eller tilsvarende estere, med immobilisert lipase fra Candida Antarctica som biokatalysator [348]. Antioksidantaktiviteten til tyrosol ble økt ved acylering, men det ble ikke funnet noen sammenheng med antall dobbeltbindinger i fettacylgruppen (skjema 35).

Noen estere ble syntetisert fra naturlige fenoler og -liponsyre i en reaksjon katalysert av Novozym 435 (den immobiliserte lipase B fra Candida Antarctica) i en butanon-heksanblanding [349]. Antioksidantaktiviteten ble bestemt ikke bare ved radikalfjerningsanalyse, men også ved å måle inhiberingen av oksidasjonen i en tunfiskeoljeemulsjon. Esteren 2-(3,4-dihydroksyfenyl)etyl-5-(1,2-ditiolan-3-yl)pentanoat, oppnådd fra tyrosol og -liponsyre, fulgte ved aromatisk hydroksylering (Scheme36), viste utmerket antioksidantaktivitet i begge testene, og ifølge forfatterne kan den brukes som pro-drug, fordi den ved hydrolyse frigjør forbindelser som er ikke-toksiske eller til og med sunne.

Senere ble det funnet at 2-S-lipoyl-koffeinsyremetylester var en hemmer av tyrosinase fra humane melanomceller [350].
Målet om å tilberede en enkelt lipidfenol, unngå plagsom separasjon av en komplisert blanding, ble oppnådd ved en flertrinnsstrategi som involverer både kjemisk og enzymatisk katalyse. Immobilisert lipase fra Candida Antarctica (CAL-B) ble brukt i et organisk medium [351] (skjema 37).
![Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol Chemo-enzymatic approach for the synthesis of 1-[11-(ferulyloxy)undecanoyl)]glycerol](/Content/uploads/2022842169/20220328111325cc1b5fb0d7394a028caf7ce4b3cdd52d.png)
Etter karakterisering gjennomgikk den tilberedte 1-[11-(ferulyloksy)undecanoyl)glyserol antimikrobielle, antioksidant- og cytotoksiske studier. Den antimikrobielle aktiviteten var moderat, antioksidantaktiviteten var utmerket og aktiviteten mot noen kreftcellelinjer var lovende, så forfatterne forutså potensielle kosmetiske og biomedisinske anvendelser.
Transesterifiseringsreaksjon med Candida Antarctica lipase B ble utført, behandlet 4-hydroksyfenyleddiksyre med triolein og fiskeolje, og oppnådde syntetiske stoffer som har både antioksidant og antibakteriell aktivitet [352].
5.2. Kjemiske synteser av lipidfenoler
Lipidfenoler ble fremstilt som estere, enten fra fenoler med langkjedede karboksylsyrer eller fra fenolsyrer. Utvalgte eksempler på syntetiske lipidfenoler er rapportert i tabell 1.

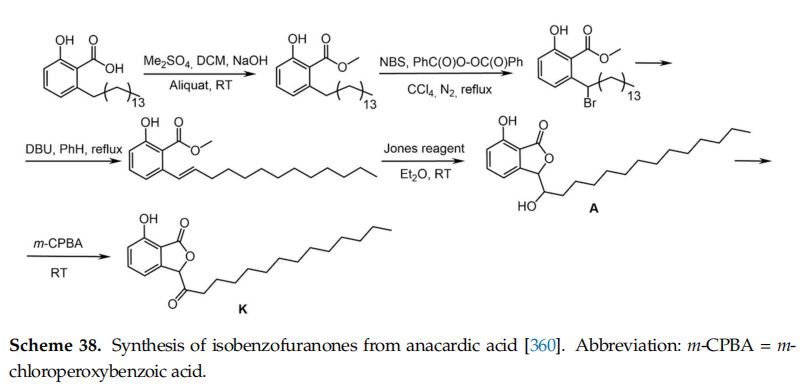
Anakardinsyre, fra ferske og tørre cashewnøtter av Anacardium occidentale, ble transformert til isobenzofuranoner, som illustrert i skjema 38, med en alkohol(A) eller keto(K)funksjonalitet i den langkjedede [360].
Både isobenzofuranoner A og K, så vel som den asykliske forløperen, var moderat til signifikant aktive i cytotoksisitetsscreening med forskjellige humane kreftcellelinjer.
En god antioksidantevne til å stabilisere olivenolje ble observert med en familie av fenoliske fettsyreestere, fremstilt av 3,4-dihydroksybenzoylalkohol (protokatechuisk alkohol) eller hydroksytyrosol og fettsyrer. Reaksjonen ble utført i vannfri THF, i nærvær av et karbodiimid og DMAP[361]. Alle de tjue forbindelsene ble undersøkt som potensielle antioksidanter i raffinert olivenolje. Lengden på alkylkjeden festet til fenylringen ser ut til å påvirke aktiviteten.
Etter funnet at 5-alkyl- og 5-alkylresorcinoler, isolert fra sopp-Merulius incarnates, hemmet meticillin-resistent Staphylococcus aureus [362], var en god syntetisk metode nødvendig, fordi de ikke er lett tilgjengelige. tilgjengelig, men er viktig for analytiske, metabolske og bioaktivitetsstudier. En generell metode, basert på Wittig-reaksjonen, ble utviklet [363] for å overvinne problemet med alkylkjedeinnføring i den aromatiske ringen. Problemet ble løst ved å reagere langkjedede alkanoler, når tilgjengelige, med semi-stabiliserte benzylfosfoniumylider eller alternativt 3,{10}}dimetoksybenzenkarbaldehyd med alkylfosfoniumylider. Prosedyren ga 5-alkylresorcinoler med alkylkjeder opptil 25 C-atomer. Reaksjonen ble utført i vann eller en vann-DMSO-blanding, med MW-bestråling, i trykksatt eller i en åpen beholder. Ett eksempel for hver rute er vist i skjema 39.

Moderat til god in vitro antioksidantaktivitet ble vist av 1,2-dibutanoyloksy-2-(4-hydroksy-3-metoksyfenyl)etylbutanoat, en lipidfenol oppnådd fra ferulsyre [354] .
2-Metyl-5-[(2Z)-non-2-en-1-yl]benzen-13-diol og 5-[(2Z)-non{ {10}}en-1-yl]benzen-1,2,3-triol ble fremstilt som syntetiske derivater av den naturlige 5-[(2Z)-non{{18} }en-1-yl]benzen-1,3-diol (climacostol), et forsvarskjemikalie i protozoen Climacostomum virens[355]. De strukturelle modifikasjonene i den aromatiske ringen (henholdsvis en metyl- og en hydroksylgruppe) økte toksisiteten.
Long-chain alkyl hydroxycinnamates were prepared from the corresponding monoesters of malonic acid and benzaldehyde derivatives by Knoevenagel condensation [364]. The observed antioxidant activity followed the order caffeic esters > sinapic esters >feruliske estere.
12-Hydroksy-9-oktadekansyre (ricinolsyre) ble transformert til (Z)-metyl-12-aminooktadeka-9-enoat og deretter reagert med fenolsyrer, og dannet de tilsvarende amidene [356 ]. Den undersøkte antioksidantaktiviteten indikerte at modifikasjon av fenolsyrer med lipofile deler forbedrer deres antioksidant- og antikreftegenskaper.
Det er verdt å signalisere en konseptuelt annen type lipidfenoler, nemlig fenylsulfonylfuroksanderivatene av koffeinsyre og andre fenolsyrer [357]. Foruten gode antioksidantaktiviteter in vivo, viste disse forbindelsene antikoagulerende og vasodilatasjonseffekter som ble tilskrevet den NO-frigjørende evnen.
Koffeinsyre eller 3,4-dimetylkoffeinsyrer ble reagert med eplesyre og deretter koblet med monoglyserider av fettsyrer med kjedelengder fra 8 til 18 C-atomer [359]. Kombinasjonene av fenol- og fettsyrer ga en serie på seks amfifile forbindelser som ble testet for aktivitet. De viste seg å være ikke-giftige og ga stabile olje-i-vann-emulsjoner, med potensial for bruk i mat-, farmasøytisk og kosmetisk industri, ifølge forfatterne.

6. Polyfenoler
Naturligpolyfenolerutgjør en tallrik og stort sett distribuert gruppe av bioaktive molekyler i spiselige planter, med bioaktiviteter som spenner fra kardiovaskulær beskyttelse til forebygging av kreft [365-368].
Polyfenoler er karakterisert ved tilstedeværelsen av en benzo-smeltet heteroaromatisk ring av pyren- eller Pyridium-typen. De er vanligvis navngitt av en semi-systematisk nomenklatur, basert på den overordnede heterosyklusen. Således kalles benzopyrenderivater med en fenylsubstituent flavoner, mens fenolsubstituerte benzofenoner er indikert som flavoner. Strukturene til stamforbindelser og deres fenylderivater er samlet i figur 9.

Syntesen av naturlig og semisyntetisk høyoksidert bioaktivpolyfenolerble gjennomgått i 2008, og diskuterte fremskritt og utfordringer [369]. Alternativt kan mer effektiv og bærekraftig produksjon komme fra mikrobielle cellefabrikker, som gjennomgått i 2018 [370].
Kjemiske transformasjoner av naturlige fenoler kan føre til mer effektive arter hvis strukturelle trekk på grunnlag av biologisk aktivitet er forstått. Følgelig er resultater av kjemiske modifikasjoner for representative polyfenoler rapportert i det følgende.
6.1.Fenoler fra Chroman
Catechin er en polyfenol fra flavanolfamilien som finnes i grønn te. Derivater rapportert i figur 10 ble fremstilt fra racemisk katekin (tetrametoksy, pentaacetoksy og syklisk) [371]. Katekin og derivatene ble testet for antimikrobiell aktivitet mot rotkoloniserende sopp, som ble opprettholdt, men med lavere effektivitet, i de mindre polare forbindelsene.

Den antioksidative radikalfjerningen av (pluss)-katechin, undersøkt mot galvinoksylradikalet, forsterkes ved reaksjon med ninhydrin [374].
For å løse problemet med økende resistens av mikroorganismer, ble studier rettet mot å forberede og teste syntetiske derivater av katekin. Den systematiske foretringen av 3-hydroksylgruppene med lineære alkylkjeder av forskjellig lengde eller med substituerte benzylgrupper ga et bibliotek av 3-O-alkylanaloger av katekin [372] som ble brukt til å teste den antifungale aktiviteten som en funksjon av strukturen. Forbindelser med lengre kjeder (C14-C16) viste svakere aktiviteter enn forbindelser med C8-C12-kjeder.
Dessuten, ved å variere -OH-funksjonaliteten i 3, ble tolv derivater av (-)-katechin fremstilt [373]. Bare tre forbindelser viste antibakteriell og soppdrepende aktivitet høyere enn standardmedisinene (neomycin og mikonazol). Molekylær docking-studier stemte overens med eksperimentelle resultater.
Brazilin og den oksiderte analogen brazilein (Figur 11) er kromanderivater som finnes i planter (Caesalpinia sappan L.), kjent for sine anti-inflammatoriske egenskaper. Nye syntetiske derivater ble fremstilt for å utforske deres antitumoraktivitet. Syntesen av brasilianere [375] ble oppnådd med utgangspunkt i 1,3-dihydroksybenzen (resorcinol) og 3-klorpropansyre, med dannelsen av nøkkelmellomproduktet 7-hydroksy-4-kromanon . De syntetiserte brasilianerne (figur 11) ble testet for anti-inflammatoriske effekter mot en rekke humane kreftcellelinjer, men bare noen av de syntetiske derivatene viste en viss forbedring i forhold til det usubstituerte brazileinet.

6.2. Fenoler fra Chromen
Kumarin (2H-chromen-2-one), det vanligste derivatet av kromen, og substituerte kumariner finnes i grønne planter, hvor de utøver forskjellige virkninger [377].
Tatt i betraktning allsidigheten av reaksjoner som fører til kumarin-heterosykkelsystem [378, ble en rekke substituerte kumariner syntetisert og lovende aktivitet ble funnet med kumarin-fusjonerte 14A-tiazepiner, syntetisert med utgangspunkt i 4-hydroksykumariner(skjema 40)[379].

Kumariner og benzokumariner substituert med en hydroksylgruppe i 7-eller 8--posisjoner ble fremstilt og testet in vitro for en rekke biologiske aktiviteter [380]. Generelt leverte de kraftige superoksidanionfjernere og hemmet in vitro lipidperoksidasjon; på den annen side viste de ikke signifikant lipoksygenase-hemmende aktivitet.
6.3.Fenoler fra Chromon
Quercetin (3,3'4',5,7-pentahydroksyflavon) er en flavonol som stort sett finnes i planter, matvarer og drikkevarer, ofte sammen med fisetin (3,3'4',7-tetrahydroksyflavon) .
Interessen for quercetin ble tilskyndet av dets anti-kreft, anti-inflammatoriske og antioksidant roller. Spesiell relevans tilbys av den antihypertensive effekten [381]. Mange syntetiske derivater ble fremstilt med det formål å oppnå anti-kreftkandidater som kan overvinne quercetin-problemer: (i) lav løselighet i vann, (ii) lav biotilgjengelighet og (ii) rask nedbrytning. Studier på biologisk aktivitet var ikke tilstrekkelig til å vurdere den faktiske effektiviteten til disse derivatene, selv om noen av dem virket lovende [382]. På den annen side ga enkel kompleksdannelse med Cu(I) et Cu(quercetin)(bipy)-kompleks med forbedrede antioksidantegenskaper sammenlignet med fritt quercetin [383].
Interessen for de terapeutiske egenskapene til quercetin og derivater er ikke begrenset til cytotoksisitet, som kan sees av antall patenter rapportert mellom 2010 og 2015 [384]. Utvalgte meningsfulle eksempler er samlet i tabell 2.

De fleste av slike derivater involverte transformasjoner ved alle hydroksylgruppene, med modifikasjonen ved C-3-hydroksylgruppen som resulterte i en forbedring av antikreftaktivitet. Dessuten ble bioaktiviteten betydelig økt av nanoteknologi.
Problemet med lite løselighet i vann avflavonoiderpolyfenoler ble adressert med tanke på derivater med hydrofile substituenter, slik som sulfat [385].
En annen tilnærming var å tilberede konjugater av sukker med flavonoid som aglykon. Glukose, galaktose og rhamnose ble blant annet brukt.
Enzymatisk syntese var vellykket i å modifisere naturlige forbindelser, noe som ga ikke bare mer løselige, men også mer effektive arter i medisinske [386] eller kosmetiske [387] applikasjoner.
Det er interessant at rutin (2-(3,4-dihydroksyfenyl)-5,7-dihydroksy-3-[ -L-rhamnopyranosyl-(1→6){ {11}}D-glukopyranosyloksy]-4H-kromen-4-on) ble videre transformert ved enzymatisk transesterifiseringsreaksjon til mono- og diacetatderivater (skjema 41) med opprettholdte antioksidantegenskaper og mer effektiv evne til å penetrere cellemembranen til murine makrofager [388]. Dessuten var acetoksy-substituerte rutiner ikke toksiske for pattedyrceller, og enzymet kunne gjenbrukes.

Betydningen av sukkersubstituerte flavonoider er eksemplifisert ved myricitrin (myricetin-3-O- -L-rhamnopyranosid), hvis antioksidantaktivitet hadde en beskyttende effekt mot DNA-skader [389].
Et nytt flavonoidstillas ble utarbeidet for å introdusere salisylat- og trimetoksybenzengrupper i flavonoider [390]. Alle forbindelsene ble evaluert for antiproliferativ aktivitet mot tre humane tumorceller som viste moderat til god aktivitet.
6.4.Fenoler fra 2,3-dihydrokromon
Blant flavanoner, sekundære metabolitter av planter med et bredt spekter av biologiske aktiviteter, ble nålestriping (5-hydroksy-7-metoksyflavanon) interesse fordi det er hovedkomponenten i rotstokken til fingerrot (Kaempferia pandurata), brukt i sørøstasiatisk matlaging, kjent for å ha flere farmakologiske aktiviteter, blant annet den antimikrobielle er lovende.
Allylering og prenylering av pinostrobin ble utført ved bruk av MW-bestråling (Mitsunobu- og metatesereaksjoner, Claisen og Cope-omorganiseringer) (skjema 42), og ga forbindelser som ble testet mot en rekke kreftcellelinjer [391]. Derivatene var mer reaktive enn pinostrobin, et resultat som forfatterne tilskrev en bedre interaksjon med de biologiske målene, på grunn av den økte lipofilisiteten gitt av alkenylsubstituenter.

Pinostribin ble prenylert under enkle SN2-betingelser (skjema 43), noe som ga en blanding av produkter, hvorav de fleste mistet flavanonstrukturen. De ble separert og testet for antimikrobiell aktivitet [392], og viste en moderat effekt. Interessant nok ble flere prenylerte kumariner og quercetiner isolert fra rotbarken til Broussonefia papyrifera som metabolitter med, i noen tilfeller, cytotoksisk aktivitet [393].

Astilbin, et sukkerderivat av flavanoltaxifolin, utvinnes fra urtemedisinske planter, ofte brukt i tradisjonell kinesisk medisin. For deres mulige farmasøytiske bruk er imidlertid astilbin tilgjengelig fra ekstraksjon ikke tilstrekkelig. En effektiv prosess for å oppnå astilbin fra taxifolin var avhengig av mikrobiell fermentering i genetisk konstruert Escherichia coli (skjema 44) [394].

Et kaskade biokatalytisk system ble utviklet for å fremstille 4'-O-glukosidderivatene av naringenin (5,7-dihydroksyflavanon), et flavonoid med flere bioaktive effekter, funnet i druer og appelsiner [395]. Metoden er avhengig av å regenerere uridin difosfat fra sukrose og gjenbruke det, og utfører også preparativ skalaproduksjon. Ved samme metode ble quercetin 7-OaL-rhamnoside oppnådd.
Interessant nok viste myricitrin (myricetin-3-O- -L-rhamnopyranosid)[389] og naringenin, tilstede i ekstrakter av Cynara cardunculus, et kraftig naturlig ugressmiddel, fytotoksiske effekter på bladene til Trifolium incarnatum, og åpnet vei til naturlige ugressmidler, et felt som blir stadig viktigere på grunn av den økende motstanden til ugress mot ofte brukte [396].

7. Curcumin og Curcuminoids
Curcumin, [1,7-bis(4-hydroksy-3-metoksyfenyl)-1,6-heptadien-3,5-dionel, en gult pigment isolert fra gurkemeie (Curcuma longa Linn), er en multifunksjonell forbindelse som, i det minste fra å lese litteraturen fra de siste tjue årene, virker som en slags universalmiddel for alle sykdommene i det moderne samfunnet, inkludert kreft og Alzheimers sykdom. Fenol-OH-grupper sikrer antioksidantegenskapene, mens den omfattende konjugasjonen på grunn av ketoenollikevekten (skjema 45) er grunnlaget for fotodynamisk aktivitet.

Flere nylige anmeldelser diskuterer aspektene ved biologisk aktivitet [397-400] og mulige medisinske anvendelser [70 292,401-404] av curcumin og derivater. Viktige aspekter, som nye leveringsmetoder og synergistiske effekter med andre forbindelser, ble også diskutert, sammen med virkningsmekanismen [405]. En økende interesse vies curcuminbaserte legemidler mot nevrodegenerative sykdommer [406], spesielt Alzheimers [407] og kreft [408].
Jakten på nye curcuminderivater er motivert av (i) nødvendigheten av å øke materialtilgjengeligheten, og (i) nødvendigheten av å forbedre løseligheten i en vandig løsning.
Spesielt ved å behandle curcumin med Cu(II), ble et Cu(curcumin)(bipy)-kompleks isolert og det var en bedre antioksidant og DNA-binding sammenlignet med fritt curcumin mens det var mindre giftig, på grunnlag av dets antifungale egenskaper [383] . Det ble også rapportert at sølv-curcumin nanokonjugater, fremstilt ved en sonokjemisk metode, ble testet på hudcellelinjer og for antibakteriell aktivitet mot Escherichia coli. Resultatene indikerte at sølvnanopartikler ble gjort biokompatible av curcumin, mens de gjør curcumin mer fotostabilt og mer aktivt som et antibakterielt middel [409].
Vi diskuterer curcuminderivater i henhold til strukturelle endringer.
7.1. Mindre strukturelle endringer
Små strukturelle endringer kan endre effektiviteten tilcurcuminbioaktivitet. For eksempel ble introduksjon av en metylgruppe i posisjon 2 eller to metylgrupper, som i 2,7-dimetylcurcumin, økt anti-angiogeneseaktivitet og undertrykkelse av tumorvekst [410] observert, sammen med økt antiinflammatorisk aktivitet [411 ] og stabilitet mot enzymatisk reduksjon [412], med hensyn til curcumin.
Diacetylcurcumin, lett fremstilt ved acetylering av moderforbindelsen, viste utmerket antibakteriell aktivitet [413] og det var effektivt i antiartritisk aktivitet hos mus (tabell 3) [414].



Antioksidantaktiviteten til curcumin ble sammenlignet med den til dimetoksymetabolitter og hydrogenerte derivater [415]. Resultatene indikerte at de mettede derivatene (tetrahydro-, heksahydro- og oktahedron-kumariner) har økt antioksidantaktivitet med hensyn til kumarin (tabell 3).
Derivatet oppnådd ved innføring av prenylsubstituenter i begge aromatiske ringene ble testet mot oksidativt stress [416] (tabell 3), og viste like eller bedre antioksidantegenskaper med hensyn til curcumin.
En mer drastisk substitusjon ble utført, ved å introdusere elektrontrekkende substituenter i benzenringer, eller til og med kondensering av heterosykler (tabell 3) [417].
7.2. Substituenter i den U-umettede kjeden
De fleste syntetiske derivater kommer fra introduksjonen av substituenter i posisjon 4, og påvirker dermed curcumin tautomer likevekt. Viktig bioaktivitet knyttet til keto-enol likevekten er interaksjonen med amyloid (A) aggregering, tilstede ved Alzheimers sykdom. En omfattende undersøkelse av keto-enol tautomere likevekter i substituerte curcuminer ble utført [432-434]. Nylig ble det rapportert at 4,4-disubstituert curcumin (Figur 12), der ketoformen er den eneste mulige, binder ikke-fibrillære løselige A-oligomerer, og blir, som forfatterne sier," en førstegenerasjons forbindelse rettet mot A-oligomerer" [435].
Fluorerte curcuminderivater viste betydelig hemming av det tioredoksininteragerende proteinet (TXNIP), som er assosiert med flere sykdommer [418].
Et antall curcuminderivater substituert med syre- eller estergrupper i posisjon 4 ble fremstilt [436] (Figur 13). Surhet, lipofilisitet og kinetisk stabilitet ble bestemt, sammen med frie radikalfjernende aktivitet, for å evaluere ethvert forhold mellom struktur og aktivitet. Esterderivatene viste selektivitet mot kolonkarsinomceller, sannsynligvis som et resultat av deres høyere lipofilisitet takket være curcumin.
![The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers The 4-Substituted curcumins that inhibit the formation of large amyloid aggregates [434] and 4,4-disubstituted curcumin that binds amyloid oligomers](/Content/uploads/2022842169/20220328112546d633ce9f0cd54ad68e1c33ed5c4758d7.png)

En annen tilnærming var introduksjonen av en umettet del i posisjon 4 (tabell 3), ved Knovenagel-reaksjon med benzenkarbaldehyd, 4-hydroksybenzaldehyd og 4-hydroksy-3-metoksy-benzaldehyd (vanillin)419 ]. De oppnådde derivatene ble testet for anti-malaria-aktivitet mot P. falciparum, og vanillinderivatet var betydelig potent.4-Benzylidenkurkuminer, fremstilt av 2-hydroksybenzenkarbaldehyd [420] og 4-benzylidenkurkuminer, ble undersøkt som antioksidantmidler, og begge var effektive for å dempe grå stær i dyrkede rottelinser.
7.3. Modifikasjon av -dikarbonyldelen
18 nye derivater, som fortsatt inneholder hepta-1,6-dien-3,5-dionstrukturen til curcumin, men med en av karbonylgruppene innlemmet i cykloheptanondelen, ble syntetisert av en allsidig syntetisk strategi [421]. Ett eksempel på substituert tropinon er rapportert i tabell 3. Forfatterne er sikre på at familien av dikarbonylcurcuminer med tropanringen vil ha viktig aktivitet siden de enkle monokarbonyltropanonene var cytotoksiske mot brystkreftceller.
Et bibliotek av curcuminderivater ble oppnådd ved reaksjon med en eller to ekvivalenter sulfonamider (valgt blant sulfa-medisiner) (skjema 46) [437]. Antibakterielle og antifungale aktiviteter ble evaluert mot Gram-positive og Gram-negative mikroorganismer, med gode resultater.

3,4-Dihydropyrimidin-2(1H)-on og tionanaloger av curcumin (tabell 3) ble syntetisert i godt utbytte ved en én-pots multi-komponent cyklokondensasjon under MW-bestråling [425]. Antibakterielle og antioksidantstudier ble utført in vitro med resultater som av forfatterne ble ansett som "moderat" i det førstnevnte tilfellet og "utmerket" i det sistnevnte.
Et pyrazolderivat av curcumin ble fremstilt for å prøve å inkorporere i det samme molekylet de strukturelle egenskapene til curcumin og av asteroidelignende forbindelse (cykloheksylbisfenol A) [422]. Forbindelsen ble funnet å være nevrobeskyttende i cellekulturanalyser, også mot intracellulær og ekstracellulær amyloid. Dessuten ble det funnet å ha minneforbedrende egenskaper i en gjenkjenningstest for rotteobjekter [423].

7.4. Delvis erstatning av -dikarbonyldelen
Delvis erstatning av -dikarbonyldelen av curcumin ble ansett som nyttig for å overvinne problemet med dens utilfredsstillende stabilitet. En serie monokarbonylanaloger av curcumin, syntetisert fra det opportunt substituerte benzaldehydet og en cykloalkan [438-440]. Stabiliteten til de substituerte cyklopentanonene og cykloheksanonene ble forbedret in vitro. Den cytotoksiske aktiviteten var også høyere med cykloheksanoner, med bemerkelsesverdig betydning av substituenter elektroniske effekter (skjema 47).

Aminokarbonylcurcuminanalogene ble testet mot pro-inflammatoriske cytokiner, og viste en kraftigere hemmende evne enn curcumin.
Symmetriske bis(aryliden)ketoner ble fremstilt ved å reagere cykloalkanoner med substituerte benzaldehyder, i en syrekatalysert aldolisk kondensasjon. De fleste av de syntetiserte forbindelsene viste hemming av eggstokkreftcellevekst, selv med celler som var resistente mot cisplatin [441].
Flere syntetiske aminokarbonylcurcuminanaloger ble testet mot Trichomonas vaginalis (regnes som den "vanligste ikke-virale seksuelt overførbare infeksjonen i verden")[442];15-difenylpenta-1,4-dien{ {5}}en,15-bis(2-klorfenyl)Penta-1.4-dien-3-en og 2,6-bis({ {13}}klorbenzyliden)cykloheksanon viste signifikant antiparasittisk aktivitet ved effektive konsentrasjoner lavere enn curcumin.
Nylig ble et første, men meget lovende resultat oppnådd med (2E,6E)-2,6-bis(2(trifluormetyl)benzyliden)cykloheksanon, som ble funnet å helbrede diabetiske sår i mus [426] (tabell 3).
Et dusin curcuminaminokarbonylanaloger ble syntetisert for å finne forbindelser med økt kjemisk stabilitet og til slutt bedre antikreftaktivitet mot noen menneskelige kreftceller [427]. To av dem (tabell 3) oppfylte kravene og ble suksessivt testet mot melanomceller, noe som resulterte i selektivt toksisk428].
Nye curcuminoider som inkorporerte 4H-pyran heterosykler ble fremstilt ved én-pots kondensasjon av curcumin med propanodinitril og et substituert benzenkarbaldehyd (skjema 48) [443]. Den påfølgende modifikasjonen av -dikarbonyldelen forbedret inhiberingen av -glukosidasen, et av enzymene som er ansvarlige for karbohydrathydrolysering og derfor for postprandial hyperglykemi. Denne funksjonen, sammen med antioksidantaktivitet, har mulige gunstige konsekvenser mot diabetes mellitus, spesielt fordi ingen toksisk effekt ble observert på den vanlige menneskelige tarmens mikroflora.

7.5. Reduser lengden på umettet kjede
En curcumin-analog, 5-(3,4-dihydroksyfenyl)-3-hydroksy-1-(2-hydroksyfenyl)Penta-2,4- diene-1-one viste antiinflammatorisk aktivitet hos mus (tabell 3)[429]. Lignende forbindelser med samme skjelett ble brukt for å fastslå viktigheten av oppregulering av reaktive oksygenarter i undertrykkelsen av tumorigenese [444]. Ifølge forfatterne er disse forbindelsene lovende for utviklingen av et kreftmedisin med få bivirkninger.
En lignende, men kortere forbindelse, (Z)-3-hydroksy-1-(2-hydroksyfenyl)-3-fenylprop-2-en-1-on, ble fremstilt for å starte fra 2-hydroksyfenylmetylketon og benzoyl
klorid (skjema 49). Det resulterende molekylet viste selektiv cytotoksisitet på brystkreft MCF-7-celler [445], humane tykktarmskreftcellelinjer [446] og humane osteosarkomceller [447].

7.6. Derioatioes med bare "halvparten" av curcuminstrukturen
En familie av forbindelser, navngitt av forfatterne retro-curcuminoider, ble forberedt for å opprettholde bare "halvparten" av curcuminstrukturen (skjema 50), fordi -dikarbonyldelen ble ansett som ansvarlig for curcumin-knapphet stabilitet [448]. De resulterende forbindelsene viste relevant cytotoksisk aktivitet mot humane kreftcellelinjer, men de skadet ikke friske celler.

En syntetisk amidanalog viste antioksidative og antiinflammatoriske egenskaper. Det ble testet med gode resultater på hepatisk steatose hos mus med indusert fedme [430] (tabell 3).
Et bibliotek av curcumin-resveratrol-hybrider ble syntetisert med utgangspunkt i hydrazidderivatet av substituert kanelsyre og en serie substituerte benzaldehyder [449]. Eksemplet illustrert i skjema 51 refererer til den mest lovende hybriden som et antitumor-multimålmiddel.

7.7. Fotosensibilisatorer
Curcumin kan være en utmerket fotosensibilisator, på grunn av sin gode biokompatibilitet, men den praktiske bruken er sterkt begrenset av dens lave stabilitet og knappe løselighet i vann. En løsning ble søkt for å fremstille curcuminderivater med kationiske substituenter [450] (Figur 14).

Alle derivatene viste høy stabilitet med pH og temperatur. Når det gjelder fotodynamiske egenskaper, var de i stand til å fremme fotodynamisk inaktivering av E.coli, med den heksakationiske arten som den mest effektive, sannsynligvis på grunn av den høye hydrofilisiteten.
En sammenlignende studie ble utført på forskjellige curcuminderivater syntetisert ad hoc, med sikte på å øke vevspenetrasjonen, øke absorpsjonsmaksimum. Således, 1,11-difenyl-1,3,8,10-undekatetraen-57-dion og 1,7-bis(4'-dimetylaminofenyl){{11 }},6-heptadienyl-3,5-dion presenterte lovende egenskaper når det gjelder generering av reaktive oksygenarter og derfor effektivitet i fotodynamisk terapi [431]. 8. Konklusjoner
Naturlige fenoler og deres derivater med biologisk aktivitet utgjør et raskt voksende forskningstema, med tanke på deres mange nåværende og fremtidige anvendelser. Deres strukturelle mangfold gir mange muligheter for kjemiske transformasjoner, rettet mot å overvinne ulempene med naturlige fenoler. Men bortsett fra noen retningslinjer som dukket opp fra det enorme antallet publikasjoner, som behovet for å forbedre stabiliteten og biotilgjengeligheten til de bioaktive forbindelsene, er bildet av strukturelle krav ennå ikke komplett, med tanke på optimalisering av in vivo og in-field-applikasjoner .
