Acteosid, en komponent av Stachys Sieboldii MIQ, kan være et lovende antinefritisk middel: effekt av akteosid på halvmånetype anti-GBM-nefritt hos rotter
Mar 08, 2022
For mer informasjon:ali.ma@wecistanche.com
Kazumi Hayashi, Tadashi Nagamatsu, Mikio Ito, Tomohisa Hattorian og Yoshio Suzuki
Institutt for farmakologi, Farmasøytisk fakultet, Meijo University, 150 Yagotoyama, Tenpaku-Ku, Nagoya 468, Japan
ABSTRAKT
Effekten avakteosid(ACT) på anti-GBM av halvmånetypenefritthos rotter ble undersøkt. Når rotter ble behandlet medActeosidfra den første dagen etter iv injeksjon av anti-GBM serum,Acteosidhemmet forhøyet proteinutskillelse i urinen. IActeosid-behandlede rotter, kolesterol- og kreatinininnhold og antistoffproduksjon mot kanin-r-globulin i plasmaene var lavere enn hos de nefritiske kontrollrottene. Histologisk observasjon viste at dette midlet undertrykte hypercellularitet og forekomsten av halvmånedannelse, adhesjon av kapillærveggen til Bowmans kapsel og fibrinoid nekrose i glomeruli. Videre var rotte-IgG- og C3-avsetninger på GBM betydelig mindre iActeosidbehandlet gruppe enn i kontrollnefritgruppen. Når behandlingen ble startet fra den 20. dagen etter iv injeksjon av anti-GBM-serum, hvorved sykdommen var etablert,Acteosidresulterte i en lignende effekt pånefritiskrotter som nevnt ovenfor. Disse resultatene tyder på at Acteosid kan være en nyttig medisin mot raskt progressiv glomerulonefritt, som er preget av alvorlige glomerulære lesjoner med diffuse halvmåner.
Nøkkelord: Crescentic-type anti-GBMnefritt,Acteosid, Rotte-IgG, Rotte-C3

Klikk for å Cistanche bruker med Acteoside
Chyorogi Stachys sieboldii MIQ (Labiatae) er foreskrevet for mange sykdommer, og denne knollen brukes som mat av kinesere, russiske og japanske. Nyere undersøkelser har vist at chyrogi har antianoksi-virkning(1), hemmende virkning på hyaluronidase-aktivitet (2) og immunsuppressiv virkning (3).
På den annen side har det blitt nevnt at immunresponsen deltar i utviklingen av nefritt. For å si det mer konkret, er glomerulær skade mediert av immunkompleksavsetning i glomeruli, etterfulgt av immuninflammatorisk reaksjon, inkludert komplementaktivering og frigjøring av andre inflammatoriske mediatorer. I nyere studier har det blitt viet mye oppmerksomhet til bidraget til den cellemedierte immunresponsen i utviklingen av glomerulonefritt (4, 5). Dessuten har Neild et al. (6) rapporterte at undertrykkelse av T-cellefunksjon av cyklosporin A (CyA) blokkerte den påfølgende utviklingen av glomerulære lesjoner ved akutt sykdomsnefritt. Vi rapporterte at mizoribin (7), azatioprin (7), CyA (8), metylprednisolon (9) og noen plantekomponenter (10) har immundempende virkning, viste en helsebringende effekt på anti-GBM-nefritt. Selv om disse immunsuppressive midlene utøver antinefritisk virkning, er det vanskelig å bruke dem i kliniske studier på grunn av deres bivirkninger (11). Derfor forventes et nytt immunsuppressivt middel for behandling av nefritt i det kliniske stadiet å bli utviklet.
Hensikten med denne studien var å belyseanti-nefritisk effekt av akteosid, en komponent av chyorogi, på halvmånetype anti-GBM-nefritt hos rotter.
MATERIALER OG METODER
Dyr
Sprague-Dawley-hannrotter som veier ca. 160 g (Nihon SLC, Hamamatsu), ble brukt til alle forsøk. Disse dyrene ble holdt i et luftkondisjonert rom ved 23 ± 1 C under forsøksperioden.
Narkotika
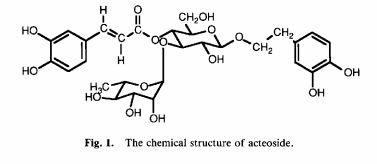
Den kjemiske strukturen til akteosid (ACT) (Tsumura Co., Ltd., Tokyo) er vist i fig. 1. Denne komponenten ble ekstrahert fra luftdelen av chyorogi (Stachys sieboldii MIQ). Renheten til ACT ble verifisert ved HPLC (kolonne: TSK gel ODS-80TM (4.0 id x 250 mm); Mobil fase: 20 prosent CH3CN/H2O, inneholdende 10 AcOH; Strømningshastighet: 0,7 ml/min. Temp.: romtemperatur; Deteksjon: UV 254 nm) ved Tsumura Co., Ltd. ACT brukt i disse eksperimentene hadde en renhet på over 9970. ACT ble oppløst i destillert vann. Dipyridamol (Dip) (Boehringer Ingelheim, Tyskland) og azatioprin (Aza) (Sigma, St. Louis, MO, USA) ble også brukt; Disse medikamentene ble suspendert i 1070 gummi arabicum.
Induksjon av halvmånetype anti-GBM nefritis
Crescentic-type anti-GBM nefritis ble indusert ved å immunisere rottene som hadde fått en nefritogen dose av kanin anti-rotte GBM (anti-GBM) serum med kanin r-globulin (rG) i henhold til en liten modifikasjon av den tidligere rapporterte metoden ( 12). I dette forsøket veide rottene ca. 160 g ble administrert 0,6 ml/dyr av anti-GBM-serum i halevenen.

Effekten av testmedikamenter ble estimert ved å administrere dem fra den første dagen etter anti-GBM-seruminjeksjonen (heterolog fase) eller den 20. dagen etter antiGBM-seruminjeksjonen (autologe faser). I forsøkene ble det samlet inn 24- timers urinprøver, og rottene ble deretter delt inn i 5 eller 6 grupper på 8 rotter slik at det gjennomsnittlige proteininnholdet i 24-t urinen i hver gruppe var på en tilsvarende nivå.
Evaluering av den antinefritiske effekten av testmedikamentene
I eksperimentet med medikamentell behandling fra den heterologe fasen ble fire grupper gitt oralt henholdsvis 3, 10 eller 30 mg/kg/dag ACT eller 100 mg/kg/dag Dip i et volum på 1 ml per 100 g. av kroppsvekt, daglig fra 1. dag eller dagen etter iv injeksjon av anti-GBM-serum til 40. dag. I eksperimentene med legemiddelbehandling fra den autologe fasen ble tre eller fire grupper gitt oralt 3, 10 eller 30 mg/kg dag med ACT (A) eller 30 mg/kg/dag med ACT, 100 mg/kg/dag av Dypp eller 50 mg/kg/dag av Aza (B), henholdsvis, i et volum på 1 ml per 100 g kroppsvekt, daglig fra den 20. dagen etter iv injeksjon av anti-GBM-serum til den 40. (A) eller 45. (B) dag. Den gjenværende gruppen ble gitt oralt vehikkelen (destillert vann) i stedet for testmedikamenter og fungerte som nefritisk kontroll. I tillegg ble en ubehandlet (normal) gruppe brukt for sammenligning med de nefritiske gruppene.
Urin- og blodansamlinger
{{0}} timers urinprøver ble tatt ved å holde hvert dyr i et individuelt metabolsk bur i 24 timer. Ved begynnelsen av urinoppsamlingen fikk hvert dyr 8 ml destillert vann oralt uten fôring. Urinen ble deretter sentrifugert ved 3,000 rpm i 15 minutter ved 41C og supernatanten ble brukt for å bestemme protein. På den siste dagen av eksperimentet ble 2,0 ml blod tappet fra nyrevenen til hver bedøvet rotte med en engangssprøyte og satt inn i et rør som inneholdt 0,125 ml heparin. Blodet ble sentrifugert ved 5,000 rpm for å oppnå plasma for bestemmelse av noen parametere.

Bestemmelser av urinprotein og plasmakolesterol og kreatinininnhold
Urinproteinutskillelsen ble bestemt ved metoden til Kingsbury et al. (13) og uttrykt som mg/24 timers urin. Kolesterolinnholdet ble bestemt med et kommersielt analysesett (Determine TC-5; Kyouwa Medix Co., Ltd, Tokyo) (14) og uttrykt som mg/dl plasma. Kreatinininnholdet ble bestemt ved å bruke et kreatininbestemmelsessett (CRE-EN; Kainos, Inc., Tokyo) og uttrykt som mg/dl plasma/100 g kroppsvekt.
Måling av plasmaantistofftiter mot -G
Plasmaantistofftiteren mot rG ble bestemt ved indirekte hemagglutinering ved bruk av sensibiliserte røde blodceller fra sau (15).
Måling av plasmakomplement CH50 nivå
Plasmakomplement CH50-nivået ble bestemt ved metoden til Mayer (16).
Vurdering av histopatologiske parametere
For den lysmikroskopiske studien ble nyrene isolert fra rotter bedøvet med pentobarbital, deretter dehydrert og fiksert ved å senke vevet trinnvis inn i ulike bekymringstradisjoner for etylalkohol fra lav til høy. Vevene ble deretter innebygd i parafin og seksjonert i 2 til 3 em-tykke skiver. I studiene av anti-GBM-nefritt av halvmånetype ble snittene farget med hematoksylin og eosin og Massons trikrom. Antall kjerner (hypercellularitet), halvmånedannelse, adhesjon av Bowmans kapsel til kapillærveggen (adhesjon) og fibrinoid nekrose i glomeruli ble observert under et lysmikroskop. For å vurdere disse parameterne ble et ekvatorialt tverrsnitt valgt ved tilfeldige prøvetakingsmetoder. Femti glomeruli/tverrsnitt ble observert, og fremkomsthastigheten av halvmånedannelse, adhesjon og fibrinoid nekrose ble uttrykt som prosentandeler av glomeruli (forekomst) som hadde disse morfologiske endringene som tidligere beskrevet (17). Evalueringen ble utført av en annen person som ikke visste identiteten til hver prøve. For å vurdere hypercellularitet ble et ekvatorialt tverrsnitt valgt ved en tilfeldig prøvetakingsmetode. Antall kjerner (inkludert kjerner av glomerulære celler og eksudative leukocytter) ble talt og uttrykt som gjennomsnittlig antall per glomerulært tverrsnitt i 10 glomeruli/seksjon.

Immunhistokjemi
I vev for immunoenzymatisk farging av rotte-IgG ble parafinsnittene kuttet som beskrevet ovenfor, og snittene ble behandlet med 0.1 prosent protease i 0.05 M Tris- HCl-buffer i 7 minutter og deretter vasket i avkjølt 0.01 M fosfatbufret saltvann (PBS), pH 7,4. Seksjonene ble deretter inkubert med anti-rotte IgG muse monoklonalt antistoff (mAb) (Cappel, West Clester, PA, USA) ved en fortynning på 1:100 i 90 minutter. Seksjonene ble vasket igjen med PBS, behandlet med 0,3 prosent hydrogenperoksid i metanol i 20 minutter for å blokkere endogen peroksidase, og inkubert med biotinylert affinitetsrenset anti-muse-IgG og avidinert pepperrotperoksidase med 3,3'-diaminobenzidintetrahydroklorid (DAB) (Vecta stain ABC Kit; Vector institution, Burlingame, CA, USA). Alle trinn ble utført ved romtemperatur.
Vev for immunoenzymatisk farging av prolifererende cellekjerneantigen (PCNA), som er en markør for celleproliferasjon, ble fiksert i 10 prosent formalin i PBS, og det parafininnstøpte vevet ble farget med samme prosedyre som for rotte-IgG unntatt for bruken av en mAb (19A2; Coulter Immunology, Hialeah, FL, USA) til PCNA.
Kvantifisering av rotte-IgG, C3 og PCNA på vevssnitt
Det totale arealet av immunreaktivt rotte-IgG og C3 i glomerulus ble målt i 30 glomeruli per seksjon ved bruk av en bildeanalysator (Toyobo Image analyzer V1; Toyobo Co., Ltd., Tokyo) og presentert som mm2/glomerulær tverrsnitt (GCS) ). PCNA-positive celler i glomerulus ble talt med bildeanalysatoren, og resultatene ble uttrykt som antall celler/GCS
statistiske analyser
Dataene representerer gjennomsnittet ± SD, og resultatene ble statistisk evaluert av ANOVA. Når disse resultatene var parametriske, ble disse statistisk evaluert ved Duncans test. Når resultatene var ikke-parametriske, ble de statistisk evaluert ved Kruskal-Wallis-testen. Den hemmende prosenten ble beregnet som følger:
Hemmende prosentandel ( prosent )=(Kontroll - Testmedikament) x 100 / (Kontroll - Normal)
RESULTATER
Effekt av akteosid i halvmånetype anti-GBM-nefritt
Urinproteinutskillelse (fig. 2 og 3): Når behandlingen med ACT ble startet fra dagen etter anti-GBM seruminjeksjonen (heterolog fase), ble den første signifikante suppresjonen på urinproteinet observert på 5. dag ved 30 mg /kg, po; på den 20. dagen ved 3 og 10 mg/kg, po; og på den 40. dagen med Dip ved 100 mg/kg, po
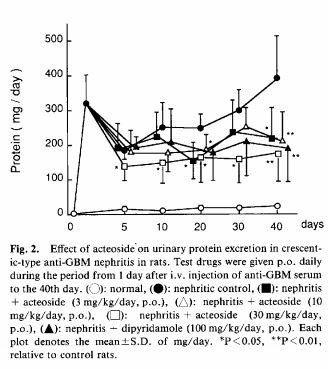
Når ACT ble gitt fra den 20. dagen etter antiGBM-seruminjeksjonen (autolog fase), hemmet ACT ved 10 og 30 mg/dag økningen av proteinutskillelsen i urinen innen den 30. dagen. På den annen side var Aza ved 50 mg/kg svakere enn ACT ved 30 mg/kg, men ikke signifikant, og Dip hadde ingen effekt.

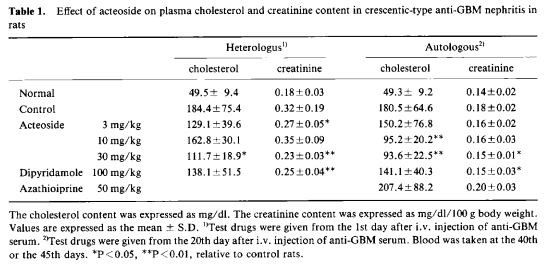
Plasmakolesterol og kreatinininnhold (tabell 1): Plasmakolesterol- og kreatinininnholdet ble bestemt på den 40. eller 45. dagen. Plasmakolesterolinnholdet i de nefritiske kontrollrottene var markert forhøyet. I kontrast ble økningen av kolesterolinnholdet redusert med ACT (30 mg/kg) fra den heterologe fasen med 60 prosent av kontrollnivået og med ACT (30 mg/kg) fra den autologe fasen med 62'o av kontrollen nivå. Kreatinininnholdet i plasma i de nefritiske rottene var også forhøyet. På den annen side, i ACT (30 mg/kg) fra begge fasebehandlede rotter, var plasmakreatinininnholdet likt det for normale rotter.
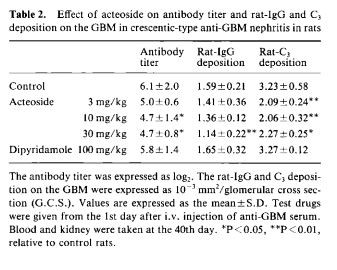
Plasmaantistofftiter mot rG: Nefritiske rotter hadde vist markert akselerert antistoffproduksjon. Den akselererte antistoffproduksjonen ble undertrykt til 72 prosent av kontrollnivået ved behandling med ACT (10 og 30 mg/kg) fra den heterologe fasen (tabell 2), ACT (30 mg/kg) fra den autologe fasen og Aza til 70 og 51 prosent av kontrollnivået, henholdsvis (data ikke vist), og det ble ikke påvirket av Dip.
Histologisk observasjon (tabell 3, fig. 4 og 5): Lysmikroskopisk undersøkelse av de nefritiske glomeruli avslørte lesjoner preget av alvorlig halvmånedannelse, adhesjon, fibrinoid nekrose og proliferasjon av mesangiale celler. Histologisk observasjon viste at ACT (fra både den heterologe og autologe fasen) hemmet hypercellularitet og forekomsten av halvmånedannelse, adhesjon og fibrinoidnekrose i glomeruli innen den 40. eller 45. dagen. Lesjonene til Dip- og Aza-behandlede nefritiske rotter var også mindre enn hos de nefritiske kontrollrottene. Imidlertid, når nefritiske rotter ble behandlet med Dip fra den autologe fasen, ble histologiske endringer lite påvirket av Dip (data ikke vist).



Glomerulær celleproliferasjon, nemlig økningen i PCNA-positive celler i glomeruli, ble observert inefritiske rotter. I kontrast, på den 30. dagen, en 52 prosent reduksjonsjon i celleproliferasjon ble observert, og dette var assosiert wmed en betydelig reduksjon i glomerulære cellerlularitet sammenlignet med kontrollen (tabell 3).
Avsetning av immunreaktant (tabell 2 og fig. 6): Det var mulig å observere rotte-IgG- og C3-avsetninger på GBM i de nefritiske kontrollrottene; de ble imidlertid ikke funnet hos normale rotter. ACT (30 mg/kg) fra den heterologe fasen reduserte rotte-IgG-avsetning på GBM med 72 prosent av kontrollnivået. Dessuten reduserte ACT (3, 10 og 30 mg/kg) fra den heterologe fasen rotte-C3-avsetning på GBM med 60 til 69 prosent innen den 40. dagen. Selv når ACT ble gitt fra den autologe fasen, var hemming av rotte-IgG og C3-avsetning lik resultatene ovenfor. Nedfallet påvirket ikke rotte-IgG og C3-avsetning. Aza reduserte imidlertid rotte-IgG- og C3-avsetning på GBM med henholdsvis 67 og 68 prosent (data ikke vist).

Effekt av ACT på komplementaktivitet og C3-avsetninger på GBM ved anti-GBM-nefritt av originaltype (fig. 7)

Anti-GBM-nefritt av original type ble indusert hos rotter ved injeksjon av 0,6 ml anti-GBM-serum i halevenene deres, som beskrevet tidligere (18). Nefritiske rotter ble forbehandlet og etterbehandlet med ACT ved 30 mg/kg, po og kobragiftfaktor (CVF) (Sigma) ved 10 fig/rotte, ip, tre ganger, hver 8. time. ACT- og CVF-behandlinger reduserte proteinutskillelsen i urinen med en hemmende prosentandel på ca. henholdsvis 35 grader og 71 prosent. CH50 i nefritt kontrollrotter var markant lavere enn hos normale rotter 24 timer etter induksjon av nefritt. ACT hemmet den reduserte CH50 og økte C3-avsetningen på GBM hos nefritiske kontrollrotter. CVF opphevet CH50- og C3-avsetningen. Videre, i in vitro-eksperimentet, hemmet ACT komplementaktiveringen med 37 prosent. Når ACT ble administrert til normale rotter, reduserte ACT komplementaktiveringen i ex vivo-eksperimentet (data ikke vist).
DISKUSJON
Raskt progredierende glomerulonefritt og nyresykdommer ved Goodpastures syndrom er ondartede sykdommer som går over i nyresvikt 2 eller 3 måneder etter utviklingen av sykdommen (19). Kjennetegn på denne nefritten involverte hypercellularitet, markert infiltrasjon av nøytrofiler og monocytter, og halvmånedannelse i glomeruli. Cocktailterapi med immunsuppressive midler, blodplatehemmende medisiner og steroider har hovedsakelig blitt brukt på denne sykdommen. På den annen side, selv om CyA er et overlegent immundempende middel som har en gunstig effekt på eksperimentell nefritt (6, 8), er det rapportert at CyA forårsaker nyredysfunksjon og forårsaker irreversibel histologisk endring i glomeruli (11). Metylprednisolon har mange bivirkninger. Videre er rebound-fenomenet og abstinenssyndromet etter langvarig behandling med denne medisinen to av problemene. Derfor må det utvikles et nytt immundempende middel for behandling av nefritt som har færre bivirkninger.
Crescentic-type anti-GBM nefritis er en eksperimentell modell som viser histologiske og patologiske endringer som ligner på de ved raskt progressiv glomerulonefritt og nyresykdom ved Goodpastures syndrom (20). Utviklingen og progresjonen av denne nefritten består av 2 faser som er mediert av immunresponser. Den tidlige reaksjonen, den såkalte heterologe fasen, skyldes avsetning av anti-GBM-antistoff, etterfulgt av komplementavhengig akkumulering av polymorfonukleære granulocytter (21, 22). Den sene fasen (autolog fase) utvikles ved binding av autologe antistoffer avsatt langs GBM og tilstrømning av monocytter/makrofager til glomeruli etter denne reaksjonen (22, 23). Denne nefritten er preget av bifasisk urinprotein og hypercellularitet som involverer halvmånedannelse og fibrinoid nekrose. Halvmåneformasjonen antas å være mediert av migrerte makrofager og prolifererte epitelceller (22, 24).
Vi har tidligere rapportert at mizoribin og Aza, et immunsuppressivt middel (7), hemmet økningen av plasmaantistoff mot kanin-IgG og Pachyman, hovedkomponenten i Poria cocos (18), reduserte graden av C3-avsetning på GBM, og begge var markert effektiv mot anti-GBM nefritt.
ACT-behandlinger undertrykte utviklingen av anti-GBM glomerulonefritt, vurdert ved reduksjon av proteinuri og plasmakolesterol, forebygging av nedsatt nyrefunksjon og forebygging av progressive histologiske endringer inkludert utvikling av glomerulære halvmåner og hypercellularitet. På den 40. dagen reduserte ACT ved 30 mg/kg alene signifikant mengden av rotte-IgG-avsetning på GBM mediert av undertrykkelse av antikroppsproduksjon i denne nefritiske modellen. På den annen side ble mengden C3-avsetninger på GBM redusert med ACT ved 3, 10 eller 30 mg/kg. Dessuten hemmet ACT betydelig komplementaktivering i både in vitro og ex vivo eksperimenter. Reduksjonen av CH50 hos nefritiske kontrollrotter ble hemmet av ACT. Dataene ovenfor antyder at ACT hemmer nyreskade ved å undertrykke komplementaktivering, fordi komplementmembranangrepskompleks (MAC) er involvert i patogenesen av glomerulær skade (25), og den sublytiske MAC har potensielle inflammatoriske mediatorer som kan være assosiert med glomerulær skade, mesangial celleproliferasjon og ekstracellulære matriksdiffusjoner, slik som reaktive oksygenarter (26), protease (27), prostaglandiner (28) og interleukin-1 som cytokiner (29), samt kollagen (30).
Det antas at komplementaktivering er nært knyttet til leukocyttinfiltrasjon. I nyere studier ble det rapportert at C5a provoserte monocytt- og nøytrofiladhesjon til henholdsvis mesangiale celler og endotelceller (31, 32). Derfor skal vi i en videre studie undersøke effekten av ACT på akkumulering av leukocytter i glomeruli.
REFERANSER
1 Yamahara J, Kitani T, Kobayashi H og Kawahara Y: Studies on Stachys sieboldii MIQ. II Anti-anoksi-virkning og de aktive bestanddelene. Yakugaku Zasshi 110, 932-935 (1990) (Abstrin engelsk)
2 Takeda Y, Fujita T, Satoh T og Kakegawa H: På de glykosidiske bestanddelene av Stachys sieboldii MIQ. og deres effekter på hyaluronidaseaktivitet. Yakugaku Zasshi 105, 955-959 (1985) (Abstr på engelsk)
3 Sasaki H, Nishimura H og Morita T: Immunsuppressive prinsipper for Rehmannia-fåter var. hueichingensis. Planta Med 55, 458-462 (1989)
4 Saito T og Atkins RC: Bidrag av mononukleære leukocytter til progresjonen av eksperimentell fokal glomerulær sklerose. Kidney Int 37, 1076-1083 (1990)
5 Tipping PG, Neale TJ og Holdsworth SR: T-lymfocyttdeltakelse i antistoffindusert eksperimentell glomerulonefritt. Kidney Int 27, 530-537 (1985)
6 Neild GH, Ivory K og Williams DG: Cyclosporin A hemmer sactus serumsyke hos kaniner. Clin Exp Immunol 52, 586-594 (1983)
7 Okamoto K, Ito M og Suzuki Y: Studier av antinefritisk effekt på mizoribin (p-INN, Bredinin®), et nytt immunsuppressivt middel, og azatioprin (2): Effekt på halvmånetype anti-GBM-nefritt hos rotter. Jpn J Pharmacol 34, 33-41 (1984)
8 Nagamatsu T, Kojima N, Kondo N, Hattori T, Kojima R, Ito M og Suzuki Y: Undertrykkelse av cyklosporin A av anti-GBM-nefritt hos rotter. Jpn J Pharmacol 58, 27-36 (1992)
9 Taniguchi H, Nagamatsu T, Kojima R, Ito M og Suzuki Y: Markert antinefritisk virkning og mindre uønskede effekter av metylprednisolonsultanat ved intermitterende administrering hos rotter. Jpn J Pharmacol 64, 79-88 (1994)
10 Hattori T, Furuta K, Hayashi K, Nagamatsu T, Ito N og Suzuki Y: Studier av antinefritiske effekter av plantekomponenter (6): Antinefritiske effekter og mekanismer av phellogen drine (OB-5) på halvmåne- type anti-GBM nefritt hos rotter (2). Jpn J Pharmacol 60, 187-195 (1992)
11 Mason J: Effektene av Sandimmune på nyrene. Clin Res Bull 6, 47-51 (1989)
12 Ito M, Yamada H, Okamoto Y og Suzuki Y: Crescentic-type nefritt indusert av anti-glomerulær basalmembran (GBM) serum hos rotter. Jpn J Pharmacol 33, 1145-1154 (1983)
13 Kingsbury FB, Clark CP, Williams G og Post AL: Den raske bestemmelsen av albumin i urinen. J Lab Clin Med 11, 981-989 (1926)
14 Zurkowski P: En rask metode for kolesterolbestemmelse med en enkelt reagens. Clin Chem 10, 451-453 (1964)
15 Mcleish KR, Clark CP, Williams G og Post AL: Undertrykkelse av antistoffsyntese av prostaglandin E som en mekanisme for å forhindre murin immunkompleks glomerulonefritt. Lab Invest 47, 147-152 (1982)
16 Mayer MM: Komplement- og komplementfiksering. I Experimental Immunochemistry, s 133-240, Charles C. Thomas, Springfield (1961)
17 Hattori T, Ito M, Nagamatsu T og Suzuki Y: Studier av den antinefritiske effekten av TJ-8014, en ny japansk urtemedisin (3): Effekter på halvmånetype anti-GBM-nefritt hos rotter. Jpn J Pharmacol 52, 131-140 (1990)
18 Hattori T, Hayashi K, Nagao T, Furuta K, Ito M og Suzuki Y: Studier av antinefritiske effekter av plantekomponenter (3): Effekt av pachyman, hovedkomponenten av Poria cocos Wolf på opprinnelse nal-type anti-GBM nefritt hos rotter og dens mekanismer. JpnJ Pharmacol 59, 89-96 (1992)
19 Shibata S, Miyakawa Y, Naruse T, Nagasawa T og Takuma T: Et glykoprotein som induserer nefrotoksisk antistoff: Dets isolasjon og rensing fra rotte glomerulær basalmembran. J Immunol 102, 593 601 (1969)
20 Falk RJ: ANCA-assosiert nyresykdom. Kidney Int 38, 998-1010 (1990) 21 Mulligan MS, Johnson KJ, Todd RF III, Issekutz TB, Miyasaka M, Tamatani T, Smith CW, Anderson DC og Ward PA: Requirements for leukocyte adhesion molecules in nephrotoxic nephritis. J Clin Invest 91, 577-587 (1993)
22 Nahas AME: Vekstfaktorer og glomerulær sklerose. Kidney Int 41, Supp 36, S15-S20 (1992)
23 Boyce NW, Holdsworth SR, Dijkstra CD og Atkins RC: Kvantifisering av intraglomerulære mononukleære fagocytter i eksperimentell glomerulonefritt hos rotter ved bruk av spesifikke monoklonale antistoffer. Pathology 19, 290-293 (1987)
24 Becker GJ, Hancock WW, Stow JL, Glasgow EF, Atkins RC og Thomson NM: Involvering av makrofager i eksperimentell kronisk immunkompleks glomerulonefritt. Nephron 32, 227-233 (1982) 25 Perkinson DT, Baker PT, Couser WG, Johnson BJ og Adler S: Membrane attack complex deposition in experimental glomerular injury. Am J Pathol 120, 121-128 (1985)
26 Alder S, Baker PJ, Johnson RJ, Ochi RF, Pritzl P og Couser WG: Komplementmembranangrepskompleks stimulerer produksjonen av reaktive oksygenmetabolitter av mesangiale celler fra dyrkede rotter. J Clin Invest 77, 762-767 (1986)
27 Johnson RJ, Couser WG og Alpers CE: Den humane nøytrofilistinproteasen, esterase og cathepsin G kan mediere glomerulær skade in vivo. J Exp Med 168, 1169-1174 (1988)
28 Cybusky AV, Lieberthal W, Quigg RJ, Rennke HG og Salant DJ: En rolle for tromboksan i komplementmediert glomerulær skade. Am J Pathol 128, 45-51 (1987)
29 Lovett D, Hansch G, Resch K og Gemsa D: Aktivering av glomerulære mesangiale celler av terminale komplementkomponenter. Stimulering av frigjøring av prostanoid og interleukin-l-lignende faktor. Immunobiology 168, 34-35 (1986)
30 Torbohm I, Schonermark M, Wingen AM, Berger B, Rother K og Hansch GM: C5b_8 og C5b_9 modulerer kollagenfrigjøringen av humane glomerulære epitelceller. Kidney Int 37, 1098-1104 (1990)
31 Lo SK, Detmers PA, Levin SM og Wrigh SD: Forbigående adhesjon av nøytrofiler til endotelet. J Exp Med 169, 1779 -1793 (1989) 32 Brady HR, Denton MD, Jimenez W, Takata S, Palliser D og Brenner BM: Chemoattractants provoserer monocyttadhesjon til humane mesangiale celler og mesangial celleskade. Kidney Int 42, 480-487 (1992)






