Itopride øker effektiviteten av behandlingen av opioidindusert forstoppelse hos palliative pasienter: En observasjonsstudie uten intervensjonⅠ
Oct 31, 2023
Introduksjon: Det anbefales på det sterkeste at avføringsmidler rutinemessig foreskrives for forebygging av opioid-indusert obstipasjon (OIC). Beviset som støtter effektiviteten av prokinetikk for denne indikasjonen er sparsomt. Denne studien tar sikte på å verifisere om itoprid, lagt til forebyggende OIC-terapi, øker effektiviteten av forebygging av opioid-indusert forstoppelse hos voksne palliative pasienter.
Materiale og metoder: I en spørreskjemabasert observasjonsstudie fikk alle pasienter vanlige avføringsmidler pluss ett av følgende: oksykodon/nalokson (OXN); itoprid (ITP); eller oksykodon/nalokson + itoprid (OXN +ITP). Det primære målet var reduksjonen i nødvendigheten av bruk av avføringsmiddel på en 0-4 skala vurdert etter 7 dagers behandling.

Klikk til naturlige rettsmidler mot forstoppelse
Resultater: 92 pasienter oppfylte inklusjonskriteriene i de fire gruppene: OXN (n=12), ITP (11), OXN + ITP (9) og kontrollgruppen (kun avføringsmidler ved behov) (60). Nødvendigheten av avføringsmidler ble redusert i grupper der itoprid ble brukt, med en statistisk signifikant forskjell i forhold til kontroll, oksykodon/nalokson (p=0.009), eller i kombinasjon. OXN reduserte ikke bruk av avføringsmiddel (p=0.22).
Konklusjon: Alle intervensjoner virket like effektive i forebygging av OIC. Tilsetning av itoprid, men ikke oksykodon/nalokson, resulterte imidlertid i en reduksjon i nødvendigheten av bruk av avføringsmiddel hos OIC-pasienter, og det ser ut til å være verdifullt i denne ofte refraktære tilstanden. Randomiserte, kontrollerte studier vil være verdifulle for å oppnå bevis av god kvalitet uten systematisk skjevhet.
Introduaksjon
Opioidanalgetika er nøkkelelementet i smertebehandling hos kreftpasienter [1–3]. Men selv noen få dager med opioidbehandling kan føre til alvorlig tarmdysfunksjon. Opioid-indusert obstipasjon (OIC) rammer 42,4 % av onkologiske pasienter i sluttstadiet og er et av de hyppigste symptomene foruten smerte og kakeksi hos disse pasientene [4]. OIC er definert i Roma IV Diagnostic Criteria som nye eller forverrede symptomer på konfastsettelse ved oppstart, endring eller økning av opioidterapi, som må inkludere to eller flere av symptomene som definerer funksjonell obstipasjon.
Kriteriene må være oppfylt de siste 3 månedene med symptomdebut minst 6 måneder før diagnose [5, 6]. En så lang observasjonsperiode er imidlertid ikke mulig hos de fleste palliative pasienter fordi overlevelsen i mange tilfeller er mye kortere. Det er grunnen til at Polish Society of PalliativeMedicine anbefaler 7 dagers observasjon som er tilstrekkelig for den riktige kliniske beslutningen om avføringsbehandling, som i valideringsprosessen ble bevist å være en effektiv tilnærming [7]. Forstoppelse er en plagsom bivirkning av opioider fordi den ikke opphører , men øker med økt varighet av opioidbehandling.
OIC er vanskelig å håndtere, og effektiviteten til vanlige avføringsmidler er dårlig [2, 3, 8]. I 85–95 % av tilfellene reduserer forstoppelse helserelatert livskvalitet, selv om to tredjedeler er av mild og moderat intensitet [9]. Forstoppelse genererer også en ekstra økonomisk byrde for helsesystemet [10]. Dårlig respons på OIC er en betydelig barriere for effektiv smertebehandling. Hver tiende pasient trenger bytte av smertestillende middel, og halvparten av pasientene med obstipasjon får suboptimal analgesi på grunn av gastrointestinale bivirkninger [11]. Opioidbehandlede pasienter er mer sannsynlig å bruke behandling for obstipasjon sammenlignet med de som ikke får opioider [12].

Det anbefales sterkt, både av European Association for Palliative Care og EuropeanSociety for Medical Oncology, at avføringsmidler for behandling eller profylakse av opioidindusert forstoppelse rutinemessig foreskrives [2, 13]. Intensiteten av forebyggende avføringsmiddel bør ta sikte på å nå minst tre avføringer per uke og kontrollere intensiteten av subjektive symptomer [7].
En alternativ forebyggingsmetode kan være bruk av opioidantagonister som depotnalokson kombinert med oksykodon [14]. Svært lavkvalitets bevis tyder på at naloksoninkombinasjon med oksykodon reduserer risikoen for forstoppelse uten økt smerte sammenlignet med oksykodon alene hos voksne med maligniteter og opioid-indusert forstoppelse [15].
Alle opioider induserer forstoppelse, men i forskjellig grad. Høye doser tramadol er mindre forstoppende enn små doser morfin [16,17]. Hyppigheten av forstoppelse etter oksykodone eller morfin er lik [18]. Parenterale opioider svekker intestinal peristaltikk mindre enn orale [19]. Transdermal fentanyl og buprenorfin induserer tarmdysfunksjon sjeldnere, selv om det er deres hyppigste bivirkning [20–22].
Imidlertid skilte transdermale opioider seg ikke fra orale opioider i frekvensen av obstipasjon i større observasjonskohortstudier [23, 24]. Tarmdysfunksjon skyldes både den sentrale og perifere virkningen av opioider.Sentralmekanismen består av aktivering av nevroner i ryggmargen, noe som fører til langsommere tarmpassasje og redusert sekret.
Imidlertid er OIC hovedsakelig indusert av aktivering av lokale μ-opioidreseptorer i tarmen, som er tilstede i magen, tynntarmen og tykktarmen, hovedsakelig i myenteric og submucosal plexus, og på immunceller i lamina propria [25]. Påvirkningen av opioider summerer til syvende og sist opp til tre gastrointestinale effekter: en reduksjon i utskillelsen av væske, depresjon av peristaltiske sammentrekninger og fremme av ikke-fremdrivende motilitetsmønstre, og spasme i alle lukkemusklene [26]. Dehydrering av tarminnholdet fører til forekomsten av fecalstones, som er vanskelige å avføre gjennom den forspente analsfinkteren. Tarmen blir overbelastet og forlenget av disse harde avføringsmassene [25, 26].
Dette forklarer hvorfor bulkavføringsmidler er ineffektive [13]. På den annen side anbefales osmotiske og stimulerende avføringsmidler i OIC. Effektiviteten deres er imidlertid dårlig fordi de ikke adresserer teopioidreseptor-mediert mekanisme for tarmdysfunksjon, så et betydelig antall pasienter oppnår ikke tilstrekkelig lindring av symptomene [27]. Bortsett fra dette kan langvarig bruk av avføringsmiddel være assosiert med skade på muskelfunksjon i tarmen; ernæringsmessige underskudd i form av tap av vann, vitaminer og mineraler; og nyrestein eller nyresvikt, i tillegg til å modifisere effekten av andre legemidler [28].
Så en alternativ eller tilleggsmetode kan være å legge til prokinetikk, som kan øke effektiviteten til avføringsmidler eller opioidantagonister. Det kliniske beviset for denne effekten er imidlertid sparsomt, bortsett fra 5-HT4-reseptoragonistprucaloprid [29]. Metoklopramid virker ikke på tarmen, og bør derfor ikke betraktes som forstoppelse. Itopride er en dopamin D2-antagonist med acetylkolinesterasehemmende virkning.

Det har en stimulerende virkning på tykktarmsperistaltikk, og driver kolonluminalt innhold, forskjellig fra cisaprid og mosaprid, og derfor kan det være et nyttig medikament for behandling av funksjonell obstipasjon [30]. Polske retningslinjer foreslår å bruke prokinetikk, som itoprid, for behandling av forstoppelse [14]. Derfor bruker noen spesialister i palliativ behandling det off-label, ikke bare for dyspepsi, men også for behandling av forstoppelse.Denne studien hadde som mål å verifisere om itoprid er effektivt i behandlingen av opioid-indusert forstoppelse hos voksne palliative pasienter i klinisk setting.
De primære resultatene var:
• gjennomsnittlig endring i nødvendigheten av avføringsmiddel på en 0–4-skala vurdert etter 7 dager medbehandling; et negativt tall betyr en nedgang,
• gjennomsnittlig antall avføringer, • gjennomsnittlig intensitet av tarmsymptomer,
• the frequency [%] of constipation, defined as at least one of the following: – the last defecation > 2 days, – the number of days with defecation < 4, – any subjective bowel symptom with intensity >2 i en 0–4 skala (som nedenfor på s. 4 c–h).
De sekundære resultatene var:
• hyppigheten (%) av pasientene med tarmbevegelser kun etter klyster (eller manuell avføringsvakuering) etter 7 dagers behandling,
• uheldige effekter.
Materialer og metoder
Denne åpne observasjonsstudien ble utført på voksne palliative pasienter med forstoppelse, som fikk sterke opioider og ikke hadde blitt behandlet med itoprid før observasjonen. Alle pasienter fikk vanlige avføringsmidler, og i tillegg oksykodon/nalokson (OXN-gruppe), oritopride (ITP-gruppe) eller oksykodon/nalokson + itoprid (OXN + ITP-gruppe).
Kontrollgruppen (CTRL) brukte kun avføringsmidler om nødvendig. Inklusjonskriteriene var: leselig og fullstendig dokumentasjon, alder over eller lik 18 år, hjemmehospice eller poliklinikk for palliativ behandling, minst to besøk utført i 7.–8. dagsintervaller (dag 0 og dag 7), sterke opioider brukt 7 dager før dag 0 til dag 7, ingen itoprid brukt opp til dag 0.
Strukturert spørreskjema
Palliative behandlere brukte et spørreskjema for å rapportere data samlet inn i deres medisinske dokumentasjon. Spørreskjemaet inneholdt følgende elementer:
1) Dato.
2) Sted (hjem, ambulant, palliativ avdeling på sykehus, hospits).
3) ECOG-ytelsesstatus, vurdert av en lege.
4) Tarmsymptomer de siste 7 dagene, vurdert av pasienten:
a) siste avføring [dager],
b) antall dager med avføring[dager],
c) vanskeligheten med avføring på en skala fra {{0}}–4, der 0 – ingen problemer («normal avføring»), 1 – mild («ganske normal»), 2 – moderat, 3 – signifikant /ofte, 4 – ekstreme vanskeligheter/alltid,
d) for lite avføring på en {{0}}-4 skala, der 0 – normal avføring, 1 – fra tid til annen (mild intensitet), 2 – ganske ofte (moderat intensitet),3 – veldig ofte , 4 – alltid,
e) avføring for hard på en skala fra 0–4 (se ovenfor),
f) følelsen av ufullstendig avføring på en {{0}}-4 skala, der 0 – ingen symptom, 1 – mild intensitet/noen ganger, 2 – moderat intensitet/ganske ofte, 3 – signifikant intensitet/svært ofte , 4 – ekstrem intensitet/alltid,
g) anstrengelse eller klem for å prøve å passere tarmbevegelser, på en 0–4 skala (se ovenfor),
h) nødvendigheten av bruk av avføringsmidler på en {{0}}-4 skala, hvor 0 – ingen avføringsmidler brukt, 1 – fra tid til annen (noen ganger), 2 – ofte brukt,3 – tarmbevegelser først etter bruk av vanlige avføringsmidler, 4 – tarmbevegelser kun etter et klyster eller manuell avføringsevakuering.
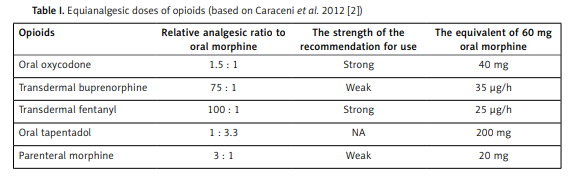
5) De daglige dosene av opioider er omregnet til teoral morfinekvivalent (tabell I).
6) Itopride brukte 50 mg tid (ja/nei).
7) Bivirkninger.
Alle utøverne hadde deltatt på et fordypningskurs om symptomkontroll før datainnsamling. De var klar over de polske retningslinjene for forebygging og behandling av forstoppelse hos palliative pasienter. Målet med avføringsmiddelbehandling, i henhold til disse retningslinjene, var å sikre tarmbevegelser hos pasienter som tok opioider minst tre ganger i uken (helst annenhver dag) [14].
Kilde til data
Dataene ble samlet inn i 2018 av 16 palliative behandlere i 10 (hjemme-, sengeliggende og ambulerende) palliative sentre for voksne pasienteri Polen. Studien fikk godkjenning fra den bioetiske komiteen. Størrelsen på undergruppene var et av resultatene og skulle ikke estimeres ved bruk av statistiske metoder. Vi antok at minimum 100 innsamlede spørreskjemaer skulle være tilfredsstillende for å verifisere forskrivningsatferden angående forebygging av forstoppelse.
Statistisk analyse
Kruskal-Wallis og Mann-Whitney U-tester ble brukt for statistisk analyse av ikke-parametriske data. Frekvensanalyse ble utført ved å bruke c2 og Fishers eksakte tester på riktig måte. P-verdier mindre enn 0.05 ble ansett som statistisk signifikante. Dataene ble analysert ved bruk av Statistica 13 (StatSoft).
Naturlig urtemedisin for å lindre forstoppelse-Cistanche
Cistanche er en slekt av parasittiske planter som tilhører familien Orobanchaceae. Disse plantene er kjent for sine medisinske egenskaper og har blitt brukt i tradisjonell kinesisk medisin (TCM) i århundrer. Cistanche-arter finnes hovedsakelig i tørre og ørkenområder i Kina, Mongolia og andre deler av Sentral-Asia. Cistanche-planter er preget av deres kjøttfulle, gulaktige stilker og er høyt verdsatt for deres potensielle helsemessige fordeler. I TCM antas Cistanche å ha styrkende egenskaper og brukes ofte til å gi næring til nyrene, øke vitaliteten og støtte seksuell funksjon. Det brukes også til å løse problemer knyttet til aldring, tretthet og generell velvære. Mens Cistanche har en lang historie med bruk i tradisjonell medisin, er vitenskapelig forskning på dens effekt og sikkerhet pågående og begrenset. Imidlertid er det kjent for å inneholde forskjellige bioaktive forbindelser som fenyletanoidglykosider, iridoider, lignaner og polysakkarider, som kan bidra til dens medisinske effekter.

Wecistanche sincistanche pulver, cistanche tabletter, cistanche kapsler, og andre produkter er utviklet ved hjelp avørkencistanchesom råvarer, som alle har god effekt på å lindre forstoppelse. Den spesifikke mekanismen er som følger: Cistanche antas å ha potensielle fordeler for å lindre forstoppelse basert på tradisjonell bruk og visse forbindelser den inneholder. Mens vitenskapelig forskning spesifikt på Cistanches effekt på forstoppelse er begrenset, antas det å ha flere mekanismer som kan bidra til potensialet til å lindre forstoppelse. Avføringseffekt:Cistanchehar lenge vært brukt i tradisjonell kinesisk medisin som et middel mot forstoppelse. Det antas å ha en mild avføringseffekt, som kan bidra til å fremme avføring og indusere forstoppelse. Denne effekten kan tilskrives forskjellige forbindelser som finnes i Cistanche, for eksempel fenyletanoidglykosider og polysakkarider. Fukting av tarmene: Basert på tradisjonell bruk anses Cistanche å ha fuktighetsgivende egenskaper, spesielt rettet mot tarmen. Å fremme hydrering og smøring av tarmene kan bidra til å myke verktøy og lette passasjen, og dermed lindre forstoppelse. Anti-inflammatorisk effekt: Forstoppelse kan noen ganger være assosiert med betennelse i fordøyelseskanalen. Cistanche inneholder visse forbindelser, inkludert fenyletanoidglykosider og lignaner, som antas å ha anti-inflammatoriske egenskaper. Ved å redusere betennelse i tarmen, kan det bidra til å forbedre regelmessig tarmbevegelse og lindre forstoppelse.
