Del Ⅰ Rollene til mitokondriell DNA-skade i nyresykdommer: En ny biomarkør
Jun 12, 2023
Abstrakt
Nyren er et mitokondrierrikt organ, og nyresykdommer er anerkjent som mitokondrierelaterte patologier. Intakt mitokondrielt DNA (mtDNA) opprettholder normal mitokondriell funksjon. Mitokondriell dysfunksjon forårsaket av mtDNA-skade, inkludert nedsatt mtDNA-replikasjon, mtDNA-mutasjon, mtDNA-lekkasje og mtDNA-metylering, er involvert i utviklingen av nyresykdommer. Her gjennomgår vi rollene til mtDNA-skade i ulike settinger av nyresykdommer, inkludert akutt nyreskade (AKI) og kronisk nyresykdom (CKD). Ved en rekke nyresykdommer er mtDNA-skade nært forbundet med tap av nyrefunksjon. Nivået av mtDNA i perifert serum og urin gjenspeiler også status for nyreskade. Å lindre mtDNA-skader kan fremme gjenoppretting av mitokondriell funksjon ved eksogen medikamentell behandling og dermed redusere nyreskade. Kort sagt konkluderer vi med at mtDNA-skade kan tjene som en ny biomarkør for å vurdere nyreskade i ulike årsaker til nyresvikt, noe som gir et nytt teoretisk grunnlag for mtDNA-målrettet intervensjon som et terapeutisk alternativ for nyresykdommer.
Nøkkelord
mitokondrielt DNA; nyresykdommer; mtDNA-replikasjon; mtDNA-mutasjon; mtDNA-lekkasje; mtDNA-metylering.

Klikk her for å få fordelene med Cistanche
Introduksjon
Nyren fjerner metabolske avfallsprodukter gjennom den glomerulære filtrasjonsbarrieren og opprettholder vann-elektrolyttbalansen via renal tubulær reabsorpsjon. Som et organ med høyt energibehov har nyrene rikelig med mitokondrier for å generere ATP for å opprettholde sin indre homeostase. Et økende antall studier har avdekket at mitokondriell dysfunksjon spiller en viktig rolle i forekomsten og progresjonen av nyresykdommer, inkludert akutt nyreskade (AKI) og kronisk nyresykdom (CKD) [1,2]. Mekanismen for mitokondriell dysfunksjon forblir imidlertid udefinert.
Mitokondrielt DNA (mtDNA) er et dobbelttrådet sirkulært DNA som er uavhengig av kjernefysisk DNA. Normalt er mtDNA med en lengde på 16 596 basepar lokalisert i mitokondriematrisen. mtDNA har sitt eget transkripsjons- og translasjonssystem og koder for 2 rRNA, 22 tRNA og 13 polypeptider. Disse polypeptidene inkluderer ND1-6, ND4L, COXI-III, cyt-b, ATPase6 og ATPase8, som er involvert i sammensetningen av mitokondrielle respiratoriske komplekser for å opprettholde integriteten til elektrontransportkjeden (ETC) og stabilitet av oksidativ fosforylering (OXPHOS) [3]. Funksjonen til OXPHOS gir den fysiologisk nødvendige energien til celler og organer, og ETC er hovedkilden til produksjon av reaktive oksygenarter (ROS). mtDNA-skade fører til ineffektiv mitokondriell funksjon, slik som ROS-overproduksjon, redusert ATP-generering og endrede metabolittprofiler [4]. Skadet mtDNA ble ledsaget av oksidativt stressaktivering og redusert mitokondriell masse [5]. Viktigere er at mtDNA-integritet er nært knyttet til mitokondriell funksjon. I tillegg til å bestemme mitokondriell funksjon direkte, kan mtDNA også fungere som en endogen patogen faktor. Merkelig nok har de siste studiene rapportert at mtDNA som lekker inn i cytoplasmaet kan fungere som en inflammatorisk mediator og aktivere den naturlige inflammatoriske immunresponsen [6,7].
Prosessen med DNA-transkripsjon og replikasjon er ofte ledsaget av mutasjoner, slettinger, innsettinger, translokasjoner og trådbrudd. Disse skadene kan raskt avsløres av det nukleære DNA-reparasjonssystemet for å fremme genomisk integritet (8]. Ho
wevermtDNA mangler moden skadefølende signalering og beskyttende histoner. Overdreven ROS-produksjon medierer oksidativ stressskade i celler og kan også forverre mtDNA-mutasjoner, trådbrudd og slettinger, og skaper en ond sirkel av mtDNA-skader (9]Derfor er den mer følsom for å bli svekket av interne og eksterne ugunstige faktorer.
Rollene til mtDNA-skade i flere sykdommer, som kreft, kardiovaskulære sykdommer, leversykdommer og nevrologiske sykdommer, har tiltrukket seg mye oppmerksomhet (10-13Tilsvarende har det blitt rapportert at mtDNA-skade, inkludert svekket mtDNA-replikasjonmtDNA-mutasjoner, mtDNA lekkasje, og mtDNA-modifikasjon, spiller en viktig rolle i utviklingen av nyresykdommer (Figur 1.) I denne gjennomgangen oppsummerer vi rollene til mtDNA-skade i nyresykdommer og fremhever den potensielle verdien for diagnostiske og terapeutiske mål.

Figur 1. Vanlige typer mtDNA-skader. mtDNA-skade inkluderer svekket mtDNA-replikasjon, mtDNA-mutasjoner, mtDNA-lekkasje og mtDNA-metylering. mtDNA-replikasjon fungerer på en semi-konservert måte og inneholder flere enzymer, som TWINKLE, Poly y, POLRMT ogmtSSB, som kan hindre mtDNA-replikasjon når de blir forstyrret. De vanlige typene mtDNA-mutasjoner inkluderer substitusjon, translokasjon, innsetting og sletting. Lekket mtDNA kan overføres til perifert plasma og urin via henholdsvis sirkulasjons- og urinsystemet under påvirkning av DNMls, metyldonorforbindelsene avledet fra SAM overføres til CpGislands for å danne 5'-metylcytosin. (OriH, opprinnelsen til replikasjon av tungtråd; OriL, opprinnelsen til replikering av letttråd; Poly, polymerase gamma; POLRMT, mitokondriell RNA-polymerase; mtSSBmitokondrielt enkeltstrengs bindende protein; SAM, S-adenosyl-L-metionin; SAH, S-adenosyl-L.homocystein; SAMC, S-adenosylmetioninbærer; DNMT-er og DNA-metyltransferaser).

Cistanche ekstrakt
Vanlige typer mtDNA-skader
1. Nedsatt mtDNA-replikasjon
Stabiliteten til mtDNA er avgjørende for å opprettholde den sunne funksjonen til mitokondrier i cellene. mtDNA-replikasjon og distribusjon i mitokondrielle nettverk spiller en viktig rolle i å opprettholde mitokondriell homeostase. I likhet med nukleær DNA-replikasjon, fungerer mtDNA-replikasjon på en semi-konservert måte og innebærer flere typer mekanismer, inkludert trådforskyvning og trådkoblede modeller [14]. I hver cellesyklus replikerer mtDNA flere ganger, og replikasjonen av begge trådene, den tunge tråden og den lette tråden, er ikke synkronisert. mtDNA-replikasjon er nært knyttet til mitokondriell metabolisme, og aktiviteten kan påvirkes av endringer i spesifikke mitokondrielle metabolitter, slik som nukleotider og NAD pluss. Interessant nok økte eksogent tilskudd med NAD pluss-forløperen, beta-nikotinamidmononukleotid, mengden av mitokondrielle nukleotider og fremmet mtDNA-replikasjon [15]. Redusert mtDNA-kopiantall er assosiert med økt oksidativt stress gjennom ROS-overproduksjon, noe som ytterligere resulterer i mitokondrierelaterte metabolske forstyrrelser og apoptose [16].
En rekke beslektede enzymer og regulatoriske faktorer er involvert i mtDNA-replikasjon, slik som mtDNA-polymerase (POL ), mitokondriell enkeltstrengsbindende protein (mtSSB), mitokondriell helicase TWINKLE, topoisomerase og mitokondriell transkripsjonsfaktor A (TFAM) [17,18 ]. Alle disse faktorene er hovedsakelig kodet av kjernefysiske gener. Derfor er mtDNA-replikasjon regulert av både sitt eget og kjernefysiske DNA. POL - mangelfulle celler opplever alvorlig delesjon av mtDNA, som reddes ved å øke mitokondriell deoksyribonukleosidtrifosfatproduksjon [19]. Aktiverende transkripsjonsfaktor assosiert med stress 1 (ATFS-1) er fraværende i sunne mitokondrier på grunn av dens nedbrytning av den mtDNA-bundne proteasen Lon peptidase 1 (LONP-1), men den akkumuleres i skadede mitokondrier. LONP-1-hemming øker ATFS-1- og PLO-binding til mtDNA og fremmer mtDNA-replikasjon og forbedrer dermed mtDNA-heteroplasmiforholdet og gjenoppretter OXPHOS [20]. mtSSB er kritisk nødvendig for å begrense transkripsjonsinitiering for å optimalisere RNA-primerdannelse ved to opphav til mtDNA-replikasjon og dens mutasjoner påvirker mtDNA-replikasjon og induserer mtDNA-delesjon [21,22]. TFAM-mangel forverrer reduksjonen av mtDNA-kopinummer og OXPHOS [23]. Oppsummert er fullstendig mtDNA-replikasjon en ryddig prosess. Når ett av disse trinnene blir forstyrret, kan det føre til nedsatt mtDNA-replikasjon.

Standardisert Cistanche
2. mtDNA-mutasjoner
mtDNA ser ut til å være hyppigere og mer mottakelig for mutasjoner enn kjernefysisk DNA. mtDNA-mutasjoner er ofte funnet i mors arvelige sykdommer, og ugunstige miljøfaktorer kan også forårsake sporadiske mtDNA-mutasjoner [24]. Både den genkodende regionen og forskyvningsløkken (D-loop), som spiller en rolle i transkripsjonsregulering, kan muteres i mtDNA, og dermed påvirke de vitale områdene i genomet.
Fordi hvert mitokondrie inneholder en annen mengde mtDNA-kopier, kan typene mtDNA-mutasjoner deles inn i homogene og heterogene mutasjoner. Homogene mutasjoner refererer til mutasjonen av alt mtDNA i mitokondrier, mens heterogene mutasjoner refererer til sameksistensen av mutant og villtype mtDNA. mtDNA-mutasjoner har den kumulative effekten av defekt mitokondriell funksjon, og forårsaker svekkelse av en cellulær energiforsyning [25]. De biologiske konsekvensene av mutasjoner avhenger av andelen mutant mtDNA og typen mutasjon som bæres av cellene. Minimum antall kopier av mtDNA-mutasjoner som forårsaker dysfunksjon i spesifikke vev og organer kalles terskelverdien, og jo lavere terskelverdien er, desto større er sannsynligheten for sykdomsforekomst [26]. Mutasjonsterskelverdien har viktige implikasjoner for den kliniske manifestasjonen av energiavhengighet og sykdommen og terskelverdien er forskjellig mellom individuelle vev og organer.
Med den kontinuerlige forbedringen av deteksjonsteknologier blir mtDNA-mutasjonsrelaterte sykdommer oppdaget og får i økende grad oppmerksomheten til forskere og klinikere. Studier har funnet at mtDNA-mutasjoner er assosiert med utviklingen av en rekke sykdommer, inkludert kardiovaskulære sykdommer, nyresykdommer, svulster og aldring [27–30]. For tiden er det mangel på effektiv behandling for mtDNA-mutasjonsrelaterte sykdommer, som hovedsakelig fokuserer på å forbedre kliniske symptomer. Derfor er det spesielt viktig å nøyaktig oppdage stedene for mtDNA-mutasjoner.

Cistanche pulver
3. mtDNA-lekkasje
Mitokondriemembranen ligner på cellemembranen og har en tolagsstruktur for å opprettholde integriteten til mitokondriene. Lipider og proteiner er hovedkomponentene i den indre mitokondrielle membranen (IMM) og den ytre mitokondrielle membranen (OMM). Forskjellen i sammensetningen deres bestemmer at IMM og OMM har forskjellige fysiologiske funksjoner. OMM inneholder et stort antall integrerte membranproteiner som regulerer mitokondriell permeabilitet. I kontrast er IMM sammensatt av en rekke bærerproteiner og metabolismerelaterte enzymer som er ansvarlige for komplekse mitokondrielle biokjemiske reaksjoner. Normalt er mtDNA innkapslet i mitokondriematrisen. Når den strukturelle integriteten til mitokondriemembranen er forstyrret, frigjøres mtDNA til cytoplasmaet. Defekt mitokondriell membranstruktur og økt permeabilitet er nøkkelårsaker til mtDNA-lekkasje. Endret lipidsammensetning i mitokondriell membran fører til økt mitokondriell permeabilitet og mtDNA-lekkasje [31]. Mitokondriell skade forårsaket av flere faktorer er ofte ledsaget av mtDNA-lekkasje. Nyere studier avslørte at mtDNA kan frigjøres til cytoplasmaet gjennom flere veier, for eksempel BAK/BAX-poren, spenningsavhengig anionkanal (VDAC) oligomerpore og mitokondriell permeabilitetsovergangspore (mPTP) [32–34], som vist. i figur 2. Disse prosessene er imidlertid studert i inkonsekvent grad blant ulike sykdommer.
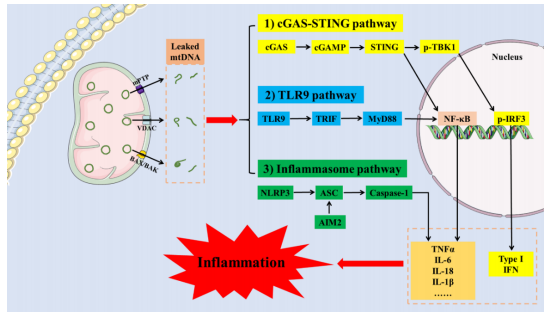
Figur 2. mtDNA-lekkasje induserer betennelsesaktivering. mtDNA frigjøres til cytoplasmaet gjennom flere veier, slik som BAK/BAX-poren, VDAC-oligomerporen og mPTP tDNAfrigitt i cytoplasmaet aktiverer inflammatoriske responser gjennom flere signalveier inkludert cGAS-STING, TLR9, NLRP3 og AIM2 inflammasom. (cGAS, syklisk GMP-AMP-syntase; STING, stimulator av interferon-gener; CGAMP, syklisk guanosinmonofosfat-adenosinmonofosfat; p-TBK1, fosfo-TANK-bindende kinase-1; TLR9, tolllignende reseptor 9; TRIF, TIR-domeneholdig adapterinduserende IFN B; MyD88, myeloid differensieringsprotein 88, NLRP3nod-lignende reseptor pyrin 3; ASC, apoptoseassosiert flekklignende protein; AlM2, fraværende i melanom2; VDAC, spenningsavhengig anionkanal; mPTP, mitokondriell permeabilitet transition pore?INFa, tumornekrosefaktor a; IL-6, interleukin-6; IL-18, interleukin-18; IL-1B, interleukin{{30} }B; NF-KB. nukleær faktor kappa-B; p-IRF3, fosfo-interferon regulatorisk faktor -3; IFN, interferon).
Accumulated mtDNA in the cytoplasm is recognized as an endogenous pathogen and activates innate immune and inflammatory responses [12,35]. mtDNA released into the cytoplasm can activate inflammatory responses through multiple signaling pathways, including the cyclic GMP-AMP synthase (cGAS)-stimulator of interferon genes (STING), toll-like receptor 9 (TLR9), nucleotide-binding oligomerization domain-like receptor protein 3 (NLRP3) and absent in melanoma (AIM2) inflammasome signaling pathways [36]. cGAS is a member of the nucleotidyl transferase family and contains a DNA-binding region, which recognizes endogenous and exogenous DNA, including viral DNA, mtDNA, chromosomal terminal telomeric repeat sequence DNA, and cytoplasmic chromatin fragments. The recognition of DNA by cGAS is length-dependent, and DNA can effectively bind to cGAS when the length of dsDNA is >45 bp [37]. Fosfolipase-ryggraden i DNA binder seg til cGAS på en ikke-sekvensavhengig måte og induserer konformasjonsendringer [38]. mtDNA frigjort til cytoplasma eller perifer sirkulasjon gjenkjennes av cGAS og katalyserer genereringen av den andre messenger sykliske guanosinmonofosfat-adenosinmonofosfat (cGMP), som ytterligere aktiverer STING-relaterte veier, inkludert type 1 interferon (IFN) respons og den klassiske NF-κB inflammatorisk vei, og aktiverer dermed immunbetennelsen [39]. TLR9 er et transmembranprotein hovedsakelig lokalisert i det endoplasmatiske retikulumet, som inneholder en ekstracellulær region som gjenkjenner patogen-assosierte molekylære mønstre (PAMPs) og en intracellulær region inkludert en toll/interleukin-1 reseptor (TIR) struktur for nedstrøms signalering. TLR9 kan fungere som en DNA-gjenkjenningsreseptor og delta i den naturlige immunresponsen i menneskekroppen. Et økende antall studier tyder på at TLR9 spiller en viktig rolle i utviklingen av autoimmune sykdommer [40,41]. TLR9 er et medlem av TLR-familien av proteiner som er nærmest relatert til mtDNA [42]. mtDNA aktiverer TLR9 og er involvert i cytokinproduksjon, miltapoptose og nyreskade ved sepsis [43]. TLR9 medierer dannelsen av inflammatoriske responser ved å aktivere NF-KB inflammatorisk vei via myeloide differensieringsfaktor 88 (MyD88) [44]. NLRP3 aktiverer caspase-1 og gastrin D (GSDMD), frigjør store mengder inflammatoriske faktorer og initierer pyroptose, en ny ordnet celledødsmåte [45]. NLRP3 kan gjenkjenne både PAMP-er og fareassosierte molekylære mønstre (DAMPs), og aktivere NLRP3-inflammasom, som består av NLRP3-reseptorprotein, apoptoseassosiert flekklignende protein (ASC) og caspase-1-forløperprotein (pro- caspase-1). En fersk studie fant at mtDNA som lekker inn i cytoplasmaet aktiverte NLRP3-inflammasom i brunt fettvev, som er engasjert i fedme-indusert insulinresistens og svekket termogenese [46]. Den dobbelttrådete DNA-reseptoren AIM2 gjenkjenner også mtDNA frigitt gjennom BAK/BAX-porer og utløser IL-1-sekresjon og pyroptose [47].

Cistanche tubulosa
4. mtDNA-metylering
DNA-metylering er en av de mest studerte epigenetiske mekanismene. Under påvirkning av DNA-metyltransferaser (DNMT) overføres metyldonorforbindelsene avledet fra S-adenosylmetionin (SAM) til CpG-øyene for å danne 50 -metylcytosin (50 -mC), som er den vanligste typen av DNA-metylering. DMNT-er inkluderer to hovedgrupper, DNMT3a og DNMT3b, som katalyserer de novo-metyleringen av umetylerte DNA-duplekser, og DNMT1, som opprettholder metyleringstilstanden til DNA etter semi-konservert replikasjon. Det er rapportert at DNMT-er spiller en betydelig rolle i å regulere trikarboksylsyremetabolitter, mitokondriell respirasjon og oksidativt stress [48,49].
Nyere studier har avdekket at mtDNA også kan være metylert og metylert mtDNA ligger til grunn for sykdomsprogresjon [50]. Nivåene av mtDNA-metylering kan påvirkes av flere intracellulære eller ekstracellulære faktorer. Signifikante abnormiteter i mtDNA-metylering forekommer i en rekke sykdommer, spesielt i mitokondrierelaterte sykdommer [51]. Metylering av mitokondriegenomet kan føre til etiologien til menneskelig sykdom og endrede metyleringsnivåer av mtDNA ble vurdert i dyremodeller og humant vev fra pasienter med fedme, diabetes, kreft og kardiovaskulære og nevrodegenerative sykdommer [14]. Hypermetylering av mtDNA-gener induserer også systemisk insulinresistens og en relatert metabolsk lidelse [52].
mtDNA-metylering er et fremvoksende og ufullstendig forstått fenomen som regulerer mitokondriell funksjon. mtDNA-metylering driver på forskjellige steder av kodende gen-loci, noe som resulterer i redusert mtDNA-kopiantall og endret genuttrykk [53]. Graden av mtDNA-metylering var negativt korrelert med mtDNA-innhold [54]. mtDNA-metylering kan betraktes som en tidlig molekylær hendelse og en potensiell biomarkør for effektiv sykdomsprediksjon og diagnose. mtDNA-metylering er en reversibel epistatisk modifikasjon, noe som gjør den til et viktig terapeutisk mål. Genredigering av mtDNA-metylering er fortsatt i grunnforskning og tidlig klinisk stadium, og som sådan kan sikkerhetsproblemer ikke ignoreres. Det er håpet at utviklingen av mitokondriell genredigeringsteknologi vil hjelpe oss til å forstå hvordan mtDNA metyleres ytterligere.
Referanser
1. Tang, C.; Cai, J.; Yin, XM; Weinberg, JM; Venkatachalam, MA; Dong, Z. Mitokondriell kvalitetskontroll ved nyreskade og reparasjon. Nat. Rev. Nephrol. 2021, 17, 299–318. [CrossRef] [PubMed]
2. Bhatia, D.; Capili, A.; Choi, ME Mitokondriell dysfunksjon ved nyreskade, betennelse og sykdom: Potensielle terapeutiske tilnærminger. Nyre Res. Clin. Pr. 2020, 39, 244–258. [CrossRef]
3. Gilea, AI; Ceccatelli, BC; sorenskriver, M.; di Punzio, G.; Goffrini, P.; Baruffini, E.; Dallabona, C. Saccharomyces cerevisiae som et verktøy for å studere mutasjoner i kjernefysiske gener involvert i sykdommer forårsaket av mitokondriell DNA-ustabilitet. Genes 2021, 12, 1866. [CrossRef] [PubMed]
4. Hershberger, KA; Rooney, JP; Turner, EA; Donoghue, LJ; Bodhicharla, R.; Maurer, LL; Ryde, IT; Kim, JJ; Joglekar, R.; Hibshman, JD; et al. Mitokondriell DNA-skade i tidlig liv resulterer i livslange underskudd i energiproduksjon mediert av redokssignalering i Caenorhabditis elegans. Redox Biol. 2021, 43, 102000. [CrossRef] [PubMed]
5. van der Slikke, EC; Star, BS; van Meurs, M.; Henning, RH; Moser, J.; Bouma, HR Sepsis er assosiert med mitokondriell DNA-skade og redusert mitokondriell masse i nyrene til pasienter med sepsis-AKI. Crit. Care 2021, 25, 36. [CrossRef] [PubMed]
6. Jin, L.; Yu, B.; Armando, I.; Han, F. Mitokondriell DNA-mediert betennelse ved akutt nyreskade og kronisk nyresykdom. Oksyd Med. Cell Longev. 2021, 2021, 9985603. [CrossRef]
7. Melki, I.; Allaeys, I.; Tessandier, N.; Levesque, T.; Cloutier, N.; Laroche, A.; Vernoux, N.; Becker, Y.; Benk-Fortin, H.; Zufferey, A.; et al. Blodplater frigjør mitokondrielle antigener i systemisk lupus erythematosus. Sci. Overs. Med. 2021, 13, eaav5928. [CrossRef]
8. Kockler, ZW; Osia, B.; Lee, R.; Musmaker, K.; Malkova, A. Reparasjon av DNA-brudd ved bruddindusert replikering. Annu. Rev. Biochem. 2021, 90, 165–191. [CrossRef]
9. Zhang, X.; Wu, X.; Hu, Q.; Wu, J.; Wang, G.; Hong, Z.; Ren, J. Mitokondriell DNA i leverbetennelse og oksidativt stress. Life Sci. 2019, 236, 116464. [CrossRef]
10. Lin, YH; Lim, SN; Chen, CY; Chi, HC; Ja, CT; Lin, WR Funksjonell rolle for mitokondrielt DNA i kreftprogresjon. Int. J. Mol. Sci. 2022, 23, 1659. [CrossRef]
11. Lechuga-Vieco, AV; Latorre-Pellicer, A.; Calvo, E.; Torroja, C.; Pellico, J.; Acin-Perez, R.; Garcia-Gil, ML; Santos, A.; Bagwan, N.; Bonzon-Kulichenko, E.; et al. Heteroplasmi av villtype mitokondrielle DNA-varianter i mus forårsaker metabolsk hjertesykdom med pulmonal hypertensjon og skrøpelighet. Opplag 2022, 145, 1084–1101. [CrossRef]
12. Zhong, W.; Rao, Z.; Xu, J.; Sun, Y.; Hu h.; Wang, P.; Xia, Y.; Pan, X.; Tang, W.; Chen, Z.; et al. Defekt mitofagi hos gamle makrofager fremmer cytosolisk lekkasje av mitokondriell DNA for å aktivere STING-signalering under steril leverbetennelse. Aldringscelle 2022, 21, e13622. [CrossRef] [PubMed]
13. Nie, Y.; Murley, A.; Golder, Z.; Rowe, JB; Allinson, K.; Chinnery, PF Heteroplasmatiske mitokondrielle DNA-mutasjoner i frontotemporal lobar degenerasjon. Acta Neuropathol. 2022, 143, 687–695. [CrossRef] [PubMed]
14. Stoccoro, A.; Coppede, F. Mitokondriell DNA-metylering og menneskelige sykdommer. Int. J. Mol. Sci. 2021, 22, 4594. [CrossRef] [PubMed]
15. Nomiyama, T.; Setoyama, D.; Yasukawa, T.; Kang, D. Mitochondria metabolomics avslører en rolle av beta-nikotinamid mononukleotidmetabolisme i mitokondriell DNA-replikasjon. J. Biochem. 2022, 171, 325–338. [CrossRef]
16. Castellani, CA; Longchamps, RJ; Sun, J.; Guallar, E.; Arking, DE Tenking utenfor kjernen: Mitokondrielt DNA-kopinummer i helse og sykdom. Mitokondrion 2020, 53, 214–223. [CrossRef]
17. Roy, A.; Kandettu, A.; Ray, S.; Chakrabarty, S. Mitokondriell DNA-replikasjon og reparasjonsdefekter: Kliniske fenotyper og terapeutiske intervensjoner. Biochim. Biofys. Acta Bioenergi. 2022, 1863, 148554. [CrossRef]
18. Manini, A.; Abati, E.; Comi, fastlege; Corti, S.; Ronchi, D. Mitokondriell DNA homeostase svekkelse og dopaminerg dysfunksjon: En skjelvende balanse. Aldring Res. Rev. 2022, 76, 101578. [CrossRef]
19. Blazquez-Bermejo, C.; Carreno-Gago, L.; Molina-Granada, D.; Aguirre, J.; Ramon, J.; Torres-Torronteras, J.; Cabrera-Perez, R.; Martin, MA; Dominguez-Gonzalez, C.; de la Cruz, X.; et al. Økte dNTP-pooler redder utarming av mtDNA i humane POLG-mangelfulle fibroblaster. FASEB J. 2019, 33, 7168–7179. [CrossRef]
20. Yang, Q.; Liu, P.; Anderson, NS; Shpilka, T.; Du, Y.; Naresh, NU; Li, R.; Zhu, LJ; Luk, K.; Lavelle, J.; et al. LONP-1 og ATFS-1 opprettholder skadelig heteroplasmi ved å fremme mtDNA-replikasjon i dysfunksjonelle mitokondrier. Nat. Cell Biol. 2022, 24, 181–193. [CrossRef]
21. Piro-Megy, C.; Sarzi, E.; Tarres-Sole, A.; Pequignot, M.; Hensen, F.; Quiles, M.; Manes, G.; Chakraborty, A.; Senechal, A.; Bocquet, B.; et al. Dominante mutasjoner i mtDNA vedlikeholdsgenet SSBP1 forårsaker optisk atrofi og homeopati. J. Clin. Undersøk. 2020, 130, 143–156. [CrossRef] [PubMed]
22. Jiang, M.; Xie, X.; Zhu, X.; Jiang, S.; Milenkovic, D.; Misic, J.; Shi, Y.; Tandukar, N.; Li, X.; Atanassov, I.; et al. Mitokondriene enkelttrådet DNA-bindende protein er essensielt for initiering av mtDNA-replikasjon. Sci. Adv. 2021, 7, eabf8631. [CrossRef] [PubMed]
23. Otten, A.; Kamps, R.; Lindsey, P.; Gerards, M.; Pendeville-Samain, H.; Muller, M.; van Tienen, F.; Smeets, H. Tfam Knockdown resulterer i reduksjon av mtDNA-kopinummer, OXPHOS-mangel og abnormiteter i sebrafiskembryoer. Front. Cell Dev. Biol 2020, 8, 381. [CrossRef] [PubMed]
24. Sercel, AJ; Carlson, NM; Patananan, AN; Teitell, MA Mitokondriell DNA-dynamikk i omprogrammering til pluripotens. Trender Cell Biol. 2021, 31, 311–323. [CrossRef]
25. Sato, T.; Goto-Inoue, N.; Kimishima, M.; Toyoharu, J.; Minei, R.; Ogura, A.; Nagoya, H.; Mori, T. En ny ND1-mitokondriell DNA-mutasjon arves av mor i veksthormontransgenese hos amago-laks (Oncorhynchus masouIshikawae). Sci. Rep. 2022, 12, 6720. [CrossRef]
26. McMillan, RP; Stewart, S.; Budnick, JA; Caswell, CC; Hulver, MW; Mukherjee, K.; Srivastava, S. Kvantitativ variasjon i m.3243A > G-mutasjon produserer diskrete endringer i energimetabolismen. Sci. Rep. 2019, 9, 5752. [CrossRef]
27. Liu, H.; Liu, X.; Zhou, J.; Li, T. Mitokondrielt DNA er en viktig drivkraft ved iskemi-reperfusjonsskade ved kardiovaskulære sykdommer. Oksyd. Med. Cell Longev. 2022, 2022, 6235747. [CrossRef]
28. Xu, C.; Tong, L.; Rao, J.; Ye, Q.; Chen, Y.; Zhang, Y.; Xu, J.; Mao, X.; Meng, F.; Shen, H.; et al. Heteroplasmic and homoplasmic m.616T>C i mitokondrier tRNAPhe fremmer isolert kronisk nyresykdom og hyperurikemi. JCI Insight. 2022, 7, e157418. [CrossRef]
29. Ji, X.; Guo, W.; Gu, X.; Guo, S.; Zhou, K.; Su, L.; Yuan, Q.; Liu, Y.; Guo, X.; Huang, Q.; et al. Mutasjonsprofilering av mtDNA-kontrollregionen avslører tumorspesifikk evolusjonær seleksjon involvert i mitokondriell dysfunksjon. Ebiomedicine 2022, 80, 104058. [CrossRef]
30. Nunn, CJ; Goyal, S. Beredskap og seleksjon i mitokondriell genomdynamikk. Elife 2022, 11, e76557. [CrossRef]
31. Hancock-Cerutti, W.; Wu, Z.; Xu, P.; Yadavalli, N.; Leonzino, M.; Tharkeshwar, AK; Ferguson, SM; Shadel, GS; De Camilli, P. ER-lysosom lipidoverføringsprotein VPS13C/PARK23 forhindrer avvikende mtDNA-avhengig STING-signalering. J. Cell Biol. 2022, 221, e202106046. [CrossRef] [PubMed]
32. McArthur, K.; Whitehead, LW; Huddlestonn, JM; Li, L.; Padman, BS; Oorschot, V.; Geoghegan, ND; Chappaz, S.; Davidson, S.; San, CH; et al. BAK/BAX makroporer letter mitokondriell herniering og mtDNA-utstrømning under apoptose. Science 2018, 359, eaao6047. [CrossRef] [PubMed]
33. Kim, J.; Gupta, R.; Blanco, LP; Yang, S.; Shteinfer-Kuzmine, A.; Wang, K.; Zhu, J.; Yoon, HE; Wang, X.; Kerkhofs, M.; et al. VDAC-oligomerer danner mitokondrielle porer for å frigjøre mtDNA-fragmenter og fremme lupuslignende sykdom. Vitenskap 2019, 366, 1531–1536. [CrossRef] [PubMed]
34. Yu, CH; Davidson, S.; Harapas, CR; Hilton, JB; Mlodzianoski, MJ; Laohamonthonkul, P.; Louis, C.; Low, R.; Mockingg, J.; De Nardo, D.; et al. TDP-43 utløser mitokondriell DNA-frigjøring via mPTP for å aktivere cGAS/STING i ALS. Cell 2020, 183, 636–649. [CrossRef]
35. Li, JS; Hao, YZ; Hou, ML; Zhang, X.; Zhang, XG; Cao, YX; Li, JM; Ma, J.; Zhou, ZX Utvikling av en rekombinasestøttet amplifikasjon kombinert med lateralstrømningspeilepinneanalyse for rask påvisning av afrikansk svinepestvirus. Biomed. Environ. Sci. 2022, 35, 133–140.
36. Harapas, CR; Idiiatullina, E.; Al-Azab, M.; Hrovat-Schale, K.; Reygaerts, T.; Steiner, A.; Laohamonthonkul, P.; Davidson, S.; Yu, CH; Booty, L.; et al. Organellar homeostase og medfødt immunforsvar. Nat. Rev. Immunol. 2022, 9, 539–545. [CrossRef]
37. Luecke, S.; Holleufer, A.; Christensen, MH; Jonsson, KL; Boni, GA; Sørensen, LK; Johannsen, M.; Jakobsen, MR; Hartmann, R.; Paludan, SR cGAS aktiveres av DNA på en lengdeavhengig måte. Embo. Rep. 2017, 18, 1707–1715. [CrossRef]
38. Kato, K.; Omura, H.; Ishitani, R.; Nureki, O. Syklisk GMP-AMP som en endogen andre budbringer i medfødt immunsignalering av cytosolisk DNA. Annu. Rev. Biochem. 2017, 86, 541–566. [CrossRef]
39. Luteijn, RD; Zaver, SA; Gowen, BG; Wyman, SK; Garelis, NE; Onia, L.; McWhirter, SM; Katibah, GE; mais, JE; Woodward, JJ; et al. SLC19A1 transporterer immunoreaktive sykliske dinukleotider. Natur 2019, 573, 434–438. [CrossRef]
40. Ding, P.; Tan, Q.; Wei, Z.; Chen, Q.; Wang, C.; Qi, L.; Wen, L.; Zhang, C.; Yao, C. Toll-lignende reseptor 9-mangel induserer osteoklastisk bentap via tarmmikrobiota-assosiert systemisk kronisk betennelse. Bone Res. 2022, 10, 42. [CrossRef]
41. Honke, N.; Lowin, T.; Opgenoorth, B.; Shaabani, N.; Lautwein, A.; Teijaro, JR; Schneider, M.; Pongratz, G. Endogent produserte katekolaminer forbedrer den regulatoriske funksjonen til TLR9-aktiverte B-celler. PLoS Biol. 2022, 20, e3001513. [CrossRef] [PubMed]
42. Hepokoski, M.; Singh, P. Mitokondrier som mediatorer av systemisk betennelse og organkrysstale ved akutt nyreskade. Er. J. Physiol. Ren. Physiol. 2022, 6, F589–F596. [CrossRef] [PubMed]
43. Tsuji, N.; Tsuji, T.; Ohashi, N.; Kato, A.; Fujigaki, Y.; Yasuda, H. Rollen til mitokondrielt DNA i septisk AKI via toll-lignende reseptor. J. Am. Soc. Nephrol. 2016, 27, 2009–2020. [CrossRef] [PubMed]
44. Pradhan, P.; Leketøy, R.; Jhita, N.; Atalis, A.; Pandey, B.; Beach, A.; Blanchard, EL; Moore, SG; Gallia, DA; Santangelo, PJ; et al. TRAF6-IRF5-kinetikk, TRIF og biofysiske faktorer driver synergistiske medfødte responser på partikkelmediert MPLA-CpG-presentasjon. Sci. Adv. 2021, 7, eabd4235. [CrossRef] [PubMed]
45. De Gaetano, A.; Solodka, K.; Zanini, G.; Selleri, V.; Mattioli, AV; Nasi, M.; Pinti, M. Molecular Mechanisms of mtDNA-Mediated Inflammation. Cells 2021, 10, 2898. [CrossRef]
46. Huang, Y.; Zhou, JH; Zhang, H.; Canfran-Duque, A.; Singh, AK; Perry, RJ; Shulman, GI; Fernandez-Hernando, C.; Min, W. Brown adipose TRX2-mangel aktiverer mtDNA-NLRP3 for å svekke termogenese og beskytte mot diett-indusert insulinresistens. J. Clin. Investere. 2022, 132, e148852. [CrossRef]
47. Wang, L.; Liu, T.; Yang, S.; Sun, L.; Zhao, Z.; Li, L.; Hun, Y.; Zheng, Y.; Ja, X.; Bao, Q.; et al. Forurensninger av perfluoralkylstoffer aktiverer det medfødte immunsystemet gjennom AIM2-inflammasomet. Nat. Commun. 2021, 12, 2915. [CrossRef]
48. Shen, J.; Wang, C.; Li, D.; Xu, T.; Myers, J.; Ashton, JM; Wang, T.; Zuscik, MJ; McAlinden, A.; O'Keefe, RJ DNA-metyltransferase 3b regulerer leddbruskhomeostase ved å endre metabolismen. JCI Insight. 2017, 2, e93612. [CrossRef]
49. Damal, VS; Ebert, SM; Lim, HW; Kim, J.; Du, D.; Jung, BC; Palacios, HH; Tcheau, T.; Adams, CM; Kang, S. En nødvendig rolle for DNMT3A i utholdenhetstrening ved å undertrykke. g ALDH1L1-mediert oksidativt stress. Embo. J. 2021, 40, e106491.
50. Liu, Q.; Li, H.; Guo, L.; Chen, Q.; Gao, X.; Li, PH; Tang, N.; Guo, X.; Deng, F.; Wu, S. Effekter av kortvarig personlig eksponering for luftforurensning på blodplate-mitokondrielle DNA-metyleringsnivåer og potensiell reduksjon av L-arginin-tilskudd. J. Hazard. Mater. 2021, 417, 125963. [CrossRef]
51. Wang, Y.; Gao, J.; Wu, F.; Lai, C.; Li, Y.; Zhang, G.; Peng, X.; Yu, S.; Yang, J.; Wang, W.; et al. Biologiske og epigenetiske endringer av mitokondrier involvert i cellulær replikativ og hydrogenperoksid-indusert for tidlig senescens av humane embryonale lungefibroblaster. Økotoksikol. Env. Saf 2021, 216, 112204. [CrossRef] [PubMed]
52. Cao, K.; Lv, W.; Wang, X.; Dong, S.; Liu, X.; Yang, T.; Xu, J.; Zeng, M.; Zou, X.; Zhao, D.; et al. Hypermetylering av hepatisk mitokondriell ND6 provoserer systemisk insulinresistens. Adv. Sci (Weinh) 2021, 8, 2004507. [CrossRef] [PubMed]
53. Liu, Y.; Song, F.; Yang, Y.; Yang, S.; Jiang, M.; Zhang, W.; Ma, Z.; Gu, X. Mitokondriell DNA-metyleringsdrift og postoperativt delirium hos mus. Eur. J. Anaesthesiol. 2022, 39, 133–144. [CrossRef] [PubMed]
54. Zhang, J.; Shang, J.; Wang, F.; Huo, X.; Sun, R.; Ren, Z.; Wang, W.; Yang, M.; Li, G.; Gao, D.; et al. Redusert mitokondriell D-løkke-region-metylering medierer en økning i mitokondrielt DNA-kopiantall i CADASIL. Clin. Epigenetics 2022, 14, 2. [CrossRef] [PubMed]
Jun Feng 1,2, Zhaowei Chen 1,2,†, Wei Liang 1,2, Zhongping Wei 1,2 og Guohua Ding 1,2,
1 avdeling for nefrologi, Renmin sykehus ved Wuhan University, Wuhan 430060, Kina
2 Nephrology and Urology Research Institute ved Wuhan University, Wuhan 430060, Kina






