Pyroptose ved nyresykdom
Feb 19, 2022
Kontakt: emily.li@wecistanche.com
Yujia Wang, Yinshuang Li og Yanfang Xu1
Abstrakt
I de siste tiårene har apoptoseinterferens blitt ansett som klinisk irrelevant i sammenheng med nyreskade. Den nylige oppdagelsen av programmert nekrotisk celledød, inkludert nekroptose, ferroptose og pyroptose, forfrisket vår forståelse av rollen til celledød inyresykdom. Pyroptose er karakterisert ved en lytisk pro-inflammatorisk type celledød som følge av gasdermin-indusert membranpermeabilisering via aktivering av inflammatoriske kaspaser og inflammasomer. De fareassosierte molekylære mønstrene (DAMPs), alarminer og pro-inflammatoriske cytokiner frigjøres fra pyroptotiske celler på en ukontrollert måte, noe som provoserer inflammasjon, noe som resulterer i sekundære organ- eller vevsskader. De kaspaser og inflammasomaktiveringsrelaterte proteiner og poredannende effektorproteiner kjent som GSDMD og GSDME har vært involvert i en rekke akutte og kroniske mikrobielle og ikke-mikrobiellenyresykdommer. Her gjennomgår vi de siste fremskrittene innen patologiske mekanismer for pyroptose inyresykdomog fremheve potensielle terapeutiske strategier i fremtiden.

Klikk her for å vite mer om måtene å behandle nyresykdom på
Introduksjon
Programmert celledød (PCD) spiller en kritisk rolle i både utviklingen av flercellede organismer og vedlikeholdet av voksent vev. I skarp kontrast til utilsiktet celledød (f.eks. nekrose) som er øyeblikkelig, katastrofal og ukontrollerbar, er PCD tett regulert, noe som muliggjør farmakologiske og genetiske moduleringer.1 I løpet av de siste tiårene har distinkte former for PCD blitt identifisert, inkludert ikke-inflammatoriske prosesser (f.eks. apoptose) og svært inflammatoriske prosesser (f.eks. pyroptose og nekroptose). I tillegg til tilstedeværelse eller fravær av betennelse, kan apoptose og pyroptose skilles ut ved morfologi. De karakteristiske morfologiske endringene av apoptose inkluderer cellekrymping, membranblebbing, apoptotisk kroppsdannelse og DNA-fragmentering, men ingeninflammatoriskinnholdsfrigjøring.2 Motsatt har pyroptose cellehevelse, membranruptur og ukontrollert frigjøring av inflammatorisk innhold. Nekroptose deler fellestrekk med pyroptose, inkludert åpenbar betennelse og tap av membranintegritet.3
Selv om pyroptose og apoptose begge er caspase-avhengige, er de spesifikke caspase-familiemedlemmene som er involvert helt forskjellige. Apoptotiske kaspaser inkluderer kaspaser-8/9/10 som initiator og kaspaser-3/6/7 som eksekutorer,4 mens pyroptose er avhengig av kaspaser-1/4/5/11 i gasdermin D ( GSDMD)-mediert pyroptose og kaspaser-3 i gasdermin E (GSDME)-mediert pyroptose.5,3 Nekroptose fortsetter via trinnvis aktivering av reseptorinteragerende proteinkinase-3 (RIPK3) og blandet avstamning kinase domene-lignende pseudokinase (MLKL), som kan hemmes av caspase-8. Det er forskjellig fra GSDM-er i pyroptose, hvis aktivering er caspase-avhengig. Forholdet mellom kjønnsmins og MLKL under fysiologiske forhold har blitt et tema av interesse for forskning.3 Ferroptose er et peroksidasjonskontrollert system som ikke involverer kaspaser, vanligvis ledsaget av en stor mengde jernakkumulering og lipidperoksidasjon.6 Ganske lite er kjent om samspillet mellom ferroptose og pyroptose.
Økende eksperimentelle bevis støtter hypotesen om at pyroptose er en betydelig faktor inyresykdommer. I denne gjennomgangen diskuterer vi de molekylære mekanismene til pyroptose, de eksisterende dataene om pyroptose inyresykdommerog potensielle terapier.
Oversikt over Pyroptosis
Eksekutører
Pyroptose er definert som gasdermin-avhengig for dets nøkkeltrinn med poredannelse i plasmamembranen utføres av masterminds, noe som gjør det ganske forskjellig fra andre typer PCD. GSDMD er det første medlemmet av gasdermin-familien som ble funnet å være involvert i pyroptose.7–9 GSDMD i full lengde forblir i en autoinhibert tilstand gjennom bindingen av C-terminalt domene til det N-terminale domenet. Ved spaltning kan det N-terminale fragmentet av GSDMD (GSDMD N) oligomerisere for å danne porer (med en indre diameter på 12–14 nm) på plasmamembranen,10 som svekker permeabilitetsbarrieren og forårsaker cellelyse. GSDMD-spaltning medieres gjennom kanoniske eller ikke-kanoniske veier som involverer henholdsvis caspase-1 eller caspaser-4/5/11.5,11 GSDMD-mediert pyroptose er definert som inflammasomavhengig gitt at caspaser-1/4 /5/11 aktiveres av forskjellige inflflammasomer. Nyere studier viste at GSDMD-spalting også kan induseres av nøytrofil elastase i aldrende nøytrofiler,12 og av kaspase-8 i makrofager under Yersinia-infeksjon.13,14
Genetisk mutasjon av GSDME, et annet medlem av gasdermin-familien, ble først identifisert som årsaken til autosomalt dominant ikke-syndromisk hørselstap hos mennesker.15 Nyere studier har avslørt rollen til GSDME i pyroptose.16,17 GSDME er sterkt uttrykt i ulike typer normalt vev; den er imidlertid stilnet i de fleste tumorceller på grunn av promotorhypermetylering, og modulering av dens ekspresjon med DNA-metyltransferasehemmer vil forbedre kjemoterapisensitiviteten.17 Forskjellig fra GSDMD, spaltes GSDME inn i GSDME-C og GSDME-N av aktivert caspase{{6 }} og er uavhengig av inflammasomdannelse. GSDME-mediert pyroptose forekommer nedstrøms for den mitokondrielle apoptotiske banen, og høy ekspresjon av GSDME og vedvarende mitokondriell permeabilitet vil endre måten celledød pågår fra apoptose til pyroptose.18
Andre medlemmer av gasdermin-familien, inkludert GSDMA, GSDMB og GSDMC, deler svært konserverte gasdermin-N- og gasdermin-C-domener med GSDMD og GSDME.19 GSDMB kan spaltes og aktiveres av granzym A fra cytotoksiske lymfocytter.20 En fersk studie viste at programmert dødsligand 1 byttet tumornekrosefaktor (TNF) - en indusert apoptose til pyroptose i kreftceller, og dette og mediert ved å forbedre GSDMC-gentranskripsjonen. GMC-aktivering ble indusert av caspase-8 etter TNF-a-behandling, under hypoksitilstanden.21 Mekanismen som GSDMA ville bli aktivert med forblir imidlertid uutforsket.
Signalveier
GSDMD-mediert pyroptose. GSDMD-mediert pyroptose initieres av gjenkjennelsen av patogen-assosierte molekylære mønstre (PAMPs) og skadeassosierte molekylære mønstermolekyler (DAMPs) med påfølgende inflammasomaktivering.22 Den første og mest omfattende studerte formen for GSDMD-mediert pyroptose er den kanoniske banen pyroptotic. , også kjent som den caspase-1-avhengige banen. Caspase-1 har lenge vært involvert i celledød, som tidligere ble forvekslet med apoptose23,24 og nekroptose.25 I 2001 ble formen for PCD som involverte caspase-1 skilt fra apoptose og nekroptose ved sin inflammatoriske respons og karakteristisk morfologi inkludert tidlig tap av membranintegritet.26,27
Som respons på patogeninvasjon eller vertsimmunologisk utfordring, oppfatter mønstergjenkjenningsreseptorer (PRR) både PAMP og/eller DAMP. I den kanoniske pyroptotiske banen, flere PRR-er som fraværende i melanom 2 (AIM2)-lignende reseptorer (ALR), nukleotidbindende oligomeriseringsdomene (NOD)-lignende reseptorer (NLR) eller pyrinproteiner, og broadaptere som apoptose-assosierte flekklignende proteiner (ASCs), vil sette sammen en multiproteinplattform (dvs. inflammasom) som rekrutterer pro-kaspase-1 og deretter genererer aktiv caspase-1.28 Som et unntak kan NLRC4 binde seg til medlemmer av NLR-familien av apoptoseinhibitoriske proteiner (NAIPs) i stedet for ASC for å danne inflammasom, og deretter aktivere procaspase-1.29 Aktivert caspase-1 har aktiviteten til å behandle pro-IL-1b og pro-IL-18 til modne former,30 som gir pyroptose proinflammatoriske funksjoner, og skiller den fra apoptose. Parallelt med prosessen med inflammatoriske cytokiner, spalter aktivert caspase-1 GSDMD for å danne membranporer22,31,32 (figur 1). Dannelsen av membranporer fører til forstyrrelse av cellemembranintegriteten, frigjøring av inflammatorisk intracellulært innhold og til slutt cellelyse. NLRP3 er det mest karakteriserte inflammasomet.33 NLRP3 reagerer på et bredt spekter av stress, inkludert intracellulære patogener og ekstra-cytoplasmatiske inflammatoriske stimuli.34 Temaet NLRP3-aktivering har tiltrukket seg stor oppmerksomhet, og forskere har foreslått forskjellige mekanismer inkludert oksidert mitokondrielt DNA, generering av mitokondrielle reaktive oksygenarter (ROS), kaliumutstrømning ut av cellen og frigjøring av katepsin etter lysosomal destabilisering.35 Til tross for mange års intensiv innsats, er de eksakte mekanismene for NLRP3-aktivering fortsatt under debatt. Det er interessant at NLRP3 kan utløses av nekroptose-signalering, 36–38 som antyder potensiell krysstale mellom nekroptose og pyroptose. AIM2-inflammasomet oppfører seg annerledes enn NLR-inflflammasomer ettersom det kan gjenkjenne og binde cytosolisk dsDNA, som kan frigjøres under patogeninfeksjon39,40 eller genereres i tumorceller.41,42
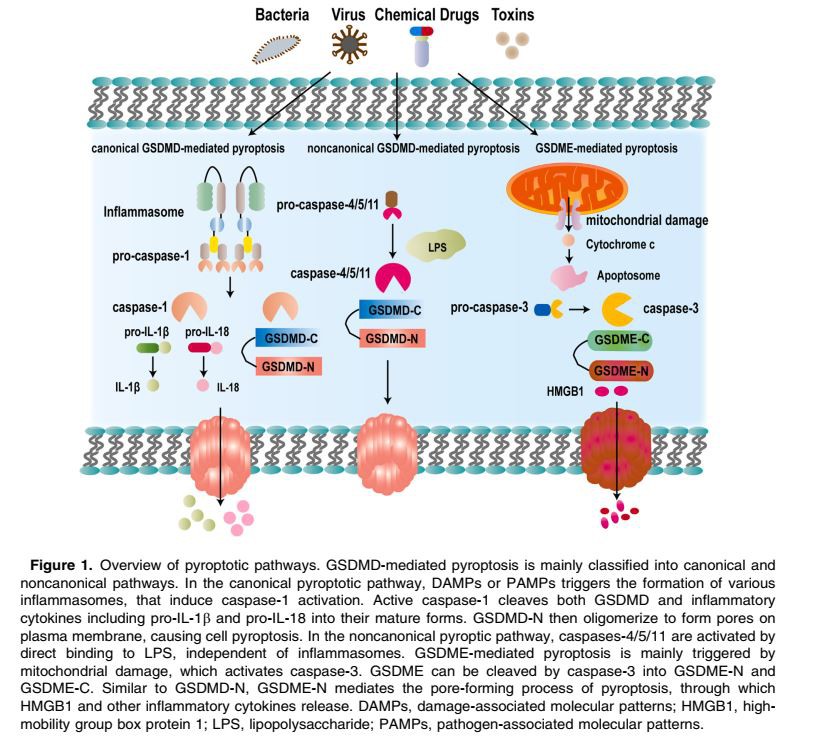
I den ikke-kanoniske pyroptotiske banen er caspase-11 (i mus) og caspaser-4/5 (hos mennesker) ansvarlige for GSDMD-spaltning (figur 1). I 2011 rapporterte Kayagaki et al.43 at tap av caspase-11 men ikke caspase-1 kunne blokkere IL-1b-modning og sekresjon indusert av gramnegative bakterier, og dermed beskytte mus mot endotoksisk sjokk. Ytterligere studier oppdaget at lipopolysakkarid (LPS), hovedtoksinet til de gramnegative bakteriene, er utløseren av det ikke-kanoniske inflammasomet.44,45 Uavhengig av PRR, kunne caspase-11 selv gjenkjenne LPS direkte ved å binde seg til lipidet. En komponent av LPS.46 Activated caspase-11 spaltet til slutt GSDMD for å indusere pyroptose, lik den kanoniske banen. I det siste har menneskelig kaspase-4/5 vist seg å ha samme funksjon som musekaspase-11. Poelzl et al.47 rapporterte at tyrosinkinase 2, en cytokinreseptorassosiert kinase, kunne fungere som en kritisk oppstrømsregulator av caspase-11 og tillot ikke-kanonisk inflammasomaktivering under endotoksemi.
I tillegg til disse kanoniske og ikke-kanoniske pyroptotiske banene, har nyere studier kastet nytt lys over GSDMD-mediert pyroptose. Kambara et al. fant at z-YVAD-fmk, en kaspasehemmer, ikke klarte å blokkere nøytrofillysat-fremkalt GSDMD-spaltning, noe som tyder på at GSDMD-spaltning med nøytrofillysat kan være kaspase-uavhengig.12 De identifiserte videre at den nøytrofile serinproteasen ELANE var GSDMD-kleaveren nøytrofiler. Orning et al.13 og Sarhan et al.14 gjorde en stor oppdagelse på en ny form for GSDMD-spaltning indusert av caspase-8 i Yersinia-infiserte makrofager. Disse to gruppene demonstrerte at hemming av transformerende vekstfaktor (TGF)b-assosiert kinase (TAK1) under Yersinia-infeksjon ville fremme dannelsen av et celledødskompleks bestående av RIPK1 og caspase-8, og drive spaltningen av GSDMD i makrofager. Videre avslørte Demarco et al.48 detaljene om caspase-8 involvering i GSDMD-spalting og ga overbevisende bevis for at caspase-8-avhengig GSDMD-aktivering ville fremme TNF-a-indusert dødelighet uavhengig av inflammasomaktivering.
GSDME-mediert pyroptose. I motsetning til andre caspase-familiemedlemmer, har caspase-3, kløveren av GSDME, lenge vært definert som den viktigste apoptotiske eksekveren for både indre og ekstrinsiske veier. GSDME-mediert pyroptose deler de samme oppstrømseffektorene med apoptose, der mitokondriell skade spiller en avgjørende rolle (figur 1). GSDME-overekspresjon i tumorceller bytter apoptose indusert av kjemoterapi til pyroptose.17 I motsetning til dette, når uttrykket av GSDME-genet oppheves, forblir makrofager i den apoptotiske fasen karakterisert ved membranblebbing og apoptotisk kroppsdannelse, i stedet for å gå inn i den pyroptotiske fasen karakterisert. ved membranhevelse og ballongdannelse.16 Foruten påvirkningene av GSDME-uttrykk, fant Xu et al.18 at vedvarende mitokondriell permeabilitetsovergang kunne drive sammenstillingen av en Apaf-1-kaspase-4/11-pyroptosom som utløser GSDME- avhengig pyroptose, mens permeabilisering av mitokondriell ytre membran fører til dannelse av apoptosom for å indusere apoptose. Kontroversielt rapporterte andre forskere at mitokondriell ytre membranpermeabilisering forårsaket av BAX/BAK-aktivering49 eller Tom20/BAX-montering50 også induserer GSDME-avhengig pyroptose i tumorceller. Dessuten kunne GSDME-N permeabilisere mitokondriene, frigjøre cytokrom c fra mitokondrier og forbedre kaspase-3-aktivering, og danne en selvforsterkende positiv feed-forward-løkke.51
Pyroptose ved nyresykdom
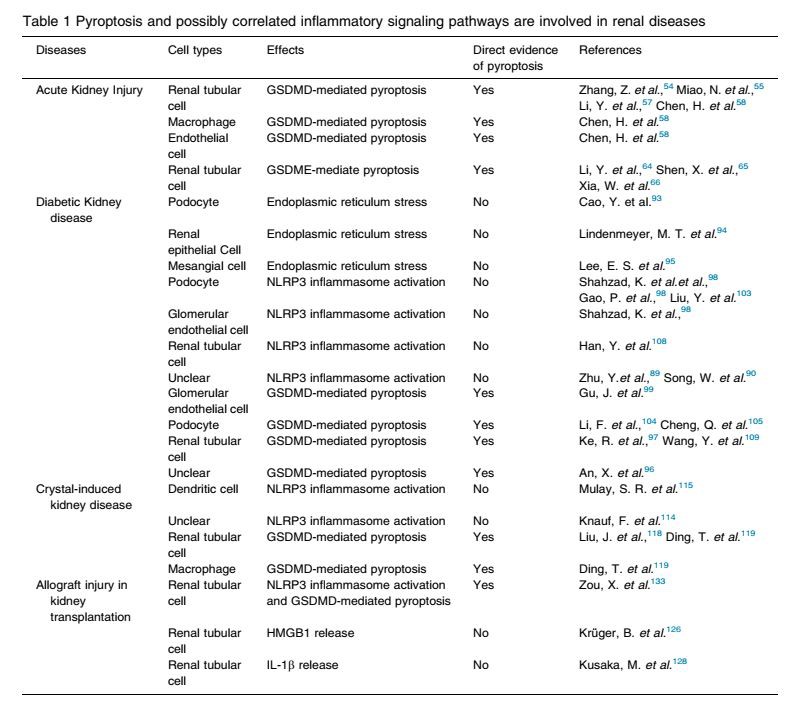
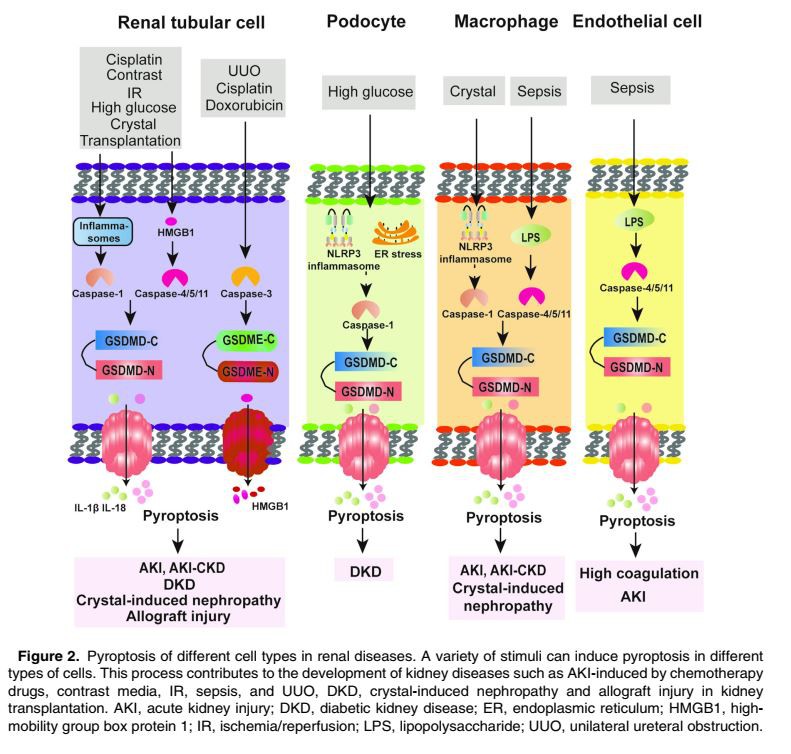
De siste årene har oppdagelsen av pyroptotiske signalveier utvidet vår forståelse av patogenesen av nyresykdommer utover apoptose. Pyroptose, som dukket opp som en effektormekanisme i medfødte immunresponser, ble først observert i makrofager og andre fagocytter.52 Det ble gjort mye arbeid for å bestemme distribusjonen og uttrykket av masterminds, spesielt GSDMD og GSDME, i ulike vev og celletyper, som har demonstrert at pyroptose ikke er begrenset til fagocytter.5 En rekkenyresykdommerindusert av mikrobielle og ikke-mikrobielle stimuli er vanligvis preget av død av nyreceller og aktiverte immunresponser. Noen eksperimenter viste at pyroptose forekommer i fastboende nyreceller og gir et stort bidrag til utviklingen av ulike nyresykdommer. Ytterligere studier har klarlagt at pyroptose i benmargsavledede infiltrerende immunceller, som har blitt utløst av nyrecelledød, kan forverre og opprettholdeskadeavnyre. Nyere forskning har videre påpekt rollen til pyroptose samt relaterte inflammatoriske signalveier i flere typernyresykdommerinkludert akuttnyreskade, diabetisk nyresykdom, krystallindusertnyresykdom, og allograftskade ved nyretransplantasjon. (Tabell 1) (Figur 2)
Akutt nyreskade (AKI)
Celledød er den sentrale patologiske hendelsen under utviklingen av AKI. Apoptose ble tidligere ansett som ansvarlig for AKI-patogenesen.53 Farmakologisk hemming av apoptotiske signalveier klarte imidlertid ikke effektivt å forhindre eller lindre AKI. Nylige fremskritt har avslørt rollen til pyroptose i AKI. I 2018 rapporterte Zhang et al.54 at caspaser-4/5/11 var nødvendig for kontrastindusert tubulær epitelcelledød. De viste videre at disse inflammatoriske kaspasene var ansvarlige for GSDMD- og IL-1b-spaltning i skadede tubulære epitelceller, som avdekket en nødvendig rolle for epitelial pyroptose i kontrastindusert AKI. Miao et al.55 oppdaget et spaltet fragment av GSDMD ved western blot-analyse av helnyrelysater i både cisplatin-induserte og iskemi-reperfusjon-induserte AKI-modeller. Og knockout av caspase-11 eller GSDMD beskyttet musene betydelig fra cisplatinindusert AKI, men denne analysen ble ikke utført i iskemi-reperfusjon (I/R)-modellen. Forfatterne observerte også GSDMD-N-translokasjon til plasmamembranen fremmet av caspase-11. En konstruktiv kommentar til dette arbeidet gjort av Tonnus et al.56 antydet at det mulige målet for GSDMD-N på intracellulære membraner og mer arbeid på den subcellulære distribusjonen av det spaltede fragmentet av GSDMD var nødvendig for å forstå en potensielt viktig dannelse av porer i intracellulære organeller. Ytterligere studier støttet bidraget av GSDMD-mediert pyroptose til AKI indusert av cisplatin.57 Vår forrige studie viste at GSDMD-mediert pyroptose synergiserte med RIPK3/MLKL-mediert nekroptose for å forsterke inflammatorisk signalering og forsterke vevsskade i prosessen med sepsis.58 funnet kumulativ beskyttelse mot sepsis indusert av cecal ligering og punktering i mus etter kombinert sletting av Gsdmd og Ripk3 (eller Mlkl). Disse to formene for nekrose samarbeidet for å bidra til akutt vevsskade inkludert nyre, lunge, lever og tarm, og systemisk koagulasjon i sepsis-dyremodellen. Våre studier på benmargstransplantasjon antydet at nekroptose og pyroptose i både myeloide og ikke-myeloide celler i stor grad bidro til progresjonen av sepsis. Det er en økende interesse for de kombinerte effektene av forskjellige celledødsveier i en enkelt patologisk tilstand.59–61 En annen studie på koagulasjonskaskader i sepsis understreket også den sentrale rollen til caspase-11/GSDMD-mediert pyroptose for initieringen av disseminert intravaskulær koagulasjon (DIC), som gir sterke støttende bevis for våre funn.62 Hemming av TNF-a, så vel som gruppeboksprotein 1 med høy mobilitet (HMGB1), kan utøve negativ kontroll av GSDMD-mediert pyroptose, og gi beskyttende effekter på AKI og akutt leverskade forårsaket av sepsis, som avgrenser denne pyroptotiske veien fra et regulatorisk synspunkt.63
En fersk studie fra vår forskergruppe belyste hvordan GSDME-mediert pyroptose økte utviklingen av ureteral obstruksjon-indusert nyretubuliskade og påfølgende renal fifibrose.64 Vi fant først det oppregulerte uttrykket og aktiveringen av Casp3 og GSDME i den obstruerte nyren i den unilaterale ureteral. obstruksjonsmodell (UUO), noe som antyder involvering av GSDME-mediert pyroptose i denne typen nyreskade. Vi bekreftet deretter at GSDME-mediert pyroptose faktisk var ansvarlig for AKI etter UUO og den påfølgende nefropatien med bruk av Gsdme / og Casp3-/- mus. Studier av benmargstransplantasjon påpekte at GSDME-mediert pyroptose i benmargsavledede infiltrerende immunceller ikke var ansvarlig for patogenesen av obstruktiv nefropati. Renale tubulære celler (RTCs)-spesifikke og hematopoietiske celler-spesifikke caspase-{11}}defisient mus ble generert for ytterligere å bekrefte at GSDME-mediert pyroptose forekommer i RTCs, men ikke i infiltrerende immunceller, hovedsakelig bidrar til progresjonen av nyreskade og fifibrose indusert av ureteral obstruksjon. For å undersøke de inflammatoriske molekylære mekanismene i prosessen, overvåket vi infiltrasjonen av inflammatoriske celler og produksjonen av pro-inflammatoriske cytokiner i nyrene. Resultatene viste at tubulær cellepyroptose kunne fremme HMGB1-sekresjon og rekruttering av makrofager og nøytrofiler etter UUO. Spesielt viste andre studier at GSDME-mediert pyroptose kan bidra til kjemoterapi medikamentindusert nefrotoksisitet.65–66

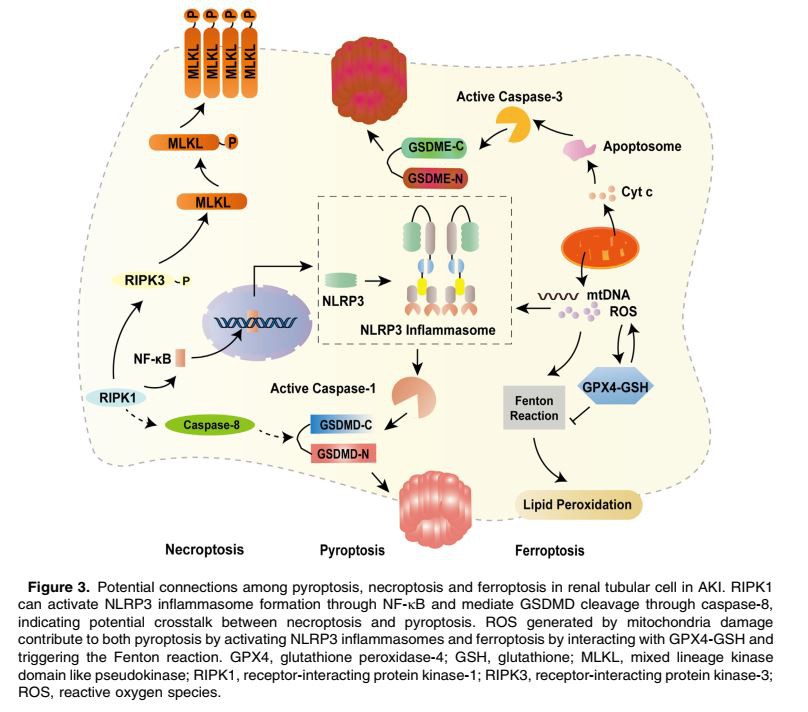
Det er verdt å merke seg at andre lytiske celledødsfall i tillegg til pyroptose også er rapportert å bidra til AKI. I tillegg til samarbeidseffektene av pyroptose og nekroptose i sepsis-indusert AKI nevnt ovenfor, støtter en voksende mengde bevis den sentrale rollen til nekroptose i AKI indusert av visse stimuli. Linkermann et al.67 identifiserte den signifikante rollen til nekroptose i iskemi-reperfusjon-indusert og cisplatin-indusert AKI som RIPK3-knockout-mus, og bruken av RIPK1-kinasehemmernekrostatin (Nec)-1 kunne begge svekke. nyreskade. Vår forskningsgruppe har vist at nekroptose er en viktig mekanisme for proksimal tubulær celledød i cisplatin-indusert nefrotoksisk AKI.68 Våre data viste at hemming av noen av kjernekomponentene i den nekroptotiske veien (RIPK1, RIPK3 eller MLKL) enten ved hjelp av gen knockout eller en kjemisk hemmer, kan redusere cisplatin-indusert proksimal tubuliskade hos mus. Derimot forsterket overekspresjon av RIPK1 eller RIPK3 cisplatinindusert nekroptose in vitro. Vi identifiserte også de essensielle effektene av nekroptose i patofysiologien til IR-skade og påfølgende progresjon til kronisk nyresykdom (CKD), hvor aktivering av NLRP3-inflammasom ble utløst.69 Hvorvidt aktivering av NLRP3 ved nekroptose kan virke oppstrøms for den pyroptotiske veien i AKI er uklart ennå. I tillegg viste flere studier RIPK1 som en signifikant driver for NF-jB-aktivering, en effektiv trigger for NLRP3. I Yersinia-infiserte makrofager utøvde RIPK1 positiv kontroll for caspase-8-indusert GSDMD-spaltning, hvor RIPK3/MLKL-mediert nekroptose ble hemmet.13 Imidlertid RIPK1-kaspase-8-GSDMD-aksen har ikke blitt oppdaget i nyreceller. Ferroptose er rapportert å dominere i visse former for AKI inkludert cisplatinindusert nyreskade70 og rabdomyolyse.71–72 Tonnus et al.73 fant at dysfunksjon av de viktigste ferroptoseovervåkingssystemene ville hypersensibilisere mus til tubulær nekrose under AKI. Martin-Sanchez, D. et al.74 studerte tidspunktet for celledødsveier under utvikling av AKI og fant at ferroptose og nekroptose medierte henholdsvis den første og andre bølgen av celledød i folsyre (FA)-indusert AKI. Det ble vist at ferroptose var ansvarlig for å initiere FA-indusert AKI og nekroptose tillot AKI å vedvare. ROS, produsert i mitokondrier under oksidativ fosforylering eller ved endoplasmatisk retikulum (ER) stress, driver lipidperoksidasjon – kjerneprosessen til ferroptose – og interagerer med glutation (GSH)-glutationperoksidase 4 (GPX4) systemet, som effektivt forhindrer ferroptose. Selv om det er mangel på solid bevis for en detaljert sammenheng mellom ferroptose og andre PCD-er, gir mitokondrierskader og ROS-generering i ferroptose potensielle ledetråder for dens krysstale med nekroptose og pyroptose (figur 3).
Diabetisk nyresykdom (DKD) DKD er en glukosedrevet patogenetisk prosess som forekommer i nyrene til diabetespasienter. Nøkkelfaktorene som regulerer DKD, inkludert overdreven glukosefluks, avanserte glykosyleringssluttprodukter (AGE) og ROS, fungerer som kritiske roller i prosessen med pyroptose, enten som induktorer av inflammasom eller regulatorer av signalveien.75 Blant ulike inflflammasomer som kan indusere pyroptose, har NLRP3 vært under den mest intensive etterforskningen i DKD. Toll-like reseptor (TLR)2 og TLR4, PRR-er oppstrøms for NLRP3-aktivering, kan oppreguleres av høy glukose, og diabetespasienter med nyresvikt viser signifikant økning i TLR2- og TLR4-mRNA-ekspresjon i perifert blod.76 Stimulering av TLR2 og TLR4 er essensielt for NLRP3-aktivering.77–78 Tioredoksininteragerende protein (TXNIP) tilhører tioredoksinsystemet og kan binde seg til tioredoksin (TRX), noe som reduserer TRXs hemmende effekter på oksidativt stress.79 Det er godt etablert at TXNIP-virkning er kritisk for NLRP3-aktivering og celledestruktive responser på forskjellige DAMP-er inkludert pyroptose.80–82 Diabetiske nyrer viser forhøyet ekspresjon av TXNIP og hemming av TXNIP demper nyreskade indusert av høy glukose, og posisjonerer TXNIP som et potensielt mål for DKD-behandling.83,84 ROS har blitt foreslått som et felles signal for NLRP3-aktivering og kan aktivere NLRP3 gjennom forskjellige veier, blant dem er NF-jB-veien den mest omfattende studerte.85 NLRP3 inflammasomer kan effektivt oligomeriseres til sin aktive form gjennom ROS-utløst NF-jB-signalvei.86–88 I DKD ser det ut til at undertrykking av ROS/NF-jB/NLRP3-banen reduserer inflammatoriske responser og kontrollerer utviklingen av progressiv nyre skade.89,90 ER-stress har blitt identifisert som en annen utløser av NLRP3-inflammasom.91,92 Hyperglykemi kan indusere ER-stress i podocytter, tubulære epitelceller og mesangiale celler.93–95 Etter aktivering driver NLRP3 inflammatoriske responser gjennom prosessering av caspase-1, IL-1b og IL-18, som bidrar til DKD-progresjonen. Nyere forskning har gitt bevis for at hemming av NLRP3/caspase-1-mediert pyroptose lindrer patologiske endringer i den diabetiske nyren, noe som tyder på dets terapeutiske potensial i DKD.96–98
Pyroptose i forskjellige nyreboende celler bidrar til utviklingen av DKD. Glomerulær endotelforstyrrelse endrer glomerulær permselektivitet og oppstår i det tidlige stadiet av DKD. Delvis kolokalisering av NLRP3 eller spaltet caspase-1 med glomerulære endotelceller i histologiske seksjoner av diabetiske nyrer hos mennesker eller mus har blitt observert ved konfokal mikroskopi.98 Ytterligere studie bekreftet høy glukose-indusert glomerulær endotelcelleskade via GSDropMD-medier. 99 Podocytter har blitt ansett som det "svakeste leddet" i DKD-utvikling,100, og deres celleantall er sterkt korrelert med albuminuri hos diabetespasienter.101 Tap av podocytter er et samtidig fenomen i progresjonen av DKD, og pyroptose er rapportert til være en av de viktigste mekanismene for tap av podocytter. Genetisk sletting av TXNIP eller inhibering av NADPH-oksidase for å redusere ROS, som begge negativt kontrollerer NLRP3-aktiveringen, svekker betydelig høyglukoseindusert podocyttskade, noe som gir en pekepinn for rollen til pyroptose i diabetisk podocyttap.102 Liu et al.103 fant økt kaspase-1-aktivitet og forhøyede IL-1b- og IL-18-nivåer i podocytter eksponert for høy glukose og Li et al.104 oppdaget spaltet GSDMD-N i høyglukoseskadde podocytter, gir sikrere bevis for pyroptose i den diabetiske podocytten. Det er verdt å nevne at den ikke-kanoniske pyroptotiske banen også bidrar til podocyttskade i DKD med caspase-11/4 involvert i prosessen.105 Selv om det en gang ble antatt at tubulær dysfunksjon oppstod i det senere stadiet av DKD og utviklet seg som et resultat av glomerulær skade ser det ut til at flere og flere undersøkelser utfordrer denne hypotesen, som oppdaget at tubulusskade kan observeres i tidlig stadium av DKD og til og med spille en drivende rolle.106,107 I nyrene til db/db mus og hos HK -2 celler utsatt for høye glukoseforhold, ROS/TXNIP/NLRP3/IL-1b-aksen ble observert å være betydelig oppregulert, og blokkering av denne aksen ville lindre tubulær skade.108 Wang et al.109 oppdaget at TLR4/NF-jB og GSDMD-N uttrykk ble økt i HK-2 celler under høy glukose atmosfære og hemming av TLR4/NF-jB signalisering lindret caspase-1/GSDMD-mediert pyroptose av tubulære celler, som indikerer at pyroptose indusert av TLR4/NF-jB deltok i t diabetisk tubulær skade. Det er bemerkelsesverdig at pyroptose kanskje ikke er den eneste viktige celledødsveien i DKD. Ferroptosis,110 nekroptosis111 og apoptosis112 har blitt undersøkt i mange tilfeller. Imidlertid er tydelig forskjell og/eller kobling mellom forskjellige celledødsveier i DKD-utvikling ikke fullstendig avgrenset.
Krystallindusert nyresykdom
Krystaller kan utløse nyreskader som spenner fra milde/forbigående til alvorlige/irreparable avhengig av lokaliseringen og dynamikken i krystallavsetningen. De molekylære mekanismene til krystallinduserte nyresykdommer forblir stort sett ukjente til tross for betydelig forskningsinnsats. En gjennombruddsstudie viste at krystaller kunne stimulere aktiveringen av NLRP3 og demonstrerte den sentrale rollen til inflammasomet i krystallindusert dysfunksjon eller sykdommer.113 Senere har NLRP3/caspase-1/IL-1b-aksen blitt identifisert som hovedårsaken til utviklingen av oksalatnefropati114 og kalsiumoksalatnefropati,115 som skifter hotspot i forskningen på krystallindusert nyresykdom fra krystallavleiringer til inflammatoriske responser. Krystaller som avsettes i nyrearterier og tubuli kan både aktivere NLRP3-inflammasomet og indusere IL- 1b-avhengig betennelse. Kolesterolkrystall er den vanligste årsaken til renovaskulær skade ved renovaskulær krystallopatier. Dowell et al.116 oppdaget at kolesterolkrystaller kunne aktivere NLRP3-inflammasom og fremme IL-1b-produksjon i makrofager, som er sentralt for patogenesen av krystallindusert aterosklerose. Tubulære krystallopatier, som er et resultat av utfelling av krystaller inne i det tubulære lumen, kan fremme både AKI og kroniske nyrelesjoner.117 NLRP3-inflflammasomer er sterkt korrelert med AKI og CKD forårsaket av tubulær krystallavsetning. Liu et al.118 oppdaget forhøyet ekspresjon av GSDMD og IL-18-ekspresjon i tubulære celler eksponert for kalsiumoksalatkrystaller gjennom væskekromatografi-massespektrometri-basert tandem massetag merking kvantitative proteomiske analyser og identifisert inflammatorisk pyroptose-relatert Gene Ontology og Kyoto Encyclopedia of Genes and Genomes berikelsesanalyser. Ytterligere resultater bekreftet NLRP3-aktivering og GSDMD-avhengig pyroptose i tubulære epitelceller i kalsiumoksalatkrystall-induserte modeller. Ding et al.119 oppdaget også økte proteinnivåer av NLRP3 i nyrehomogenater fra mus med glyoksylatindusert nefrolithiasis og i HK-2-celler eksponert for kalsiumoksalatmonohydratkrystaller. Samtidig økte proteinekspresjonsnivåer av IL-1b og GSDMD ble observert i tubulære epitelceller isolert fra nyrene til glyoksylatbehandlede mus, noe som støtter forestillingen om at krystalleksponerte tubulære celler gjennomgikk GSDMD-avhengig pyroptose. Et stort antall eksperimenter ga bevis for NLRP3-aktivering av krystaller i immunceller, inkludert makrofager og dendrittiske celler på forskjellige måter,120–122 som ble bekreftet i krystallindusert nefropati.115,119 Krystaller som utfelles i tubuli forårsaker også vedvarende stimuli som fremmer utviklingen og progresjon av CKD. Knauf et al.114 viste at NLRP3-IL-1b-aksen ble oppregulert hos mus med oksalatnefropati, mens NLRP3-/- mus var fullstendig beskyttet mot den progressive nyresvikten indusert av fôring med en diett høy i løselig oksalat. En annen banebrytende studie utført av Mulay et al.115 skildret en mer dyptgripende scene der nyresvikt på grunn av oksalatnefropati var sterkt avhengig av NLRP3/ASC/caspase-1/IL-1b-aksen. Likevel har det ikke vært noen direkte påvisning av GSDMD-spaltning i prosessen med krystallassosiert renal fifibrose. Spesielt er det rapportert at andre former for PCD, inkludert RIPK3-MLKL nekroptotisk pathway123,124 og ferroptosis125, bidrar til nyreskade indusert av krystaller. Hvorvidt disse forskjellige celledødsfallene er samarbeidende eller uavhengige er fortsatt under etterforskning. Effekten av krystalltype og dynamikk på den cellulære skjebnen til nyreceller er også av enestående interesse.
Allograftskade ved nyretransplantasjon
Nyretransplantasjon er fortsatt det optimale alternativet for pasienter med nyresykdom i sluttstadiet (ESRD). Gitt den økende befolkningen som har behov for nyretransplantasjon de siste tiårene, har økende oppmerksomhet blitt viet til allograftskade hos både givere og mottakere. HMGB1 kunne frigjøres fra celler som gjennomgår pyroptose.3 Kru¨ger et al.126 fant at tubuli fra avdøde, men ikke levende donorer, farget positivt for HMGB1. De viste videre at HMGB1 kunne stimulere proinflammatoriske responser gjennom TLR4, noe som bidro til transplantatbetennelse og steril skade etter kaldkonservering og transplantasjon. Thierry et al.127 oppdaget forhøyet HMGB1 i urinen så snart som 30 minutter etter reperfusjon etter human nyretransplantasjon og tok for seg dens mulige rolle som medfødte immunformidlere ved slik skade. Inflammatoriske cytokiner IL-1b ble rapportert å øke i hjernedøde organdonorer,128,129, noe som muligens indikerer involvering av pyroptose i prosessen med organskade. Intensiv innsats har blitt gjort av forskere for å studere inflammasomaktivering ved allograft-dysfunksjon. Design et al.130 fant at genetiske varianter i NLRP3-genet påvirker den akutte avstøtingsrisikoen etter nyretransplantasjon. Wu et al.131 demonstrerte at mus med mangel på TLR-adapterproteinet MyD88 ble beskyttet mot både akutt og kronisk allograftavstøtning og økte deres overlevelse etter transplantasjon sammenlignet med villtypekontroller. En annen studie rapporterte at donor MyD88-mangel hemmet inflammatorisk cytokinekspresjon og ER-stress, og var assosiert med forbedret graftfunksjon og forlenget overlevelse av allograft.132 Videre viste en nylig studie at NLRP3-hemmeren Mcc950 kunne lindre tubulær skade og forbedre allograftfunksjonen i en nyre. transplantasjonsmodell. Redusert kaspase-1-aktivering og GSDMD-N-nivåer ble observert etter Mcc950-behandling.133 Disse resultatene gir ledetråder for involvering av pyroptose i allograftskade ved nyretransplantasjon.
Potensielle terapier rettet mot pyroptose for nyresykdom
Hemming av pyroptose Tatt i betraktning den viktige rollen til pyroptose i indre sykdommer, er modulering av denne prosessen av stor bekymring. Potensielle mål i pyroptotikum
pathway inkluderer inflflammasomer, caspases, masterminds og IL-1b (figur 4). Nekroinflammasjon utløst av immunresponser på nekrose inkludert nekroptose, ferroptose og pyroptose fører til vevsskade. Linkermann et al.134,135 fremhevet den kliniske betydningen av å målrette nekroinflammasjon ved nyreskade. Fastslå stimuli kan utløse mer enn én enkelt celledødsvei i skadeceller og vev, potensialet til kombinerte målrettede strategier på forskjellige celledødsveier har tiltrukket seg økt interesse.

Målretting mot NLRP3 inflammasom. NLRP3-inflflammasomer løper oppstrøms for caspase-1/GSDMD-mediert pyroptose, og flere medisiner rettet mot NLRP3 er utviklet med forskjellige hemmende mekanismer.136 Mcc950 er en potent og selektiv småmolekylær hemmer for NLRP3, hvis terapeutiske potensial har blitt vurdert i flere NLRP3-assosierte syndromer.137 I en murin modell av krystallnefropati indusert av dietter rike på oksalat eller adenin, reduserte Mcc950 markant inflammasomaktivering i nyre-dendrittiske celler og påfølgende IL-1b og IL{{13} } produksjon. Denne NLRP3-hemmeren forhindret også effektivt krystallindusert nyrefifibrose.138 BAY 11-7082, som opprinnelig ble rapportert å hemme IjBa-fosforylering og NF jB-aktivering,139 har blitt identifisert som en hemmer av NLRP3 ATPase. Juliana et al.140 belyste at BAY 11-7082 hemmet NLRP3-inflammasomaktivering i LPS-primede makrofager uavhengig av dens effekt på NF-jB og forhindret NLRP3--indusert ASC-pyroptosomdannelse ved å hemme NLRP3 ATPase-aktivitet. Hos mus som ble matet med en diett med høyt fettinnhold og høy fruktose, svekket BAY 11-7082 den diettinduserte økningen i NLRP3-inflammasomekspresjon, noe som resulterte i hemming av caspase-1-aktivering og interleukin (IL){{33} }b og IL-18 produksjon i lever og nyre. Kronisk BAY 11-7082-administrasjon begrenset den diett-induserte nyreskaden betydelig ved å forbedre albumin-til-kreatinin-forholdet.141 I en rottemodell av diabetisk nefropati ble det funnet at BAY 11-7082-behandling signifikant gjenopprettet nyrehistologisk arkitektur og normaliserte nivåer av inflammatoriske cytokiner inkludert IL- 1b, som støtter den renobeskyttende effekten av BAY 11-7082 for DKD.142 b-hydroksybutyrat (BHB), produsert under energimangel eller lavkarbo-diett, hemmet NLRP3-aktivering og forhindret renal fifibrose indusert av nefrokalsinose.143 De beskyttende effektene ble imidlertid ikke nødvendigvis mediert av intrarenal IL-1-frigjøring, og om BHB påvirker pyroptose gjenstår å avklare. Andre NLRP3-hemmere inkludert fluorfenidon144 og tranilast145 har blitt rapportert å spille nybeskyttende roller i den unilaterale ureteral obstruksjon (UUO) modellen mens den molekylære mekanismen som ligger til grunn for pyroptose fortsatt er uklar.
Målretting mot pyroptotiske kaspaser. Hemmere av pyroptotiske kaspaser har vært under intensiv etterforskning. Ac-YVAD-CMK, en caspase-1-hemmer, kan dempe nyrefunksjonssvikt i AKI-rottemodell146 og redusere pyroptose av glomerulære endotelceller i musemodell for diabetisk nefropati.99 VX-765, en annen caspase{{ 6}}-hemmer, var tilstrekkelig til å redusere den proinflammatoriske makrofagpopulasjonen i det senere stadiet av UUO.147 Chu et al.148 viste at det oksiderte fosfolipidet 1-palmitoyl-2-arakidonnoyl-sn-glyserol{{ 13}}fosforylkolin (oxPAPC) kan binde seg direkte til caspase-4 og caspase-11, konkurrere med LPS-binding og følgelig hemme LPS-indusert pyroptose, noe som gir nye bevis for den nøyaktige rollen til oxPAPC i inflammatorisk respons . oxPAPC og dets derivater kan gi ny innsikt for terapier rettet mot ikke-kanonisk pyroptose. Choi et al.149 rapporterte at serpin familie B medlem 1 (SERPINB1) begrenset aktiviteten til caspase-1/4/5/11 ved å undertrykke deres caspase rekrutteringsdomene (CARD) oligomerisering og enzymatisk aktivering, og avslørte en ny sjekkpunktmekanisme for inflammatoriske kaspaser. SERPINB1 samarbeidet med Forkhead box-protein O1 (FoxO1) for å lindre ROS-produksjonsindusert oksidativt stress i DKD.150. Imidlertid er det terapeutiske potensialet ved å målrette mot dette sjekkpunktproteinet fortsatt under utforskning.
Målretting av hjernen. Identifikasjon av masterminds som utøvere av pyroptose gir nytt håp om målrettet terapi av pyroptose-assosierte sykdommer. Hu et al.151 utførte biokjemisk screening med høy gjennomstrømning og identifiserte disulfiram som en effektiv hemmer av GSDMD-poredannelse. En annen studie viste at disulfiram kan forbedre GSDMD-drevet dødelighet ved murin sepsis.152 I tillegg kontrollerer disulfifiram også nekroptose negativt ved å binde MLKL.153 Sikkerhetsprofilen til disulfiram hos mennesker har blitt godt etablert over seks tiår og gjenbruker dette gamle legemidlet for nyrefunksjon. sykdommer er lovende. En GSDMD-avledet hemmer, Ac-FLTD-CMK, kan hemme GSDMD-spaltning av kaspaser-1/4/5/11 ved å binde seg direkte til den katalytiske regionen til disse kaspasene, og undertrykke derfor pyroptose nedstrøms for både kanoniske og ikke-kanoniske veier .154 En studie fra 2020 viste at kalsium (Ca)2 pluss tilstrømning var en forutsetning for funksjonen til GSDMD-N og magnesium (Mg)2 pluss blokkert Ca2 pluss tilstrømning ved å hemme den ATP-styrte Ca2 pluss kanalen P2X7, og dermed hemme funksjonen av GSDMD-N og inhibering av LPS-indusert ikke-kanonisk pyroptose. Disse resultatene antyder potensielle kliniske anvendelser av magnesiumtilskudd for sepsisbehandling.155
Målretting mot IL-1. IL-1 har blitt et forskningshotspot for immunmodulasjonsstrategier rettet mot inflammasomassosierte sykdommer. Spesielt har det humane IL-1b monoklonale antistoffet canakinumab vært under intensiv etterforskning. CANTOS-studien (Canakinumab Anti-Inflammatory Thrombosis Outcomes Study) evaluerte effekten av canakinumab hos 10 061 pasienter med tidligere hjerteinfarkt og et høysensitivt C-reaktivt proteinnivå på 2 mg/L.156 En subanalyse av CANTOS-dataene viste at IL-1b-hemming med canakinumab reduserte hyppigheten av alvorlige kardiovaskulære hendelser blant høyrisikopasienter med aterosklerose med CKD, spesielt blant de med en robust antiinflammatorisk respons på innledende behandling, noe som indikerer nytten av utviklingen av antiinflammatorisk middel i CKD.157
Synkronisert regulering av ulike PCD-er
Nylig har det blitt viet mer oppmerksomhet til krysstale og koordinering av forskjellige PCDer i visse sykdommer. Samarbeidseffekter av GSDMD-mediert pyroptose og MLKL-mediert nekroptose har blitt avslørt i AKI58 og inflammatoriske tarmsykdommer.59 Videre ble et nytt konsept kalt PANoptosis foreslått for å beskrive samreguleringen mellom pyroptose, nekroptose og apoptose og apoptose. bindende protein 1(ZBP1), transformerende vekstfaktor beta-aktivert kinase 1 (TAK1), FS7-assosiert celleoverflateantigen (Fas)-assosiert dødsdomene (FADD) og Caspase-8 kan samarbeide for å fungere som masterregulatorer for PANoptosis i orkestrering av flere celledødsveier.159,59–61 Tonnus et al.73 genererte en kombinert liten molekylhemmer (Nec-1f) som samtidig retter seg mot RIPK1 og ferroptose og beviste sin beskyttende effekt i AKI. Disse funnene legger grunnlaget for effektive terapeutiske tilnærminger til målretting av mangefasetterte celledødsveier ved nyresykdommer.

Konklusjoner
En samling bevis har antydet de avgjørende rollene til pyroptose i nyresykdom og avslørt en rekke faktorer involvert i pyroptose som NLRP3, caspase-1, GSDMDog IL-1, som kan moduleres genetisk og/eller farmakologisk for terapeutisk bruk. Kanonisk GSDMD-mediert pyroptose har vist seg å spille en sentral rolle og har potensialet som et terapeutisk mål ved ulike nyresykdommer, inkludert AKI, DKD, krystallindusert nyresykdom og allograftskade ved nyretransplantasjon. Funn på ikke-kanonisk GSDMD-mediert pyroptose, som stimuleres av LPS, har åpnet en ny vei for behandling av sepsis-indusert organskade. Og den nylige oppdagelsen av GSDME-mediert pyroptose som en nøkkelregulator for AKI og påfølgende AKI-CKD-progresjon gir ny innsikt i håndteringen av AKI og forebygging av CKD. I tillegg kan synkronisert regulering av flere celledødsveier ha mer fordelaktige effekter på nyrene, siden visse stimuli vanligvis induserer mer enn én dødsvei.
Likevel er vår forståelse av pyroptose i sammenheng med nyresykdom fortsatt begrenset. De publiserte studiene om pyroptose ved nyresykdom var basert på et begrenset antall dyre- og celleforsøk. Reproduksjon av gjeldende data samt oversettelse av eksperimentelle data til kliniske omgivelser er fortsatt nødvendig. Innsiktsmekanismene til ulike pyroptotiske veier under ulike stressomstendigheter og/eller i distinkte typer nyreceller, samt krysstale og samspill mellom pyroptose og andre former for celledød, er fortsatt stort sett ukjent. Det er av betydelig betydning å undersøke de pyroptotiske mekanismene ytterligere, så vel som orkestreringen av forskjellige PCD-er i nyrepatofysiologi, noe som vil bidra til å utnytte potensialet til målrettede terapier for å løse de kliniske dilemmaene og bryte den kliniske flaskehalsen ved nyresykdommer.
Fra: 'Pyroptosis in Kidney Disease' avYujia Wang, Yinshuang Li og Yanfang Xu1
---Journal of Molecular Biology
