Vanlig søvn og nyrefunksjon ved kronisk nyresykdom
Mar 06, 2022
Kontakt: emily.li@wecistanche.com
Vanlig søvn og nyrefunksjon ved kronisk nyresykdom: The Chronic Renal Insufficiency Cohort study
KRISTENL. KNUTSON1et al
Nøkkelorddøgnrytmer, nefrologi, proteinuri,nyre
SAMMENDRAG
Fysiologiske bevis tyder på at søvn modulerernyrefunksjon. Målet vårt var å undersøke tverrsnittssammenhengen mellomnyrefunksjonog objektivt estimert vanlig søvnvarighet, kvalitet og timing i en kohort av pasienter med mild til moderat kronisk nyresykdom. Denne studien involverte to amerikanske kliniske sentre avKronisk nyresviktKohortstudie (CRIC), inkludert 432 deltakere i en CRIC-søvnstudie. Vanlig søvnvarighet, kvalitet og timing ble målt ved bruk av håndleddsaktigrafi i 5–7 dager. Validerte søvnskjemaer vurderte subjektiv søvnkvalitet, søvnighet på dagtid og risiko for søvnapné.Nyrefunksjonble vurdert med den estimerte glomerulære filtrasjonshastigheten ved å brukeKronisk nyre sykdomEpidemiologi Samarbeidsligning og forholdet mellom protein og kreatinin i urinen. Lavere estimert glomerulær filtrasjonshastighet var assosiert med kortere søvnvarighet (1,1 mL min -1 1.73 m-2 per time mindre søvn, P=0.03), større søvn fragmentering (2,6 mL min-1 1.73 m-2 per 10 prosent høyere fragmentering,P < 0.001)="" og="" senere="" tidspunkt="" for="" søvn="" (0,9="" ml="" min{{="" 17}}.73="" m-2="" per="" time="" senere,="" p="0.05)." høyere="" protein="" til="" kreatinin-forhold="" var="" også="" assosiert="" med="" større="" søvnfragmentering="" (omtrent="" 28="" prosent="" høyere="" per="" 10="" prosent="" høyere="" fragmentering,="" p="">< 0,001).="" subjektiv="" søvnkvalitet,="" søvnighet="" og="" vedvarende="" snorking="" var="" ikke="" assosiert="" med="" estimert="" glomerulær="" filtrasjonshastighet="" eller="" protein="" til="" kreatinin-forhold.="" dermed="" var="" dårligere="" objektiv="" søvnkvalitet="" assosiert="" med="" en="" lavere="" estimert="" glomerulær="" filtrasjonshastighet="" og="" høyere="" protein="" til="" kreatinin-forhold.="" kortere="" søvnvarighet="" og="" senere="" søvntiming="" var="" også="" assosiert="" med="" en="" lavere="" estimert="" glomerulær="" filtrasjonshastighet.="" leger="" som="" behandler="" pasienter="">Kronisk nyre sykdombør vurdere å forespørre om søvn og eventuelt sende til klinisk søvnvurdering. Longitudinelle og intervensjonelle forsøk er nødvendig for å forstå årsaksretning.

INTRODUKSJON
Over 20 millioner voksne (omtrent 10 prosent av den voksne amerikanske befolkningen) har kroniskenyresykdom(CKD; Coresh et al., 2007; Eckardt et al., 2013). Hemmetnyrefunksjoner assosiert med økt risiko for hjerte- og karsykdommer og aldersjustert dødelighet og, somnyrefunksjonforverres, øker disse risikoene (Eckardt et al., 2013; Gansevoort et al.,2013). Dermed vil identifisering av nye, modifiserbare risikofaktorer assosiert med progresjon av CKD øke vår forståelse av patofysiologien til CKD og potensielt føre til nye terapier for å forhindre eller forsinke sluttstadietnyresykdom(ESRD) og redusere helsebelastningen forbundet med CKD.
En ny risikofaktor kan være utilstrekkelig søvn, inkludert utilstrekkelig søvn, dårlig søvnkvalitet og senere søvntiming. Under normale forhold modulerer søvn i stor grad nøkkelhormonene som er involvert i kontrollen avnyrefunksjon, spesielt de av rennin-angiotensin-aldosteron-systemet, som viser store døgnvariasjoner som er avhengige av søvn (Brandenberger et al., 1994; Charloux et al., 1999; Hurwitz et al., 2004; Turek et al., 2012 ). Normal søvn undertrykker natriumutskillelse i urin (Rubin et al., 1978), og akutt total søvnmangel reduserer den normale nattlige økningen i plasmareninaktivitet (PRA) og aldosteron (Charloux et al., 2001). Søvnkvalitet, uavhengig av søvnvarighet, kan også spille en viktig rolle inyrefunksjonfordi den raske øyebevegelsen (REM)–non(N)REM-syklusen under normal søvn driver en robust ultradian oscillasjon av PRA og aldosteron (Brandenberger et al., 1988, 1994). Eksperimentelle studier som manipulerte søvn eller døgnsystemet har observert betydelige endringer i flere fysiologiske systemer som kan påvirkenyrefunksjon, inkludert økt aktivitet i det sympatiske nervesystemet (Buxton et al., 2010; Spiegel et al., 1999, 2004; Stamatakis og Punjabi, 2010; Tasali et al., 2008), endringer i 24-h-profilene for vekst hormon og kortisol (Buxton et al., 2010; Spiegel et al., 1999, 2000), økt blodtrykk (Sayk et al., 2010; Scheer et al., 2009; Tochikubo et al., 1996) og nedsatt glukose toleranse (Buxton et al., 2010; Leproult et al., 2014; Nedeltcheva et al., 2009; Scheer et al., 2009; Spiegel et al., 1999; Stamatakis og Punjabi, 2010; Tasali et al., 2008). . Gitt disse etablerte assosiasjonene mellom søvn, circadian justering og flere fysiologiske systemer som påvirkernyrefunksjon,det er mulig at vanlige søvnmønstre kan påvirke risikoen og alvorlighetsgraden av CKD.
Tidligere forskning har funnet at selvrapportert vanemessig søvnvarighet er assosiert med utbredt og tilfeldig CKD (Turek et al., 2012). Studier har funnet at forekomsten avnyresykdomellernyrehyperfiltrering var høyere hos de som rapporterte kort søvnvarighet, så vel som hos de som rapporterte lang søvnvarighet sammenlignet med de som sov 7–8 timer per natt (Cheungpasitporn et al., 2016; Kim et al., 2017; Lin et al., 2017; Salifu et al., 2014), selv om en studie bare observerte denne sammenhengen hos kvinner (Choi et al., 2017). Videre var forekomsten av proteinuri større blant personer som rapporterte kortere søvnvarighet (mindre enn eller lik 5 timer per natt) i et utvalg ansatte ved Osaka University i Japan (Yamamoto et al., 2012). Til slutt fant en studie av japanske type 2-diabetespasienter uten CKD at både selvrapporterte korte og lange søvnvarigheter var signifikant assosiert med høyere urin-albumin-kreatinin-forhold (Ohkuma et al., 2013). Hvorvidt søvnkarakteristika er assosiert mednyrefunksjonblant folk som allerede harnyresykdomgjenstår å bestemme.
Målet med denne studien var å undersøke sammenhengen mellom søvn ognyrefunksjon, som vurdert av både den estimerte glomerulære filtrasjonshastigheten (eGFR) og urinprotein til kreatinin ratio (PCR) hos pasienter med mild til moderat CKD. Vanlig søvnvarighet, kvalitet og timing ble objektivt vurdert via aktigrafi og selvrapportering av søvnkvalitet; søvnighet på dagtid og risiko for søvnapné ble innhentet via spørreskjemaer. Vår hypotese var at utilstrekkelig søvn, definert som kortere søvnvarighet, dårligere søvnkvalitet, senere søvntidspunkt eller større søvnighet på dagtid, ville være assosiert med verrenyrefunksjon.
MATERIALER OG METODER
CRIC- og HCRIC-kohorter
DeKronisk nyresviktCohort (CRIC) Study er en prospektiv observasjonsstudie av over 3000 personer med CKD (Feldman et al., 2003). CRIC-studien ble etablert for å forbedre vår forståelse av CKD og dets forhold til hjerte- og karsykdommer og andre komplikasjoner av CKD. Ved påmelding var deltakerne i alderen 21–74 år, hadde en eGFR-verdi over 20 mL min 1 1.73 m 2 og under 50–70 mL min 1 1.73 m 2, avhengig av alder, og ca. 50 prosent hadde type 2 diabetes mellitus. Ekskluderingskriterier inkluderte å være institusjonalisert; har tidligere gjennomgått dialyse i mer enn 1 måned; har en tidligere diagnose av polycystisknyresykdom; etter å ha hatt en organ- eller benmargstransplantasjon; har vært på immunsuppressive medisiner for nyresykdom de siste 6 månedene; kreftkjemoterapi innen 2 år; nåværende deltakelse i en annen forskningsstudie inkludert kliniske studier; har New York Heart Association klasse III eller IV hjertesvikt, cirrhose, HIV-infeksjon eller AIDS, multippelt myelom ellernyrecellekarsinom (Yaffe et al., 2010). CRIC-deltakere ble rekruttert på syv steder over hele USA. Denne tilleggsstudien for søvn rekrutterte forsøkspersoner fra to av disse stedene: University of Illinois, Chicago, Illinois, USA; og Case Western Reserve University, inkludert University Hospital, det tilknyttede MetroHealth System, og Cleveland Clinic, i Cleveland, Ohio, USA. En andre kohort, Hispanic CRIC (HCRIC)-kohorten, ble opprettet for å øke antallet latinamerikanere i studien (Fischer et al., 2011). Inklusjons-/eksklusjonskriteriene og de kliniske evalueringene for HCRIC var identiske med CRIC; HCRIC involverte imidlertid bare ett sted, University of Illinois, Chicago, USA. Deltakere i CRIC- og HCRIC-studiene deltok i årlige kliniske undersøkelser. Vi brukte de kliniske dataene som ble innhentet nærmest søvnvurderingen i våre analyser. Intervallet mellom den kliniske undersøkelsen og søvnvurderingen var 21 dager i gjennomsnitt; 63 prosent av utvalget hadde de to vurderingene innen 90 dager fra hverandre og 92 prosent innen 180 dager.
Institusjonelle vurderingsstyrer ved University of Chicago, University of Illinois, Chicago, USA, og alle tre nettstedene ved Case Western Reserve University, Cleveland, Ohio, USA godkjente protokollen. Alle deltakere ga skriftlig informert samtykke.

Cistanche-nyresykdom symptomer
Målinger
Utfallsmål
Nyrefunksjonble vurdert ved bruk av eGFR og PCR på grunn av deres veletablerte og komplementære roller i å iscenesette CKD og forutsi utfall. Fastende blodprøver ble tatt ved hver klinisk undersøkelse og serumkreatinin ble analysert. En 24-times urinsamling ble også samlet ved hver klinisk undersøkelse, og protein- og kreatininnivåer ble målt. eGFR (mL min 1 1,73 m 2) ble beregnet ved bruk av ChronicNyresykdomEpidemiology Collaboration (CKD-EPI) ligning (Levey et al., 2009). Denne ligningen inkluderer logserumkreatinin (modellert som en 2-skråning lineær spline med kjønnsspesifikke knuter), kjønn, rase og alder på naturlig skala (Levey et al., 2009). Urin PCR (mcg mg 1) ble også beregnet.
Sove
Denne studien inkluderte både objektive estimater av vanlige søvnmønstre ved bruk av håndleddsaktivitetsovervåking og subjektive estimater av søvnkvalitet og søvnighet på dagtid. Vi brukte også et validert screeningsinstrument for å identifisere deltakere som sannsynligvis har søvnapné på grunn av snorkesymptomer.
Deltakerne hadde på seg en aktivitetsmonitor for håndleddet (Actiwatch-16 i CRIC og Actiwatch-2 i HCRIC, Philips/Respironics, Bend OR, USA) kontinuerlig i 5–7 dager for å beregne vanlig søvnvarighet og kvalitet (n { {4}}). Deltakerne i CRIC-studien ble også bedt om å bruke en aktivitetsmonitor (Actiwatch-64, Philips/Respironics, Bend OR, USA) på én fot om natten bare i opptil 3 netter for å beregne periodiske beinbevegelser, og et undersett overholdt og hadde gyldige data. I tillegg fullførte både CRIC- og HCRIC-deltakerne en serie validerte spørreskjemaer for å estimere risikoen for søvnapné, søvnighet på dagtid og subjektiv søvnkvalitet.
Aktivitetsmonitorene inneholder svært følsomme rundstrålende akselerometre som teller bevegelser i 30-s epoker. Håndleddsaktigrafi er validert mot
polysomnografi, som viser en korrelasjon for søvnvarighet mellom {{0}},82 hos insomniacs og 0,97 hos friske personer (Jean-Louis et al., 1997). Vi beregnet flere mål for søvn ved å bruke den tilhørende Actiware-programvaren. Søvnvarighet er mengden tid som brukes på å sove mellom søvnbegynnelse og endelig oppvåkning. Søvnfragmentering er en markør for søvnkvalitet og er en indeks for rastløshet uttrykt i prosent. Den beregnes ved å summere prosentandelen av søvnperioden som brukes på å bevege seg (en 30--epoke med mer enn 2 aktivitetstall anses å bevege seg) og prosentandelen av antall immobile faser (påfølgende 30- epoker uten bevegelse) som varer i bare 1 min eller mindre. Søvnstarttid er tidspunktet for søvnstart og en markør for tidspunktet for søvnperioden. Starttiden for søvn beregnes av programvaren som begynnelsen av den første 10-min. perioden der ikke mer enn én 30--epoke blir scoret som mobil. Fra fotaktigrafien estimerte vi den periodiske benbevegelsesindeksen (PLMI), som er antall benbevegelser per time søvn, ved å bruke Actiware-PLM-programvaren. Vi dikotomiserte deretter denne variabelen til<15 and="" ≥15="" movements="">
Vi administrerte tre validerte spørreskjemaer: Pittsburgh Sleep Quality Index (PSQI), Epworth Sleepiness Scale (ESS) og Berlin-spørreskjemaet. PSQI er et validert {{0}}spørreskjema som vurderer subjektiv søvnkvalitet den siste måneden (Buysse et al., 1989). Poeng varierer fra 0 til 21, og en poengsum på over 5 indikerer dårlig subjektiv søvnkvalitet. ESS er et spørreskjema med åtte elementer som vurderer søvnighet på dagtid (Johns, 1991, 1992). Poeng varierer fra 0 til 24, og en poengsum på over 10 indikerer overdreven søvnighet på dagtid. Til slutt er Berlin-spørreskjemaet et validert screeningverktøy for søvnapné (Netzer et al., 1999). Vanligvis er en deltaker identifisert som høy sannsynlighet for å ha søvnapné hvis to av tre forhold var oppfylt: (1) vedvarende snorkesymptomer; (2) vedvarende dysfunksjon på dagtid eller søvnighet; eller (3) fedme eller hypertensjon. Fordi hypertensjon var tilstede i 95 prosent av denne prøven, brukte vi imidlertid bare 'vedvarende snorkesymptomer' som en indikator på risiko for søvnapné.
Kovariater
Kovariater brukt i disse analysene inkluderer alder, kjønn, rase/etnisitet, kroppsmasseindeks (BMI), nåværende røyker, alkoholbruk og fastende glukosenivå eller tilstedeværelse av diabetes. Fire rase/etniske grupper ble undersøkt: ikke-spansktalende hvit; ikke-spansktalende svart; Hispanic/latino; og annen rase eller etnisitet. BMI (kg m-2) ble beregnet ved hjelp av målt høyde og vekt. Deltakerne ble spurt om de var en nåværende røyker (ja/nei) og om de konsumerte alkohol (ja/nei). Fastende blodprøver ble tatt ved den kliniske undersøkelsen og nivåer av glukose ble målt. Tilstedeværelsen av diabetes ble definert som fastende glukose større enn eller lik 126 mg dL-1, tilfeldig glukose større enn eller lik 200 mg dL-1 eller bruk av insulin eller antidiabetika.

Statistisk analyse
For beskrivende analyser beregnet vi gjennomsnitt og standardavvik for kontinuerlige variabler og prosentene for de kategoriske variablene. Vi undersøkte fordelingen av våre utfallsmål, og PCR ble log-transformert på grunn av en skjev fordeling. Dermed tolkes regresjonskoeffisientene som prosentvis endring per enhetsøkning i søvnmålet. For å teste for assosiasjoner mellom søvnmålene og utfallsmålene, eGFR og PCR, brukte vi separate lineære regresjonsmodeller for hvert utfall og hvert søvnmål. Kovariater i disse innledende modellene inkluderte alder, rase, kjønn, BMI, studiested (Chicago eller Ohio), systolisk blodtrykk og fastende glukose. I tillegg fordi det har vært rapportert om en U-formet assosiasjon mellomnyrefunksjonog søvnvarighet (Lin et al., 2017), la vi til en kvadratisk term for søvnvarighet til modellene for søvnvarighet. For illustrasjonene beregnet vi kvartilene for søvnvarighet, søvnfragmentering og søvnstarttid, og beregnet de marginale middelverdiene for eGFR og PCR for hver kvartil fra regresjonsmodeller som inkluderte kovariatene. Gjennomsnittlig PCR i disse figurene ble tilbaketransformert fra den naturlige loggen brukt i regresjonsmodellene. Til slutt skapte vi interaksjonsbegreper mellom tilstedeværelsen av diabetes og hvert søvnmål som kontinuerlige variabler, og mellom kjønn og hvert søvnmål for å se om assosiasjonene mellom søvn ognyrefunksjonvarierte enten mellom de med og uten diabetes eller mellom menn og kvinner. Alle analyser ble utført ved bruk av Stata SE v14 (StataCorp, College Station, TX, USA).
RESULTATER
68 deltakere utviklet ESRD før søvnvurderingen og ble derfor ekskludert fra disse analysene (fig. 1). I tillegg ekskluderte vi deltakere som manglet nøkkeldata og som hadde en eGFR<10 or="">80 mL min-1 1.73 m-2. Our final sample size was 432 patients. The description of the sample is presented in Table 1. The average age was approximately 60 years and 61% of the sample was obese (BMI≥30 kg m-2). Almost half of the participants were women, and half of the sample had diabetes. On average, these patients slept for 6.5 h per night, but this ranged from about 2 h per night to 10 h per night. Patients went to bed at 23:30 hours on average. Of those with foot actigraphy, 20% had a PLMI at or above 15 movements perh. Nearly two-thirds of the participants had PSQI scores above the clinical threshold for poor sleep quality (score >5), og mer enn 25 prosent hadde ESS-score over den kliniske terskelen for overdreven søvnighet på dagtid. Omtrent en fjerdedel av prøven hadde vedvarende snorking. Videre kvalifiserte 80 prosent av deltakerne for minst ett av følgende: dårlig subjektiv søvnkvalitet (PSQI > 5); overdreven søvnighet på dagtid (ESS > 10); eller vedvarende snorking.

Mange av søvnmålene var korrelert, om enn bare svakt eller beskjedent. For eksempel var kortere søvnvarighet assosiert med større søvnfragmentering (r {{0}}.39,P < 0.{{10}}{{2{{24="" }}}}1)="" og="" senere="" starttid="" for="" søvn="" (r="0.36,P">< 0.001).="" høyere="" plmi="" var="" assosiert="" med="" større="" søvnfragmentering="" (r="0.28," p="">< 0.001).="" høyere="" psqi-score="" var="" assosiert="" med="" større="" søvnfragmentering="" (r="0.16," p="0.001)," men="" ikke="" med="" søvnvarighet="" eller="" søvntiming="" (begge="" p=""> 0.05). Større subjektiv søvnighet var assosiert med kortere søvnvarighet (r=0.30, P < 0.001),="" større="" søvnfragmentering="" (r="0.16," p="">< 0.001)="" og="" senere="" søvntiming="" (r="" {{26="" }}.13,="" p="">
Sammenheng mellom søvn og eGFR
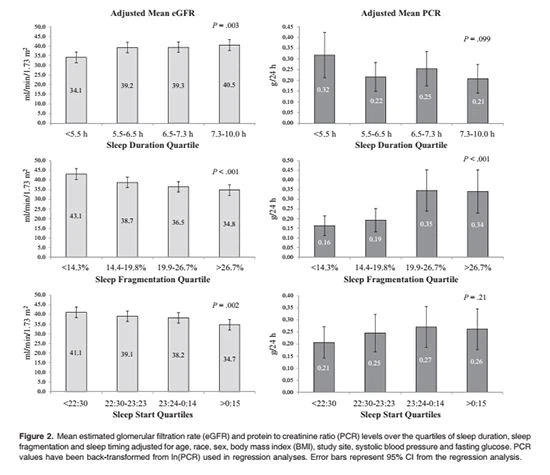
Figur 2 viser de justerte gjennomsnittene for eGFR for kvartilene for søvnvarighet, søvnfragmentering og søvntiming. Resultater fra multivariable lineære regresjonsanalyser som forutsier eGFR er presentert i tabell 2. Lavere eGFR var assosiert med kortere søvnvarighet (1,1 mL min-1∙1,73 m-2 per time mindre søvn), større søvnfragmentering (2,6) mL min{{10}},73 m-2 per 10 prosent høyere søvnfragmentering) og senere søvntiming (0,9 mL min-1∙1,73 m-2 per time seinere). Subjektiv søvnkvalitet, subjektiv søvnighet, PLMI og vedvarende snorking var ikke assosiert med eGFR. Den kvadratiske termen for søvnvarighet var ikke signifikant (P=0.30), noe som indikerer fravær av en U-formet assosiasjon mellom søvnvarighet og eGFR.
Sammenheng mellom søvn og PCR
Figur 2 viser også de ujusterte assosiasjonene mellom fordelingen av PCR og kvartilene for søvnvarighet, søvnfragmentering og søvntiming. Median PCR var signifikant høyere hos de med større søvnfragmentering, men det var ingen signifikant sammenheng mellom PCR og søvnvarighet eller kvartiler for søvntiming. I de lineære regresjonsmodellene (tabell 2) var PCR bare assosiert med større søvnfragmentering (omtrent 28 prosent høyere PCR per 10 prosent høyere søvnfragmentering). Vanlig søvnvarighet, den kvadratiske betegnelsen for søvnvarighet, søvnstarttid, PLMI, subjektiv søvnkvalitet, søvnighet og vedvarende snorking var ikke assosiert med PCR.

Vi undersøkte om sammenhengene mellom målene for søvn og målene fornyrefunksjonvariert etter diabetesstatus eller kjønn ved å teste interaksjonsbegreper i hver av modellene. Interaksjonsbegrepet mellom diabetes og PLMI ble ansett som signifikant assosiert med eGFR og i PCR (P < {{0}}.10).="" det="" ble="" derfor="" utført="" stratifiserte="" analyser="" for="" disse="" modellene.="" blant="" pasienter="" med="" ckd="" uten="" diabetes="" var="" det="" å="" ha="" en="" plmi="" større="" enn="" eller="" lik="" 15="" hendelser="" per="" time="" assosiert="" med="" lavere="" egfr="" (beta="3.8" ml="" min-1="" 1.73="" m-2,="" p="0.2," n="154)" og="" en="" høyere="" pcr="" (omtrent="" 28="" prosent="" høyere,p="0.36," n="141)," selv="" om="" ingen="" av="" assosiasjonene="" var="" signifikante.="" blant="" pasienter="" med="" ckd="" med="" diabetes="" var="" plmi="" større="" enn="" eller="" lik="" 15="" hendelser="" per="" time="" assosiert="" med="" høyere="" egfr="" (beta="4.0" ml="" min-1="" 1.73="" m-2,="" p="0.1," n="136)" og="" lavere="" pcr="" (omtrent="" 63="" prosent="" lavere,="" p="0.07," n="126)," men="" ingen="" av="" assosiasjonene="" nådde="" statistisk="" signifikans.="" diabetesinteraksjonsbegrepene="" i="" alle="" andre="" modeller="" var="" ikke="" signifikante,="" og="" ingen="" av="" interaksjonsbegrepene="" med="" kjønn="" var="" signifikante="" (alle="" p=""> 0,10).

DISKUSJON
I dette utvalget av pasienter med CKD før dialyse var større søvnfragmentering assosiert med verrenyrefunksjon, som representert ved både eGFR og urin-PCR. Kortere søvnvarighet og senere søvntiming var også assosiert med lavere eGFR, men ikke PCR. Subjektiv søvnkvalitet, søvnighet og vedvarende snorking (et symptom på søvnapné) var ikke assosiert mednyrefunksjonmålinger.
Vår studie fant at redusert søvnkvalitet, som representert ved større søvnfragmentering, var assosiert med redusert eGFR og økt PCR. Eksperimentelt indusert søvnfragmentering hos unge friske voksne reduserte insulinfølsomheten, svekket glukosemetabolisme og svekket nattlig blodtrykksfall (Sayk et al., 2010; Stamatakis og Punjabi, 2010; Tasali et al., 2008), som er risikofaktorer for utvikling av diabetes og hypertensjon. Diabetes og hypertensjon er i sin tur store risikofaktorer for utvikling av CKD (Centers for Disease and Prevention, 2007). Videre førte eksperimentell søvnfragmentering til en økning på 14 prosent i hjerte sympathovagal balanse, noe som tyder på et skifte mot høyere sympatisk aktivitet (Tasali et al., 2008). Hvis sympatisk nervøs aktivitet er forhøyet på grunn av vanlig søvnfragmentering, kan dette svekkenyrefunksjon(Masuo et al., 2010). Dessverre har tidligere eksperimentelle studier som manipulerte søvnvarighet eller kvalitet ikke undersøkt effekter på nyrefunksjonsmål. En annen observasjonsstudie brukte aktigrafi og estimert søvnfragmentering (Agarwal og Light, 2011). De fant ingen sammenheng mellom søvnfragmentering og eGFR; denne analysen inkluderte imidlertid bare 27 pasienter med CKD.
Et toveis forhold mellom søvnvarighet og kvalitet ognyrefunksjoner mulig. Bare noen få studier har dokumentert søvnkvalitet og varighet ved CKD før nyresvikt. Bevis tyder på at søvnforstyrrelser ved CKD kan være en forløper for de mer alvorlige søvnforstyrrelsene beskrevet i ESRD (Turek et al., 2012). Studier som brukte aktigrafi rapporterte at individer med ESRD hadde mer forstyrret søvn enn individer med CKD (Agarwal og Light, 2011; Barmar et al., 2009). Forhøyet aktivitet i det sympatiske nervesystemet kan føre til fragmentert søvn, og omvendt er fragmentert søvn assosiert med aktivering av det sympatiske nervesystemet. Dette toveisforholdet kan utgjøre en ond sirkel der søvnproblemer og redusert nyrefunksjon forsterker hverandre.
Funnet som senere sover timing er assosiert mednyrefunksjoner en ny oppdagelse og den kan ha sammenheng med døgnrytmer. En mulig forklaring på sammenhengen mellom søvntiming og nyrefunksjon er cirkadisk feiljustering mellom endogene klokker. Cirkadisk feiljustering kan oppstå når atferd som søvn og måltider oppstår til tider som ikke er synkroniserte med våre endogene klokker, og derfor reagerer ikke nøkkelorgansystemer riktig eller fungerer effektivt. Circadian klokker innnyreceller ser ut til å spille en viktig rolle i reguleringen av væskenivåer og blodtrykkshomeostase (Tokonami et al., 2014), så hvis det er desynkroni mellom døgnrytmene i nyrene og atferd som søvn, er det mulig at forstyrrelser i nyrefunksjon kan oppstå. En ytterligere mulig forklaring på sammenhengen mellom senere søvntiming og dårligere nyrefunksjon innebærer melatoninfrigjøring. Melatonin er et hormon som hovedsakelig skilles ut av pinealkjertelen, og denne sekresjonen hemmes av lys. Personer som holder seg oppe senere vil bli utsatt for kunstig lys om natten, og fordi lys undertrykker melatonin, kan melatoninnivået være lavere hos senere sovende. Melatonin har antioksidantegenskaper og administrering av melatoninbeskyttede nyreallotransplantater fra iskemi/reperfusjonsskade-indusert nyredysfunksjon og tubulær skade i en dyremodell (Li et al., 2009). En fersk studie på overvektige mus (Ob/Ob) fant at melatoninadministrasjon var assosiert med gunstige endringer inyreproksimale kronglete tubuli, noe som tyder på at melatonin kan være beskyttende motnyremorfologisk skade og dysfunksjon på grunn av overvekt (Stacchiotti et al., 2014).Styrken til denne studien inkluderer objektive estimater av søvnvarighet, kvalitet og timing, det store og etnisk mangfoldige utvalget. Det er imidlertid noen begrensninger å merke seg. Denne studien hadde ikke et objektivt mål på obstruktiv søvnapné (OSA), og OSA kan være assosiert med verrenyrefunksjonhos pasienter med CKD (Pierratos og Hanly, 2011), selv om ikke alle studier har observert disse assosiasjonene (Fornadi et al., 2014). Mens vi brukte et validert screeningsverktøy for å identifisere pasienter med vedvarende snorking, et hovedsymptom på søvnapné, er det mulig at forekomsten av apné ble undervurdert. Tidligere epidemiologiske data antydet at variasjon fra år til år i søvnvarighet og kvalitet er ganske lav hos middelaldrende voksne (Knutson et al., 2007), selv om stabiliteten til søvnvaner hos pasienter med CKD ikke har blitt undersøkt. Til slutt er studiedesignet tverrsnitt, og effektretningen kan ikke bestemmes. Vår studie fant signifikante assosiasjoner mellom dårligere søvnkvalitet, som indikert av større søvnfragmentering, og redusertnyrefunksjon(enten lavere eGFR eller høyere PCR). Kortere søvnvarighet og senere søvntiming var også assosiert med dårligere nyrefunksjon som indikert av lavere eGFR. Fremtidig forskning bør bruke longitudinelle og intervensjonelle design for å avgjøre om dårlig søvnkvalitet eller circadian forstyrrelse kan svekkenyrefunksjon. Leger som behandler pasienter med CKD bør vurdere å spørre om søvn og eventuelt sende til klinisk søvnvurdering. Viktigere, fremtidig forskning bør undersøke om forbedring av søvnkvalitet og/eller optimalisering av døgnrytmer hos pasienter med CKD kan bremse utviklingen av CKD.
TAKK
Finansiering til CRIC-studien ble oppnådd under en samarbeidsavtale fra US National Institute of Diabetes and Digestive and Kidney Diseases (U01DK060990, U01DK060984, U01DK061022, U01DK061021, U01DK061028, U01DK061060, U01DK06, U01DK06, U01DK060, U01DK060, U01DK0606 og U01DK061028, U01DK0601060, U01DK0601060 og UDK106061060, U01DK061028, U01DK061028, U01DK060 og UDK06060606, U01DK0606 og UDK060606. Finansiering for CRIC-søvnstøttestudien ble oppnådd gjennom en pris fra National Institutes of Health (R01DK0716960). I tillegg ble dette arbeidet delvis støttet av Clinical and Translational Science Collaborative of Cleveland, UL1TR000439 fra National Center for Advancing Translational Sciences (NCATS)-komponenten av National Institutes of Health og NIH Roadmap for Medical Research, University of Illinois ved Chicago CTSAUL1RR029879. Dr. Knutson støttes også av NIDDK R01DK095207. Dr. Lash er finansiert av NIDDK K24D K092290. Dr. Ricardo er finansiert av NIDDK K23DK094829. Disse finansierne spilte ingen rolle i studiedesign, datainnsamling, dataanalyse, datatolkning eller manuskriptforberedelse.
FORFATTERBIDRAG
Forskningside og studiedesign: KLK, JL, JH, JDT, MR, LJA, LAB, MKT, SPS, MRW, EVC; datainnsamling: KLK, ACR, NT, JC; dataanalyse/tolkning: KLK, JL, ACR, EVC; statistisk analyse: KLK. Hver forfatter bidro med viktig intellektuelt innhold under manuskriptutforming eller revisjon og aksepterer ansvarlighet for det overordnede arbeidet ved å sikre at spørsmål knyttet til nøyaktigheten eller integriteten til en del av arbeidet blir undersøkt og løst på riktig måte. KLK tar ansvar for at denne studien er rapportert ærlig, nøyaktig og transparent; at ingen viktige aspekter ved studien er utelatt; og at eventuelle avvik fra studien som planlagt er forklart.
INTERESSEKONFLIKT
Kristen L. Knutson: National Sleep Foundation Poll Fellow; James Lash: ingen; Ana C. Ricardo: ingen; James Herdegen: ingen; J. Daryl Thornton: ingen; Mahboob Rahman: ingen; Nicolas Turek: ingen; Janet Cohan: ingen; Lawrence J. Appel: ingen; Lydia A. Bazzano: ingen; Manjula Kurella Tamura: ingen; Susan P. Steigerwalt: PI for en Medtronic SPYRAL-prøve (men ingen direkte kompensasjon til henne); Matthew R. Weir: ad hoc vitenskapelig rådgiver for Janssen, Astra Zeneca, Boehringer Ingelheim, MSD, Boston Scientific, Sanofi; Eve Van Cauter: konsulent for Philips/Respironics for enheter som kan forbedre søvnkvaliteten, etterforsker-initiert støtte fra Merck og Astra-Zeneca.
REFERANSER
Agarwal, R. og Light, RP Søvn og aktivitet ved kronisk nyresykdom: en longitudinell studie. Clin. J. Am. Soc. Nephrol., 2011, 6:1258–1265.
Barmar, B., Dang, Q., Isquith, D., Buysse, D. og Unruh, M. Sammenligning av søvn-/våkenatferd i CKD-stadier 4 til 5 og hemodialysepopulasjoner ved bruk av håndleddsaktigrafi. Er. J. Kidney Dis., 2009, 53: 665–672.
Brandenberger, G., Follenius, M., Simon, C., Ehrhart, J. og Libert, JP Nattlige svingninger i plasmareninaktivitet og REM-NREM-søvnsykluser hos mennesker: en vanlig reguleringsmekanisme? Sleep, 1988, 11: 242–250.
Brandenberger, G., Follenius, M., Goichot, B., Saini, J., Ehrhart, J. og Simon, C. Tjuefiretimers profiler av plasmareninaktivitet i forhold til søvn-våkne-syklusen. J. Hypertens., 1994, 12: 277-283.
Buxton, OM, Pavlova, M., Reid, EW, Wang, W., Simonson, DC og Adler, GK. Søvnrestriksjon i 1 uke reduserer insulinfølsomheten hos friske menn. Diabetes, 2010, 59: 2126–2133.
Buysse, DJ, Reynolds, CF 3rd, Monk, TH, Berman, SR og Kupfer, DJ The Pittsburgh Sleep Quality Index: et nytt instrument for psykiatrisk praksis og forskning. Psychiatry Res., 1989, 28:193–213.
Centers for Disease and Prevention Prevalens av kronisk nyresykdom og assosierte risikofaktorer - USA, 1999–2004. Morb. Dødelig. Wkly Rep., 2007, 56: 161–165.
Charloux, A., Gronfier, C., Lonsdorfer-Wolf, E., Piquard, F. og Brandenberger, G. Aldosteronfrigjøring under søvn-våkne-syklusen hos mennesker. Er. J. Physiol., 1999, 276: E43–E49.
Charloux, A., Gronfier, C., Chapotot, F., Ehrhart, J., Piquard, F. og Brandenberger, G. Søvnmangel gjør natteøkningen i aldosteronfrigjøring hos mennesker sløvet. J. Sleep Res., 2001, 10: 27–33.
Cheungpasitporn, W., Thongprayoon, C., Gonzalez-Suarez, ML et al. Effektene av kort søvnvarighet på proteinuri og kronisk nyresykdom: en systematisk gjennomgang og metaanalyse. Nephrol.Dial. Transplant., 2016, 32: 991–996
Choi, H., Kim, HC, Lee, JY, Lee, JM, Choi, DP og Suh, I. Søvnvarighet og kronisk nyresykdom: Korean Genome and Epidemiology Study (KoGES)-Kangwha-studien. Koreanske J. Intern. Med., 2017, 32: 323–334.
Coresh, J., Selvin, E., Stevens, LA et al. Forekomst av kronisk nyresykdom i USA. JAMA, 2007, 298: 2038–2047.
Eckardt, KU, Coresh, J., Devuyst, O. et al. Utviklende betydning av nyresykdom: fra subspesialitet til global helsebyrde. Lancet, 2013, 382: 158–169.
Feldman, HI, Appel, LJ, Chertow, GM et al. The ChronicNyreinsuffisiensKohort (CRIC) Studie: design og metoder. J. Am. Soc. Nephrol., 2003, 14: S148–S153.
Fischer, MJ, Go, AS, Lora, CM et al. CKD hos latinamerikanere: grunnlinjekarakteristikker fra CRIC (Kronisk nyresviktCohort) og Hispanic-CRIC-studier. Er. J. Kidney Dis., 2011, 58: 214–227.
Fornadi, K., Ronai, KZ, Turanyi, CZ et al. Søvnapné er ikke assosiert med verre utfall hos nyretransplanterte. Sci. Rep., 2014, 4: 6987.
Gansevoort, RT, Correa-Rotter, R., Hemmelgarn, BR et al. Kronisk nyresykdom og kardiovaskulær risiko: epidemiologi, mekanismer og forebygging. Lancet, 2013, 382: 339–352.
Hurwitz, S., Cohen, RJ og Williams, GH Daglig variasjon av aldosteron- og plasmareninaktivitet: tidsforhold til melatonin og kortisol og konsistens etter langvarig sengeleie. J. Appl. Physiol., 2004: 1406–1414.
Jean-Louis, G., Von Gizycki, H., Zizi, F., Spielman, A., Hauri, P. og Taub, H. Actigraph-dataanalyseprogramvaren: I. A novel approach to scoring and interpreting sleep-wave aktivitet. Percept. Mot. Skills, 1997, 85: 207–216.
Johns, MW En ny metode for å måle søvnighet på dagtid: Epworth Sleepiness Scale. Søvn, 1991, 14: 540–545.
Johns, MW Pålitelighet og faktoranalyse av Epworth Sleepiness Scale. Søvn, 1992, 15: 376–381.
Kim, CW, Chang, Y., Sung, E. et al. Søvnvarighet og kvalitet i forhold til kronisk nyresykdom og glomerulær hyperfiltrasjon hos friske menn og kvinner. PLoS ONE, 2017, 12: e0175298.
Knutson, KL, Rathouz, PJ, Yan, LL, Liu, K. og Lauderdale, DS Intra-individuell daglig og årlig variasjon i aktigrafisk registrerte søvnmål: CARDIA-studien. Sleep, 2007, 30:793–796.
Leproult, R., Holmback, U. og Van Cauter, E. Circadian feilstilling forsterker markører for insulinresistens og betennelse, uavhengig av søvntap. Diabetes, 2014, 63: 1860–1869.
Levey, AS, Stevens, LA, Schmid, CH et al. En ny ligning for å estimere glomerulær filtrasjonshastighet. Ann. Turnuskandidat. Med., 2009, 150:604–612.
Li, Z., Nickkholgh, A., Yi, X. et al. Melatonin beskytter nyretransplantater fra iskemi/reperfusjonsskade gjennom hemming av NF-kB og apoptose etter eksperimentell nyretransplantasjon. J. Pineal Res., 2009, 46: 365–372.
Lin, M., Su, Q., Wen, J. et al. Selvrapportert søvnvarighet og lur på dagtid er assosiert mednyrehyperfiltrering i befolkningen generelt. Sleep Breath, 2017, https://doi.org/10.1007/s11325-017-1470-0 (Epub foran trykt).
Masuo, K., Lambert, GW, Esler, MD, Rakugi, H., Ogihara, T. og Schlaich, MP Rollen til sympatisk nervøs aktivitet inyreskade og sluttstadiumnyresykdom. Hypertens. Res., 2010, 33:521–528.
Nedeltcheva, AV, Kessler, L., Imperial, J. og Penev, PD. Eksponering for tilbakevendende søvnbegrensninger ved høyt kaloriinntak og fysisk inaktivitet resulterer i økt insulinresistens og redusert glukosetoleranse. J. Clin. Endokrinol. Metab., 2009,94: 3242–3250.
Netzer, N., Stoohs, R., Netzer, C., Clark, K., og Strohl, K. Bruke Berlin-spørreskjemaet for å identifisere pasienter med risiko for søvnapné-syndromet. Ann. Turnuskandidat. Med., 1999, 131: 485-491.
Ohkuma, T., Fujii, H., Iwase, M. et al. Sammenheng mellom søvnvarighet og utskillelse av albumin i urin hos pasienter med type 2 diabetes: Fukuoka Diabetes Registry. PLoS ONE, 2013, 8:e78968.
Pierratos, A. og Hanly, PJ Søvnforstyrrelser over hele spekteret av kronisk nyresykdom. Blood Purif., 2011, 31: 146–150.
Rubin, RT, Polen, RE, Gouin, PR og Tower, BB Utskillelse av hormoner som påvirker vann- og elektrolyttbalansen (antidiuretisk hormon, aldosteron, prolaktin) under søvn hos normale voksne menn.Psykosom. Med., 1978, 40: 44–59.
Salifu, I., Tedla, F., Pandey, A. et al. Søvnvarighet og kronisk nyresykdom: analyse av den nasjonale helseintervjuundersøkelsen. Cardiorenal Med., 2014, 4: 210–216.
Sayk, F., Teckentrup, C., Becker, C. et al. Effekter av selektiv slow-wave søvnmangel på nattlig blodtrykksfall og dagtid blodtrykksregulering. Er. J. Physiol. Regul. Integr. Comp. Physiol., 2010, 298: R191–R197.
Scheer, FA, Hilton, MF, Mantzoros, CS og Shea, SA Uønskede metabolske og kardiovaskulære konsekvenser av circadian feilstilling. Proc. Natl Acad. Sci. USA, 2009, 106: 4453–4458.
Spiegel, K., Leproult, R., og Van Cauter, E. Effekten av søvngjeld på metabolsk og endokrin funksjon. Lancet, 1999, 354: 1435–1439.
Spiegel, K., Leproult, R., Colecchia, EF et al. Tilpasning av 24-h veksthormonprofilen til en tilstand av søvngjeld. Er. J. Physiol. Regul. Heltall. Comp. Physiol., 2000, 279: R874–R883.
Spiegel, K., Leproult, R., L'hermite-Baleriaux, M., Copinschi, G., Penev, PD og Van Cauter, E. Leptinnivåer er avhengig av søvnvarighet: forhold med sympathovagal balanse, karbohydratregulering, kortisol og tyrotropin. J. Clin. Endocrinol.Metab., 2004, 89: 5762–5771.
Stacchiotti, A., Favero, G., Giugno, L. et al. Mitokondriell og metabolsk dysfunksjon inyrekronglete tubuli av overvektige mus: beskyttende rolle for melatonin. PLoS ONE, 2014, 9: e111141.
Stamatakis, KA og Punjabi, NM Effekter av søvnfragmentering på glukosemetabolisme hos normale personer. Chest, 2010, 137: 95–101.
Tasali, E., Leproult, R., Ehrmann, DA og Van Cauter, E. Slowwave sleep and the risk of type 2 diabetes in people. Proc. Natl Acad. Sci. USA, 2008, 105: 1044–1049.
Tochikubo, O., Ikeda, A., Miyajima, E. og Ishii, M. Effekter av utilstrekkelig søvn på blodtrykket overvåket av en ny multi-biomedisinsk opptaker. Hypertensjon, 1996, 27: 1318-1324.
Tokonami, N., Mordasini, D., Pradervand, S. et al. Lokaltnyredøgnklokker kontrollerer væske-elektrolytt homeostase og BP. Syltetøy. Soc. Nephrol., 2014, 25: 1430–1439.
Turek, NF, Ricardo, AC og Lash, JP Søvnforstyrrelser som utradisjonelle risikofaktorer for utvikling og progresjon av CKD: en gjennomgang av bevisene. Er. J. Kidney Dis., 2012, 60: 823–833.
Yaffe, K., Ackerson, L., Kurella Tamura, M. et al.Kronisk nyre sykdomog kognitiv funksjon hos eldre voksne: funn frakronisk nyresviktkohort kognitiv studie. J. Am. Geriatr. Soc., 2010, 58: 338–345.
Yamamoto, R., Nagasawa, Y., Iwatani, H. et al. Selvrapportert søvnvarighet og prediksjon av proteinuri: en retrospektiv kohortstudie. Er. J. Kidney Dis., 2012, 59: 343–355.

